
Wetenschap
Wetenschappers schakelen bakkersgist in op jacht naar nieuwe medicijnen
Gistcellen gelabeld met kleurrijke fluorescerende markers worden getoond. Krediet:Wikimedia Commons (publiek domein)
Een van de moeilijkste onderdelen van het ontdekken van medicijnen is om vast te stellen hoe een medicijn daadwerkelijk in het lichaam werkt. Het duurde bijna 100 jaar om het moleculaire doelwit van aspirine te ontdekken, maar zelfs met de allernieuwste technologie, het kan jaren duren om te ontrafelen hoe medicijnen cellen beïnvloeden. En toch, om medicijnen te ontwikkelen die effectief op ziekten zijn gericht en veilig zijn - zonder bijwerkingen - zijn deze moleculaire inzichten essentieel.
Nu heeft een nieuwe methode ontwikkeld door een internationaal onderzoeksteam het potentieel om het ontdekken van doelwitten te versnellen met behulp van gistcellen, die een eenvoudigere versie van menselijke cellen zijn, maar veel beter bekend op moleculair niveau.
Teams onder leiding van professoren Charles Boone, een professor in moleculaire genetica aan het Donnelly Centre van de Universiteit van Toronto, Tsjaad Myers, van de Universiteit van Minnesota-Twin Cities, en professoren Minoru Yoshida en Hiroyuki Osada, van het RIKEN Center for Sustainable Resource Science in Japan, ontwikkelde een nieuwe chemische genetische benadering om een medicijn te koppelen aan een cellulair proces waarop het inwerkt.
Boone en Myers zijn ook fellows bij het Canadian Institute for Advanced Research, waar Boone Senior Fellow en mededirecteur van het Genetics Networks-programma is.
De studie, gepubliceerd in het tijdschrift Natuur Chemische Biologie , getest hoe bijna 14, 000 verbindingen, waarvan honderden voorheen onontgonnen waren, invloed hebben op basale cellulaire processen, om medicijnfabrikanten te waarschuwen voor chemicaliën die het meest waarschijnlijk een bepaalde ziekte aantasten. De gegevens wezen op ~1000 chemicaliën, waarvan vele natuurlijke producten zijn afgeleid van bodemmicroben, als een rijke bron van potentiële medicijnen tegen een groot aantal ziekten, inclusief infecties, Alzheimer en kanker.
Ondanks de moderne technologie, de ontdekking van geneesmiddelen berust nog steeds grotendeels op giswerk. Om een medicijn te vinden dat zeggen, doodt kankercellen, wetenschappers doorzoeken bibliotheken die duizenden chemische verbindingen bevatten, waarvan de meeste helemaal geen effect zullen hebben.
"Er zijn veel verschillende soorten bibliotheken om uit te kiezen. Vaak kiest u een bibliotheek op basis van beschikbaarheid of kosten, geen enkele vorm van functionele informatie, en zo wordt het een schot in het duister, " zegt Dr. Jeff Piotrowski, een hoofdauteur van de krant die een postdoctoraal onderzoeker was in zowel het Yoshida- als het Boone-lab en nu werkt bij het biotechnologiebedrijf in Boston, Yumanity-therapieën, die gistcellen gebruikt om medicijnen voor neurodegeneratieve ziekten te vinden.
Met hun platform voor chemische genetica, Piotrowski en collega's konden laten zien welke delen van de cel het doelwit zijn van duizenden verbindingen uit zeven verschillende bibliotheken, zes daarvan zijn uitgebreid onderzocht en omvatten collecties van het National Cancer Institute (NCI), het National Institute of Health en het farmaceutische bedrijf Glaxo-Smith-Kline. De zevende en grootste collectie, van RIKEN in Japan, herbergt duizenden vrijwel onontgonnen natuurlijke producten van bodemmicroben.
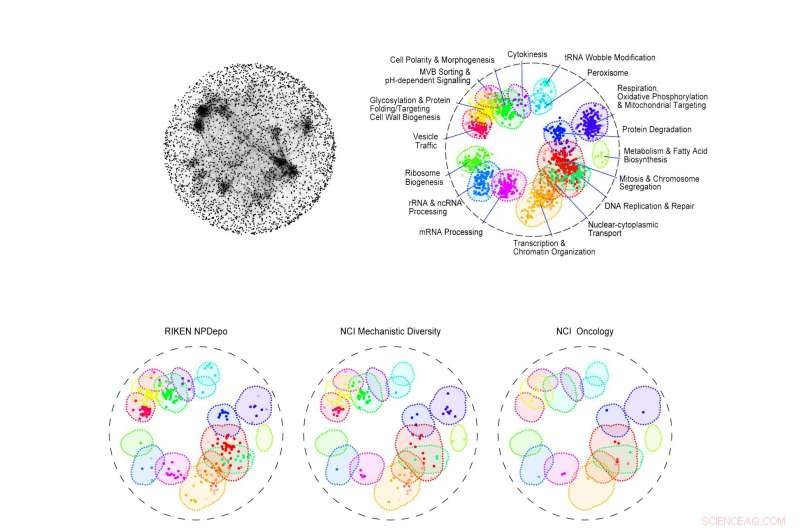
De bovenste kaart (links) laat zien hoe duizenden genen in gistcellen interageren om het cellulaire leven te orkestreren. Rechts worden 17 basale bioprocessen in verschillende kleuren getoond, waarbij stippen de belangrijkste betrokken genen vertegenwoordigen. De onderste kaarten zijn gemaakt door een chemische verbinding te koppelen aan een bioproces, medicijnfabrikanten vertellen waar ze moeten zoeken naar medicijnen die het meest waarschijnlijk op een specifieke ziekte zijn gericht. Bijvoorbeeld, de RIKEN-bibliotheek heeft meer potentiële antikankerverbindingen (onder "Mitosis and Chromosome Segregation" in rood en "DNA Replication &Repair" in mintgroen) dan andere bibliotheken. Krediet:Jeff Piotrowski
Gisten zijn momenteel het enige levende organisme waarin wetenschappers de basale cellulaire processen goed onder de knie hebben, zoals DNA-replicatie en -reparatie, energie productie, en transport van ladingmoleculen, waardoor ze een medicijn kunnen koppelen aan een bepaald bioproces.
"Door deze bibliotheken te annoteren, we kunnen zien welke bibliotheek zich op welk bioproces in de cel richt. Het geeft ons een voorsprong bij het koppelen van een verbinding aan een doel, wat misschien wel het meest uitdagende onderdeel is van het ontdekken van medicijnen, ', zegt Piotrowski.
De gegevens onthulden bijvoorbeeld, dat de RIKEN-bibliotheek verbindingen bevat die op veel verschillende manieren werken:van microbenbestrijdende chemicaliën die kunnen worden gebruikt om infecties te behandelen, op drugs die gericht zijn op cellulaire handel die betrokken is bij de ziekte van Alzheimer en Parkinson, tot degenen die interfereren met celreplicatie en kunnen worden gebruikt tegen kanker. In feite, de RIKEN-bibliotheek bleek veel nieuwe verbindingen met antikankerpotentieel te bevatten.
"Er is lang gedacht dat natuurlijke producten functioneel diverser zijn, dat ze meer kunnen dan puur gesynthetiseerde verbindingen en dat lijkt zeker waar te zijn uit onze gegevens, ' zegt Boonen.
En omdat natuurlijke verbindingen door evolutie zijn gevormd om in te werken op levende organismen, ze zijn betere kandidaten voor toekomstige medicijnen dan synthetische verbindingen die vaak niet eens in de cellen komen. Het is dan ook geen verrassing dat, van aspirine tot penicilline, aan de blockbuster kankermedicijn taxol, sommige van onze beste medicijnen komen uit de natuur.
De gegevens onthulden ook chemicaliën die meer dan één proces in de cel beïnvloeden. Deze verbindingen veroorzaken vaker bijwerkingen en kunnen het beste worden vermeden. "Met onze kaart we kunnen deze promiscue verbindingen eerder zien en ons concentreren op de goede, ', zegt Piotrowski.
Het onderzoek was mogelijk dankzij een eerder werk van Boone, Myers, en Donnelly Center-directeur Brenda Andrews, die in kaart bracht hoe duizenden genen met elkaar interageren om fundamentele processen in de cel aan te sturen. Het uitgangspunt hier was dat het verwijderen van één gen misschien niets uithaalt omdat er een back-upsysteem is, maar het verwijderen van twee genen leidt tot een diepgaand effect. Het is een beetje zoals het spelen van pick-up sticks waarbij het verwijderen van één stok per keer geen effect heeft, maar als je er twee bij elkaar verwijdert, valt de stapel naar beneden, of maakt het sterker.
In plaats van naar dubbele mutanten te kijken, de huidige studie heeft gemeten hoe enkele mutanten gecombineerd met medicijnen het welzijn van de cellen beïnvloeden. Hierdoor konden onderzoekers identificeren welk bioproces wordt beïnvloed door een bepaald medicijn, waardoor het werkingsmechanisme van het medicijn wordt geïdentificeerd. De schoonheid van het systeem dat door deze internationale, multidisciplinair onderzoeksteam was dat het alle genen in dezelfde test integreert om het gedrag van het hele genoom in reactie op een bepaald medicijn in één experiment te beoordelen.
 Kooldioxide als grondstof
Kooldioxide als grondstof Wat blokkeert enzymactiviteit door te binden aan de actieve site van een enzym?
Wat blokkeert enzymactiviteit door te binden aan de actieve site van een enzym?  Onderzoekers geven een nieuwe draai aan moleculaire zuurstof
Onderzoekers geven een nieuwe draai aan moleculaire zuurstof Wetenschappers observeren ultrasnelle geboorte van radicalen
Wetenschappers observeren ultrasnelle geboorte van radicalen Biostasis heeft tot doel de dood na traumatisch letsel te voorkomen door biochemische reacties in cellen te vertragen
Biostasis heeft tot doel de dood na traumatisch letsel te voorkomen door biochemische reacties in cellen te vertragen
 Prestaties van het regionale klimaatmodel RegCM4 boven China
Prestaties van het regionale klimaatmodel RegCM4 boven China Hoe de klimaatverandering in de landbouw te bestrijden en tegelijkertijd banen te beschermen?
Hoe de klimaatverandering in de landbouw te bestrijden en tegelijkertijd banen te beschermen? Laatste met ijs bedekte delen van de Noordelijke IJszee in de zomer kwetsbaar voor klimaatverandering
Laatste met ijs bedekte delen van de Noordelijke IJszee in de zomer kwetsbaar voor klimaatverandering Waarom consumenten hulp nodig hebben om over te stappen op duurzame voeding
Waarom consumenten hulp nodig hebben om over te stappen op duurzame voeding Smeltende gletsjers zorgen ervoor dat de zeespiegel steeds sneller stijgt
Smeltende gletsjers zorgen ervoor dat de zeespiegel steeds sneller stijgt
Hoofdlijnen
- Uit een grootschalig onderzoek blijkt dat veel geplande wegen in de tropen niet gebouwd mogen worden
- Wanneer treedt melkzuurfermentatie op?
- Wat gebeurt er met een dierlijke cel in een hypotone oplossing?
- High School Biology Topics
- Is het ethisch om stamcellen te gebruiken?
- Albatrospopulaties nemen af door visserij en veranderingen in het milieu
- De nadelen van biotechnologie
- Studie belicht de instandhoudingsbehoeften van recent ontdekte vissoorten in Southwest Virginia
- Twilight-truc:er is een nieuw type cel gevonden in het oog van een diepzeevis
- Onderzoek bevestigt dat verwarming de sterkte van een type hydrogel kan vergroten

- Hersenweefsel wekenlang in leven gehouden op een kunstmatig membraan
- Chemici waarschuwen voor onredelijke verspilling bij aanschaf van wetenschappelijke apparatuur

- Een effectieve manier om atrazin en zijn bijproducten in oppervlaktewater te elimineren

- Zelfherstellend membraan voor papieren documenten voor brandstofceltoepassingen

 Kwantummechanisch knijpen maakt atoomkrachtmicroscopie in kwantumtoestand mogelijk
Kwantummechanisch knijpen maakt atoomkrachtmicroscopie in kwantumtoestand mogelijk Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's
Wetenschappers lossen een duurzaamheidsprobleem op in brandstofcellen voor waterstofauto's Londenaren voelen zich genegeerd en niet vertegenwoordigd door advertenties
Londenaren voelen zich genegeerd en niet vertegenwoordigd door advertenties Hoe dieren stemmen om groepsbeslissingen te nemen
Hoe dieren stemmen om groepsbeslissingen te nemen NASA analyseert regenval rond tyfoon Chan-homs haveloos oog
NASA analyseert regenval rond tyfoon Chan-homs haveloos oog Wat doet acetonalcohol met een gramkleuring?
Wat doet acetonalcohol met een gramkleuring?  NASA's Juno-missie biedt infraroodtour langs de noordpool van Jupiter
NASA's Juno-missie biedt infraroodtour langs de noordpool van Jupiter Pfizer gaat niet-gepatenteerde geneesmiddelenactiviteiten combineren met Mylan
Pfizer gaat niet-gepatenteerde geneesmiddelenactiviteiten combineren met Mylan
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

