
Wetenschap
Wat is de chemische reactie tussen hcl en koh?
HCl (zoutzuur) is een sterk zuur, wat betekent dat het volledig dissocieert in water om H+ (waterstofionen) en Cl- (chloride-ionen) te vormen.
KOH (kaliumhydroxide) is een sterke base, wat betekent dat het volledig dissocieert in water en K+ (kaliumionen) en OH- (hydroxide-ionen) vormt.
Wanneer HCl en KOH worden gemengd, reageren de H+ ionen uit HCl met de OH-ionen uit KOH om watermoleculen (H2O) te vormen. Dit proces is in wezen een protonenoverdracht van het zuur naar de base.
De netto ionische vergelijking voor de reactie is:
H+ (uit HCl) + OH- (uit KOH) → H2O
Bovendien blijven de kaliumionen (K+) uit KOH en de chloride-ionen (Cl-) uit HCl in de oplossing als toeschouwerionen. Ze nemen niet rechtstreeks deel aan de neutralisatiereactie.
De algehele reactie kan als volgt worden samengevat:
HCl (aq) + KOH (aq) → H2O (l) + KCl (aq)
De producten van de reactie zijn water (H2O) en kaliumchloride (KCl), een zout dat in water oplost.
 Wat gebeurt er met watermoleculen als de temperatuur stijgt?
Wat gebeurt er met watermoleculen als de temperatuur stijgt?  Wat is het oxidatiegetal van stikstof in salpeterzuur?
Wat is het oxidatiegetal van stikstof in salpeterzuur?  Eiwit dat volledig vanuit het niets is ontworpen, functioneert in cellen als een echt enzym
Eiwit dat volledig vanuit het niets is ontworpen, functioneert in cellen als een echt enzym Hoge precisie chemische vingerafdruk maakt ondubbelzinnige identificatie mogelijk
Hoge precisie chemische vingerafdruk maakt ondubbelzinnige identificatie mogelijk Geleidbaarheid Vs. concentratie
Geleidbaarheid Vs. concentratie
 Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht
Koelende rol van fijnstof bij opwarming aarde sterker dan eerder gedacht Wijdverbreide droogtes treffen de waterbronnen in Zuid-Californië zes keer per eeuw
Wijdverbreide droogtes treffen de waterbronnen in Zuid-Californië zes keer per eeuw Waarom branden onze regenwouden?
Waarom branden onze regenwouden?  Puerto Rico hartverscheurend vijf weken na de storm
Puerto Rico hartverscheurend vijf weken na de storm Onderzoekers ontwikkelen nieuwe software voor het ontwerpen van duurzame steden
Onderzoekers ontwikkelen nieuwe software voor het ontwerpen van duurzame steden
Hoofdlijnen
- Welke klasse van enzymen hoort Lactase te zijn?
- Nieuwe intermoleculaire oppervlaktekracht onthult actomyosine-aandrijfmechanisme
- Verbeterde CRISPR-methode maakt stabiele invoeging van grote genen in het DNA van hogere planten mogelijk
- Nieuwe studie benadrukt de effecten van een wereldwijde strategie om de antibioticaconsumptie in de productie van voedseldieren te verminderen
- De 3D-structuur van het genoom bepaalt hoe genen tot expressie worden gebracht
- Wat is Tastile Stimulation?
- Door UC geleid team laat zien hoe de bacteriële gemeenschap evolueert
- Waarom zetten we de radio zachter als we verdwaald waren?
- De Stoned Ape-hypothese:hebben paddo's de menselijke evolutie beïnvloed?
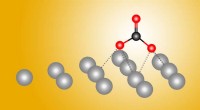
- Een wondermiddel voor de chemische omzetting van kooldioxide
- Alcohol omzetten in belangrijke ingrediënten voor nieuwe medicijnen

- Wetenschappers ontrafelen de werkingsprincipes van een veelbelovend materiaal voor het snel opladen van batterijen
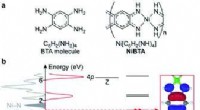
- Directe waarneming van de ad- en desorptie van gastatomen in een mesoporeuze gastheer

- Elektrochemische cel haalt lithium uit zeewater

 Stralingsrisico op historische kernproeflocatie in WA, 70 jaar later
Stralingsrisico op historische kernproeflocatie in WA, 70 jaar later Math Percentages leren lesgeven in de 6e klas
Math Percentages leren lesgeven in de 6e klas Europese planeetonderzoeksmissie gelanceerd vanuit Zuid-Amerika
Europese planeetonderzoeksmissie gelanceerd vanuit Zuid-Amerika Studies onderzoeken verschillende opvattingen, variëteiten van diversiteit
Studies onderzoeken verschillende opvattingen, variëteiten van diversiteit Gestresste cacaobomen kunnen smaakvollere chocolade produceren
Gestresste cacaobomen kunnen smaakvollere chocolade produceren Wat is een polyatomisch ion?
Wat is een polyatomisch ion?  Het marktvoordeel van een vrouwelijke merknaam
Het marktvoordeel van een vrouwelijke merknaam Uraniumverbinding bereikt record afwijkende Nernst-geleidbaarheid
Uraniumverbinding bereikt record afwijkende Nernst-geleidbaarheid
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

