
Wetenschap
Cryo-EM onthult interactie tussen belangrijke medicijndoelen
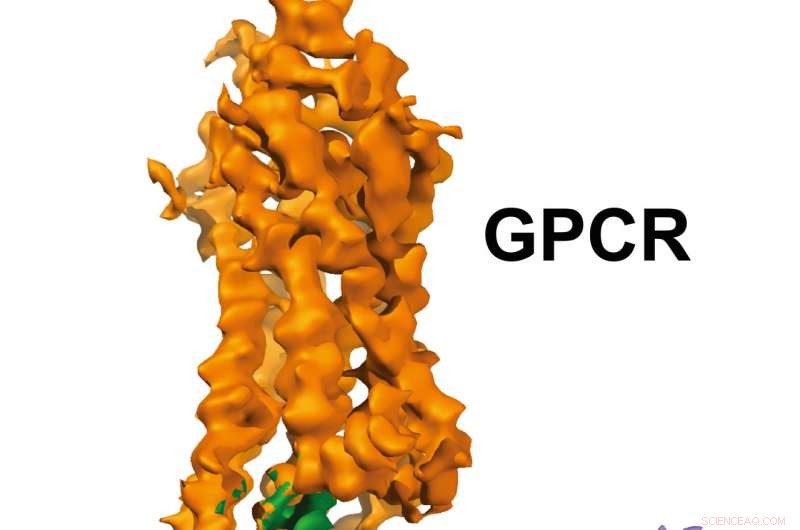
GPCR-Gi-structuur. Krediet:Xu-laboratorium, Van Andel Onderzoeksinstituut
Voor de eerste keer, wetenschappers hebben de interactie tussen twee kritieke componenten van het uitgebreide cellulaire communicatienetwerk van het lichaam gevisualiseerd, een ontdekking die zou kunnen leiden tot effectievere medicijnen met minder bijwerkingen voor aandoeningen variërend van migraine tot kanker.
De beelden met bijna atomaire resolutie, vandaag gepubliceerd in Natuur , een G-eiwit gekoppelde receptor (GPCR) vertonen, rhodopsine genaamd, gebonden aan een remmend G-eiwit, en biedt een blauwdruk om nauwkeuriger te ontwerpen, selectieve medicijnen, terwijl ook een al lang bestaand probleem in het veld wordt opgelost.
"Het visualiseren van dit complex lost een ontbrekend hoofdstuk in het GPCR-verhaal op door eindelijk te onthullen hoe deze twee moleculen in voortreffelijk detail op elkaar inwerken, " zei H. Eric Xu, doctoraat, een professor aan het Van Andel Research Institute (VARI) en een van de senior auteurs van de studie. "Alles in de biologie is gebaseerd op moleculaire interacties, dus hoe meer we weten over hoe de structuren van deze twee moleculen samenwerken, hoe beter we ons bevinden om verbeterde medicijnen te ontwerpen met minder ongewenste effecten."
De bevindingen van vandaag werden mogelijk gemaakt door het gebruik van een revolutionaire techniek genaamd cryo-elektronenmicroscopie (cryo-EM), waarmee wetenschappers moeilijk te visualiseren moleculen in verbazingwekkende helderheid kunnen zien.
"Het gebruik van cryo-EM-technologie om structurele informatie te verkrijgen over belangrijke farmaceutische doelen zoals GPCR's in verschillende staten, toont aan dat we nu in een positie zijn om deze methoden toe te passen voor toepassingen voor het ontdekken van geneesmiddelen, " zei Sriram Subramaniam, doctoraat, een onderzoeker bij het National Cancer Institute van de National Institutes of Health en een senior auteur van de studie.
Ingebed in het celmembraan, GPCR's fungeren als kanalen tussen een cel en zijn omgeving, interactie met G-eiwitten en andere signaalmoleculen, arrestines genaamd, om belangrijke berichten van en naar de cel over te brengen die een scala aan fysiologische functies reguleren, inclusief groei, immuunreacties en zintuiglijke waarneming.
Wanneer gekoppeld aan GPCR's, remmende G-eiwitten reguleren de productie van secundaire chemische boodschappers die effecten hebben door het hele lichaam, door interacties met serotoninereceptoren in de hersenen en darmen, die helpen bij het reguleren van stemming en eetlust, op interacties met dopaminereceptoren in de hersenen, die beloningsreacties en vrijwillige bewegingen beheersen, onder vele anderen.
Deze brede interacties met G-eiwitten en arrestines, in combinatie met hun toegankelijkheid aan de buitenkant van de cel, maken van GPCR's aantrekkelijke doelwitten voor therapeutische ontwikkeling. Momenteel, meer dan 30 procent van de medicijnen op de markt werken door interactie met GPCR's.
"De informatie die door onze bevindingen wordt onthuld, zal het ontwerp van een nieuwe generatie medicijnen helpen vergemakkelijken, " zei Yanyong Kang, doctoraat, een onderzoekswetenschapper in het Xu-laboratorium en co-eerste auteur van de studie. "Omdat dit het eerste GPCR-remmende G-eiwitcomplex is dat structureel is bepaald, wij geloven dat onze methoden zullen helpen leiden tot de karakterisering van andere belangrijke, maar moeilijk te visualiseren GPCR's."
De 3D-beelden die door het team zijn gegenereerd, onthullen een gespecialiseerde helix aan het einde van het remmende G-eiwit dat fungeert als een structurele handtekening, die GPCR's zoals rodopsine helpt onderscheid te maken tussen remmende G-eiwitten en een ander type G-eiwit dat bekend staat als een stimulerend G-eiwit.
De bevindingen van vandaag zijn de laatste in een reeks primeurs voor Xu en zijn team, waaronder een mijlpaal 2015 Natuur studie die voor het eerst de structuur van rodopsine en arrestine in complex samen beschreef. Dit werk, die werd geprezen als een grote doorbraak in het veld, verdiende Xu de Hans Neurath Award van The Protein Society en de Hans Neurath Foundation in 2016.
In een vervolgonderzoek gepubliceerd in Cel in 2017, Xu en zijn medewerkers hebben hun eerdere structuur van het rhodopsin-arrestin-complex verder verfijnd, en onthulde een reeks fosforylatiecodes die de assemblage van GPCR-arrestinecomplexen dicteren.
GPCR's zijn notoir moeilijk te visualiseren met behulp van traditionele röntgenkristallografiemethoden; daten, bij slechts 40 van de in totaal meer dan 800 GPCR's is de structuur bepaald, waaronder Xu's rhodopsine-arrestinecomplex.
Om de structuur van vandaag te bepalen, het team gebruikte VARI's krachtige Titan Krios cryo-elektronenmicroscoop, die in staat is moleculen 1/10 af te beelden, 000ste van de breedte van een mensenhaar en kan gemakkelijker moleculen zoals GPCR's visualiseren die in het celmembraan zijn ingebed. De Krios van het Instituut, dat deel uitmaakt van de David Van Andel Advanced Cryo-Electron Microscopy Suite, is een van de minder dan 120 van dergelijke microscopen in de wereld.
Subramaniam en zijn team hebben pionierswerk verricht in het gebruik van cryo-EM om enkele van de structuren met de hoogste resolutie die tot nu toe zijn gerapporteerd te bepalen met behulp van cryo-EM, waaronder verschillende klinisch relevante ligand-eiwitcomplexen.
 Een biomassa-naar-vloeistoffabriek voor de productie van duurzame synthetische brandstof
Een biomassa-naar-vloeistoffabriek voor de productie van duurzame synthetische brandstof Magneten gebruiken om chemische reacties te beheersen die gericht zijn op de afgifte van medicijnen in het lichaam
Magneten gebruiken om chemische reacties te beheersen die gericht zijn op de afgifte van medicijnen in het lichaam Je haar weet wat je eet en hoeveel je knipbeurt kost
Je haar weet wat je eet en hoeveel je knipbeurt kost Covalent Vs. Waterstofbindingen
Covalent Vs. Waterstofbindingen Biochemische netwerken van levens kunnen spontaan op aarde zijn gevormd
Biochemische netwerken van levens kunnen spontaan op aarde zijn gevormd
Hoofdlijnen
- Snelle papegaaien gefokt op roofdiervrije eilanden die met uitsterven worden bedreigd
- Klimaatverandering die de migratiepatronen van gierende kraanvogels beïnvloedt, studie vondsten
- Hoe permeabiliteit uit te leggen
- Amfibieën redden van een dodelijke schimmel betekent handelen zonder alle antwoorden te weten
- 10, 000 jaar oud DNA bewijst wanneer vissen meren koloniseerden
- Onderzoekers ontdekken nieuwe veeziekte en voorkomen dat deze zich verspreidt
- Twee soorten Cilia in een Paramecium
- Hoe orchideeën werken
- Wetenschappers lokaliseren jaloezie in de monogame geest
- Nieuw onderzoek biedt uitgebreide inzichten in de reactie van de hersenen op opioïden

- Akoestisch microfluïdisch platform scheidt circulerende tumorcellen voorzichtig en snel van bloedmonsters

- Plantaardige verbinding zou een sleutelrol kunnen spelen bij het bestrijden van de ziekte van Alzheimer

- Een goede kop koffie zetten is afhankelijk van scheikunde en natuurkunde

- Hoe moleculen om te zetten in Atoms

 Bomen die groeien in zout water
Bomen die groeien in zout water Vertellen rimpelingen op het oppervlak van de zon ons dat er een zonnevlam op komst is?
Vertellen rimpelingen op het oppervlak van de zon ons dat er een zonnevlam op komst is? Hoeveel katoen is er nodig om een shirt te maken?
Hoeveel katoen is er nodig om een shirt te maken?  Wetenschapper ontwikkelt wegwerpapparaten om allergieën te identificeren
Wetenschapper ontwikkelt wegwerpapparaten om allergieën te identificeren De geur van pure chocolade, gedemystificeerd
De geur van pure chocolade, gedemystificeerd LHCb kijkt naar de toekomst met SciFi-detector
LHCb kijkt naar de toekomst met SciFi-detector Brits plan om online porno te controleren wordt gezien als testcase
Brits plan om online porno te controleren wordt gezien als testcase Stijgende zeeën zorgen voor stress op de Hawaiiaanse kustplanten
Stijgende zeeën zorgen voor stress op de Hawaiiaanse kustplanten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

