
Wetenschap
Kooldioxide omzetten in koolmonoxide met behulp van water, elektriciteit

De reductie van CO 2 . Krediet:de heer Aditya Prajapati
Onderzoekers van de Universiteit van Illinois in Chicago en het Joint Center for Artificial Photosynthesis hebben vastgesteld hoe elektrokatalysatoren koolstofdioxide kunnen omzetten in koolmonoxide met behulp van water en elektriciteit. De ontdekking kan leiden tot de ontwikkeling van efficiënte elektrokatalysatoren voor grootschalige productie van synthesegas - een mengsel van koolmonoxide en waterstof.
"De elektrochemische reductie van kooldioxide tot brandstoffen is een onderwerp van groot belang omdat het een middel biedt om elektriciteit uit energiebronnen zoals wind- en zonnestraling op te slaan in de vorm van chemische bindingen, " zei Meenesh Singh, assistent-professor chemische technologie en hoofdauteur van de studie gepubliceerd in het tijdschrift Proceedings van de National Academy of Sciences .
Tijdens zijn postdoctoraal onderzoek aan de Universiteit van Californië, Berkeley, Singh bestudeerde kunstmatige fotosynthese en maakte deel uit van een team dat kunstmatige bladeren ontwikkelde die, bij blootstelling aan direct zonlicht, in staat waren om koolstofdioxide om te zetten in brandstoffen.
In zijn laatste onderzoek Singh ontwikkelde een ultramodern multischaalmodel dat een kwantumchemische analyse van het reactiepad verenigt; een microkinetisch model van de reactiedynamiek; en een continuümmodel voor transport van soorten in de elektrolyt om precies te leren hoe koolstofdioxide elektrochemisch kan worden gereduceerd door een katalysator, in dit geval zilver, en verwerkt tot koolmonoxide.
Hoewel de meest plausibele reactieroute meestal wordt geïdentificeerd aan de hand van kwantumchemische berekening van de laagste vrije-energieroute, deze benadering kan misleidend zijn wanneer dekkingen van geadsorbeerde soorten aanzienlijk verschillen, zei Singh. Het is essentieel, daarom, om de effecten van elektronische toestanden van een katalysator op atomair niveau te integreren met de dynamiek van soorten in de elektrolyt op continuümniveau voor nauwkeurige voorspelling van elektrokatalytische reactiepaden.
"Dit multischaalmodel is een van de grootste prestaties in de elektrochemie, " hij zei.
Om te begrijpen hoe elektrokatalysatoren in brandstofcellen of elektrochemische cellen werken, wetenschappers moeten eerst de elektronische en kwantumniveaus onderzoeken, wat zeer uitdagend kan zijn in de aanwezigheid van een elektrisch veld, zei Jason Goodpaster, assistent-professor scheikunde aan de Universiteit van Minnesota en een van de co-auteurs. Het kostte Singh en Goodpaster meer dan een jaar om de modellen individueel te produceren en te benchmarken en ze te integreren in een multischaalraamwerk voor volledige simulatie van de elektrochemische reactie.
Dit is de eerste keer, Singh zei, die wetenschappers kwantitatief hebben voorspeld vanuit de eerste principes, de stroomdichtheid van koolmonoxide en waterstof als functie van de aangelegde potentiaal en de druk van kooldioxide.
"Als je eenmaal herkent hoe deze reacties plaatsvinden op elektrokatalysatoren, u kunt de structuur van de katalysator en de bedrijfsomstandigheden regelen om koolmonoxide efficiënt te produceren, "Zei Singh. Omdat het productgassen zijn - koolmonoxide en waterstof zijn onoplosbaar in waterige elektrolyten - kunnen ze gemakkelijk worden gescheiden als synthesegas en worden omgezet in brandstoffen zoals methanol, dimethylether, of een mengsel van koolwaterstoffen.
Elektrokatalysatoren zoals goud, zilver, zink, Van palladium en gallium is bekend dat ze mengsels van koolstofdioxide en waterstof opleveren in verschillende verhoudingen, afhankelijk van de aangelegde spanning, zei Singh. Goud en zilver vertonen de hoogste activiteit op het gebied van koolstofdioxidereductie, en aangezien zilver overvloediger en goedkoper is dan goud, "zilver is de meest veelbelovende elektrokatalysator voor grootschalige productie van koolmonoxide, " hij zei.
 UITLEG:Is New Orleans beschermd tegen een orkaan?
UITLEG:Is New Orleans beschermd tegen een orkaan? Welke richting moet een Bluebird House onder ogen zien?
Welke richting moet een Bluebird House onder ogen zien?  VN:korte winst in luchtkwaliteit in 2020 door COVID-lockdowns
VN:korte winst in luchtkwaliteit in 2020 door COVID-lockdowns Menselijke activiteiten bleken bij te dragen aan een toename van extreme regenval in Noord-Amerika
Menselijke activiteiten bleken bij te dragen aan een toename van extreme regenval in Noord-Amerika Afbeelding:Mount Mayon, Filippijnen
Afbeelding:Mount Mayon, Filippijnen
Hoofdlijnen
- Wanneer wordt een mutatie in een DNA-molecuul doorgegeven aan nakomelingen?
- Embryonale ontwikkeling van een kikker
- Een epigenetische sleutel om gedragsverandering te ontgrendelen
- CRISPR-octrooioorlogen benadrukken het probleem van het verlenen van brede intellectuele eigendomsrechten voor technologie die publieke voordelen biedt
- Zelfs als je nog niet weet dat je ziek bent, je gezicht zal je verraden
- Wat is het verschil tussen een Centriole en een Centrosome?
- Zijn mannen of vrouwen betere navigators?
- Wat veroorzaakt psychische aandoeningen?
- Een Chromosome-diagram interpreteren
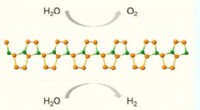
- Tijd voor een nieuwe concurrent in energieconversie en opslag
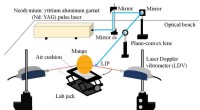
- Forensisch chemici lasertechniek onderscheidt menselijk en dierlijk bloed

- De tijd is rijp! Een innovatieve contactloze methode voor het tijdig oogsten van zachtfruit
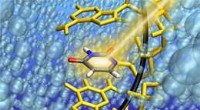
- RNA-streng maakt het vangen van uracil in de kritieke toestand mogelijk
- Nieuwe RNA-modificerende tool corrigeert genetische ziekten, inclusief aanjager van triple-negatieve borstkanker

 De noodzaak om minder te werken is een kwestie van leven en dood
De noodzaak om minder te werken is een kwestie van leven en dood Onderzoekers ontwikkelen de eerste breedbandbeeldsensorarray op basis van grafeen-CMOS-integratie
Onderzoekers ontwikkelen de eerste breedbandbeeldsensorarray op basis van grafeen-CMOS-integratie Wetenschappers kweken supervoedzame gewassen om honger in de wereld te helpen oplossen
Wetenschappers kweken supervoedzame gewassen om honger in de wereld te helpen oplossen Docking, rendez-vous en de derde wet van Newton - de uitdaging om satellieten in de ruimte te onderhouden
Docking, rendez-vous en de derde wet van Newton - de uitdaging om satellieten in de ruimte te onderhouden Klimaatwetenschappers zijn misschien niet de beste communicators van klimaatbedreigingen
Klimaatwetenschappers zijn misschien niet de beste communicators van klimaatbedreigingen Neutrino-faciliteit kan het begrip van het universum veranderen
Neutrino-faciliteit kan het begrip van het universum veranderen BLM beweging betrokken jongeren, met positieve en negatieve effecten
BLM beweging betrokken jongeren, met positieve en negatieve effecten Venus oude gelaagde, gevouwen rotsen wijzen op vulkanische oorsprong
Venus oude gelaagde, gevouwen rotsen wijzen op vulkanische oorsprong
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Danish | Norway | Swedish |

-
Wetenschap © https://nl.scienceaq.com

