
Wetenschap
Nieuwe onderzoeksinzichten in hoe een groep nieuwe op organellen gebaseerde aandoeningen cellen beïnvloedt
Inleiding:
Organellen, de gespecialiseerde compartimenten binnen cellen, spelen een cruciale rol bij het handhaven van de cellulaire homeostase en functie. Verstoringen van de structuur of functie van organellen kunnen leiden tot een reeks ziekten bij de mens, die op organellen gebaseerde aandoeningen worden genoemd. Onlangs is een groep nieuwe op organellen gebaseerde aandoeningen geïdentificeerd, die licht werpen op de ingewikkelde mechanismen die ten grondslag liggen aan cellulaire disfunctie en ziektepathogenese. Dit artikel heeft tot doel nieuwe onderzoeksinzichten te verschaffen in de manier waarop deze aandoeningen cellen op moleculair niveau beïnvloeden.
Mitochondriale aandoeningen:energieverstoring en meer:
Mitochondria, de cellulaire krachtcentrales, spelen een centrale rol in de energieproductie. Defecten in de mitochondriale functie kunnen leiden tot een reeks aandoeningen, waaronder mitochondriale encefalopathieën, cardiomyopathieën en neurodegeneratieve ziekten. Recente studies hebben de moleculaire mechanismen onthuld waarmee mitochondriale dysfunctie cellulaire processen schaadt. Mutaties in mitochondriaal DNA of defecten in oxidatieve fosforylering verstoren bijvoorbeeld de energieproductie, wat leidt tot cellulaire stress, oxidatieve schade en verminderde apoptose. Bovendien kan mitochondriale disfunctie ontstekingsreacties veroorzaken en de calciumhomeostase veranderen, wat verder bijdraagt aan de ziekteprogressie.
Lysosomale opslagstoornissen:accumulatie en disfunctie:
Lysosomen, het systeem voor de verwijdering van cellulair afval, spelen een cruciale rol bij het afbreken en recyclen van cellulaire afvalproducten. Defecten in de lysosomale functie leiden tot lysosomale stapelingsstoornissen, gekenmerkt door de ophoping van onverteerde materialen in lysosomen. Onderzoek heeft verschillende moleculaire mechanismen geïdentificeerd die ten grondslag liggen aan deze aandoeningen. Mutaties in lysosomale enzymen of defecten in lysosomale membraaneiwitten verstoren bijvoorbeeld het afbraakproces, wat leidt tot de accumulatie van specifieke substraten. Deze ophoping verstoort de cellulaire functie en veroorzaakt cellulaire schade en weefseldisfunctie.
Endoplasmatisch reticulumstress en eiwitmisvouwingsstoornissen:
Het endoplasmatisch reticulum (ER) is verantwoordelijk voor de eiwitsynthese, vouwing en transport. ER-stress, veroorzaakt door verstoringen in de eiwitvouwing of ER-functie, kan leiden tot een reeks aandoeningen, waaronder neurodegeneratieve ziekten en metabole syndromen. Recente onderzoeken hebben de moleculaire gebeurtenissen blootgelegd die worden veroorzaakt door ER-stress. Accumulatie van ongevouwen of verkeerd gevouwen eiwitten activeert de ongevouwen eiwitrespons (UPR), een cellulaire route gericht op het herstellen van ER-homeostase. Langdurige of ernstige ER-stress kan echter apoptotische routes veroorzaken, wat leidt tot cellulaire disfunctie en ziekteprogressie.
Nucleaire envelopaandoeningen:verstoring van de nucleair-cytoplasmatische communicatie:
De nucleaire envelop, bestaande uit het kernmembraan en nucleaire poriecomplexen, reguleert het transport van moleculen tussen de kern en het cytoplasma. Defecten in de nucleaire envelop kunnen leiden tot een groep aandoeningen die bekend staat als nucleaire envelopaandoeningen, waaronder laminopathieën en Emery-Dreifuss-spierdystrofie. Onderzoek heeft mutaties in nucleaire envelopeiwitten geïdentificeerd die de nucleaire architectuur verstoren, de genexpressie aantasten en de chromatine-organisatie veranderen. Deze moleculaire veranderingen beïnvloeden verschillende cellulaire processen en dragen bij aan de pathogenese van ziekten.
Conclusie:
De studie van nieuwe op organellen gebaseerde aandoeningen heeft opmerkelijke inzichten opgeleverd in de moleculaire mechanismen die ten grondslag liggen aan cellulaire disfunctie en ziektepathogenese. Onderzoek op dit gebied heeft specifieke genetische mutaties, moleculaire routes en cellulaire processen geïdentificeerd die bij deze aandoeningen worden beïnvloed. Het begrijpen van deze moleculaire mechanismen is cruciaal voor het ontwikkelen van gerichte therapieën en interventies gericht op het herstellen van de organelfunctie en het verlichten van ziektesymptomen. Voortgezet onderzoek op dit gebied is veelbelovend voor het verbeteren van de levens van mensen die door deze slopende aandoeningen worden getroffen.
 MagLab-wetenschappers ontdekken thermo-elektrische eigenschappen in veelbelovende materiaalklasse
MagLab-wetenschappers ontdekken thermo-elektrische eigenschappen in veelbelovende materiaalklasse Nieuwe gelcoatings kunnen leiden tot betere katheters en condooms
Nieuwe gelcoatings kunnen leiden tot betere katheters en condooms Chaos voorspellen met spuitbussen en AI
Chaos voorspellen met spuitbussen en AI Thermo-elektrische permanente magneet opent nieuwe mogelijkheden in technologieën voor thermisch beheer
Thermo-elektrische permanente magneet opent nieuwe mogelijkheden in technologieën voor thermisch beheer  Onderzoekers rapporteren nieuwe toestand van materie beschreven als vloeibaar glas
Onderzoekers rapporteren nieuwe toestand van materie beschreven als vloeibaar glas
 Microplasticconcentraties in Antarctisch zeewater hoger dan eerder geschat
Microplasticconcentraties in Antarctisch zeewater hoger dan eerder geschat  EU-landbouw niet levensvatbaar voor de toekomst
EU-landbouw niet levensvatbaar voor de toekomst De heldere manieren waarop bossen hun omgeving beïnvloeden
De heldere manieren waarop bossen hun omgeving beïnvloeden Hoge concentraties pesticiden blijven het Great Barrier Reef binnendringen
Hoge concentraties pesticiden blijven het Great Barrier Reef binnendringen Opgesloten Delhi geniet van frisse lucht en blauwe lucht
Opgesloten Delhi geniet van frisse lucht en blauwe lucht
Hoofdlijnen
- Wetenschappers pleiten voor een wereldwijde kiembank
- Vangstvissen kan temperatuurpieken veroorzaken bij haaien
- Zenuwonderzoek laat zien hoe cellen zich aanpassen om schade te helpen herstellen
- Niet genoeg:bescherming van algenetende vissen onvoldoende om bedreigde koraalriffen te redden, concludeert studie
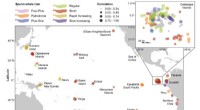
- Boomwoning, kokosnootkrakende gigantische rat ontdekt op de Salomonseilanden
- Genetisch onderzoek toont aan dat vissen in de vroege zomer een evolutionaire impact kan hebben, wat resulteert in kleinere zalm
- Great Basin zaadstudie-experiment richt zich op herstel van weidegronden
- Polygene eigenschappen: definitie, voorbeeld en feiten
- De hoogste partiële zuurstofdruk in de bloedsomloop
- Zelfs als je nog niet weet dat je ziek bent, je gezicht zal je verraden

- Neanderthalers waren eigenlijk prehistorische Picasso's
- Walvisclans gebruiken vocalisaties om hun cultuur te markeren
- Zeegras is wereldwijd een belangrijk visgebied

- Nieuwe filmtechniek onthult bacteriële signalering in scherpere resolutie

 Veranderingen in de grootte van de rat onthullen de habitat van de Hobbit-hominine
Veranderingen in de grootte van de rat onthullen de habitat van de Hobbit-hominine Hubble biedt interstellaire wegenkaart voor Voyagers galactische trektocht
Hubble biedt interstellaire wegenkaart voor Voyagers galactische trektocht Meteorieten geven aanwijzingen voor de oorsprong van het zonnestelsel
Meteorieten geven aanwijzingen voor de oorsprong van het zonnestelsel Waarom gebruiken mensen nog steeds faxmachines?
Waarom gebruiken mensen nog steeds faxmachines? Nieuw experiment geeft een beter begrip van fundamentele foto-geïnduceerde röntgenprocessen
Nieuw experiment geeft een beter begrip van fundamentele foto-geïnduceerde röntgenprocessen Hotspots in een actieve galactische kern
Hotspots in een actieve galactische kern Nieuwe uitbarstingen ontdekt in een eigenaardige, actieve dwergnova MN Draconis
Nieuwe uitbarstingen ontdekt in een eigenaardige, actieve dwergnova MN Draconis Water in asteroïdestof biedt aanwijzingen voor het leven op aarde
Water in asteroïdestof biedt aanwijzingen voor het leven op aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

