
Wetenschap
Studie onderzoekt langere levensduur door gebrekkige RNA-verwerking
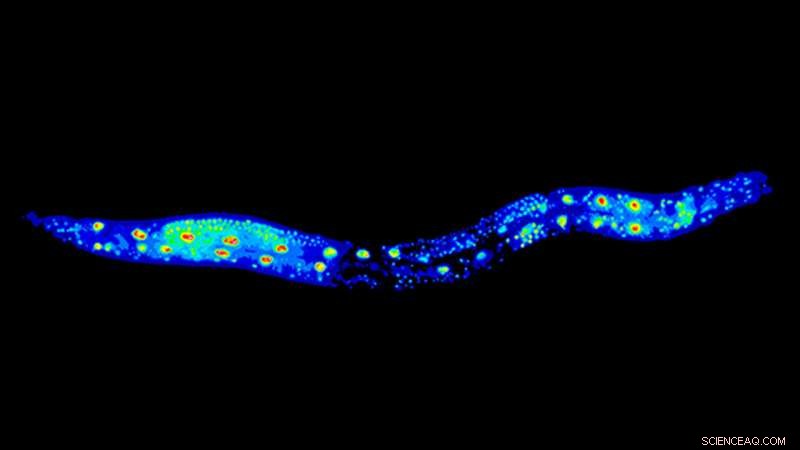
De rondworm Caenorhabditis elegans is een belangrijk modelorganisme in verouderingsonderzoek. De worm in de afbeelding is gelabeld met GFP::RNP-6. Credit:Max Planck Instituut voor Biologie van veroudering
De controle van het RNA-metabolisme is cruciaal voor de regulering van de levensduur van dieren, hebben onderzoekers van het Max Planck Instituut voor Biologie van veroudering in Keulen nu ontdekt. Ze ontdekten dat wormen langer leven wanneer bepaalde RNA's anders worden verwerkt tijdens de RNA-rijping. Dit kan voor organismen een extra manier zijn om het verouderingsproces te beheersen.
RNA is een belangrijke zender van informatie in onze cellen en dient als blauwdruk voor de aanmaak van eiwitten. Wanneer vers gevormd RNA wordt verwerkt, worden zogenaamde introns uitgesneden om het rijpe mRNA te produceren dat codeert voor eiwit. Dit snijden wordt "splicen" genoemd en wordt bestuurd door een complex dat het "spliceosoom" wordt genoemd.
Langlevende wormen
"We hebben een gen gevonden in wormen, PUF60 genaamd, dat betrokken is bij RNA-splitsing en de levensduur reguleert", zegt Max Planck-wetenschapper Dr. Wenming Huang die de ontdekking deed. Mutaties in dit gen veroorzaakten onnauwkeurige splicing en de retentie van introns binnen specifieke RNA's. Dientengevolge werden uit dit RNA kleinere hoeveelheden van de overeenkomstige eiwitten gevormd. Verrassend genoeg leefden wormen met deze mutatie in het PUF60-gen aanzienlijk langer dan normale wormen.
Vooral beïnvloed door deze defecte productie waren enkele eiwitten die een rol spelen in de mTOR-signaleringsroute. Deze signaalroute is een belangrijke sensor voor de beschikbaarheid van voedsel en dient als controlecentrum voor het celmetabolisme. Het is lang de focus geweest van verouderingsonderzoek als doelwit van potentiële anti-verouderingsgeneesmiddelen. De onderzoekers konden ook in menselijke celculturen aantonen dat verminderde niveaus van PUF60-activiteit leidden tot een lagere activiteit van de mTOR-signaleringsroute.
PUF60-mutatie bij mensen
"We denken dat we door het lot van introns in RNA's te veranderen, een nieuw mechanisme hebben ontdekt dat mTOR-signalering en levensduur reguleert", zegt Max Planck-directeur Adam Antebi, die de studie leidde die werd gepubliceerd in Nature Aging .
"Interessant is dat er ook menselijke patiënten zijn met vergelijkbare mutaties in het PUF60-gen. Deze patiënten hebben groeistoornissen en neurologische ontwikkelingsstoornissen. Misschien kunnen deze patiënten in de toekomst worden geholpen door medicijnen toe te dienen die de mTOR-activiteit beheersen. Maar dit heeft natuurlijk meer nodig Onderzoek." + Verder verkennen
Een evenwichtsoefening tussen immuniteit en levensduur
 Veranderingen in het zwaartekrachtveld van de aarde:unieke gegevensreeksen worden vervolgd
Veranderingen in het zwaartekrachtveld van de aarde:unieke gegevensreeksen worden vervolgd Planten en dieren gevonden in tropische gebieden
Planten en dieren gevonden in tropische gebieden Verspil niet, wil niet - nieuwe benaderingen van verlaten voedsel
Verspil niet, wil niet - nieuwe benaderingen van verlaten voedsel Sri Lanka verbiedt plastic na afvalcrisis
Sri Lanka verbiedt plastic na afvalcrisis In Yakutia, Rusland graaft naar diamanten in permafrost
In Yakutia, Rusland graaft naar diamanten in permafrost
Hoofdlijnen
- Dit is het seizoen om waakzaam te zijn:het risico op chocoladevergiftiging bij honden piekt met Kerstmis
- Is er een psychologische reden waarom mensen gemeen zijn op internet?
- Wat is het voordeel van het feit dat het DNA goed is ingepakt in de chromosomen?
- Manieren om te voorkomen dat studenten mobiele telefoons gebruiken in Class
- Deskundigen zijn het erover eens:het welzijn van melkvee is slechter dan vleesvee
- Tribunelichten van 9/11 kunnen gevaarlijk zijn voor vogels studie zegt:
- Ondergewaardeerde microben krijgen nu de eer voor het behouden van twee banen in de bodem
- Chimpansees die het huis verlaten stellen het ouderschap uit
- Actief transport: een overzicht van primair en secundair
- Onderzoek toont aan dat honden slimmer zijn dan katten

- Is er een psychologische reden waarom mensen gemeen zijn op internet?

- Waarom zijn mensen altruïstisch?

- Gebruik van micro-organismen om grote ziekten te bestrijden die de rundvleesindustrie treffen

- De bodemtemperatuur kan de verspreiding van plagen in gewassen voorspellen

 Belang van reptielen in het ecosysteem
Belang van reptielen in het ecosysteem Popcornvormige gouddeeltjes komen samen op Salmonella
Popcornvormige gouddeeltjes komen samen op Salmonella Schadelijke microben gevonden op wanden van rioolbuizen
Schadelijke microben gevonden op wanden van rioolbuizen Nanomaterialen in onze omgeving
Nanomaterialen in onze omgeving Nieuw boek volgt expedities om Einsteins relativiteitstheorie te testen
Nieuw boek volgt expedities om Einsteins relativiteitstheorie te testen Waarom kunnen boten van staal op het water drijven als een stalen staaf zinkt?
Waarom kunnen boten van staal op het water drijven als een stalen staaf zinkt?  Hoge harmonischen verlichten de beweging van atomen en elektronen
Hoge harmonischen verlichten de beweging van atomen en elektronen De wetenschap is duidelijk:we moeten vandaag beginnen met het creëren van onze koolstofarme toekomst
De wetenschap is duidelijk:we moeten vandaag beginnen met het creëren van onze koolstofarme toekomst
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

