
Wetenschap
Vloeistofinterface-ondersteunde SERS zouden de ziekte van Alzheimer eerder kunnen detecteren
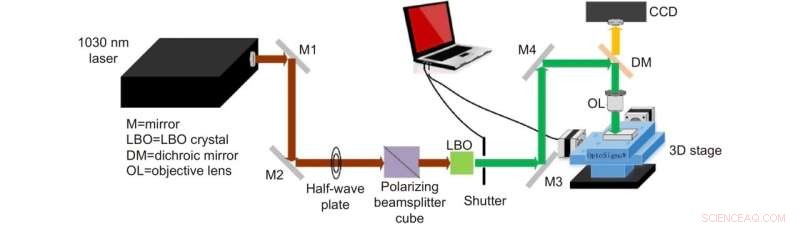
Figuur 1. Schematische voorstelling van laserfabricagesysteem voor microfluïdische SERS-chips. Krediet:Compuscript Ltd
Een nieuwe publicatie van Opto-Electronic Advances bespreekt labelvrije sporendetectie van biomoleculen door vloeistof-interface-ondersteunde Raman-verstrooiing aan het oppervlak met behulp van een microfluïdische chip.
Surface-enhanced Raman scattering (SERS) heeft de aandacht getrokken in de biotechnologie. Het is te wijten aan zijn hoge gevoeligheid voor gelokaliseerde oppervlakteplasmonresonantie van nanogestructureerde metalen. Sporendetectie van biomoleculen met een groot molecuulgewicht blijft een uitdaging omdat het behandelen van SERS-substraat met behulp van koppelings- of verknopingsmiddelen vereist is. De onderzoekers pasten SERS met vloeistofinterface toe om labelvrije sporendetectie van biomoleculen te realiseren. De resultaten suggereren dat het veelbelovend is voor de diagnose van een virusinfectie en de ziekte van Alzheimer in een vroeg stadium.
Surface-enhanced Raman-verstrooiing (SERS), gebaseerd op een optisch nabij-veldeffect dat wordt geïnduceerd door het oppervlakteplasmon van nanodeeltjes van edelmetaal of nanostructuren die worden geëxciteerd door laserstraling, versterkt de Raman-signalen tot 10 14 keer vergeleken met gewone Raman. Vanwege de verhoogde intensiteit blijft de SERS-techniek steeds meer belangstelling wekken voor detectie en analyse van biomaterialen op sporenniveau. Er is meer belangstelling voor gebieden zoals het afbeelden van organellen in een enkele cel, het volgen van kankercellen en identificatie van biomarkers.
De SERS-techniek kan in het biomedische veld worden gebruikt voor ziektediagnose in een vroeg stadium en ook bij tumortherapie. Hoewel de verbeteringsfactor van SERS doorgaans varieert van 10 6 – 10 8 vanwege het gebruik van nieuwe SERS-substraten en -methoden is detectie van één molecuul door labelvrije SERS onpraktisch vanwege SERS-knipperen, waarbij de oorsprong van dit fenomeen te wijten is aan het ontsnappen van analytmoleculen uit hotspots. Bovendien zijn biomoleculen, waaronder desoxyribonucleïnezuur (DNA) en eiwitten, moeilijk direct te detecteren door SERS. Aanvullende behandelingen met een SERS-substraat zijn nodig om de biomoleculen te binden.
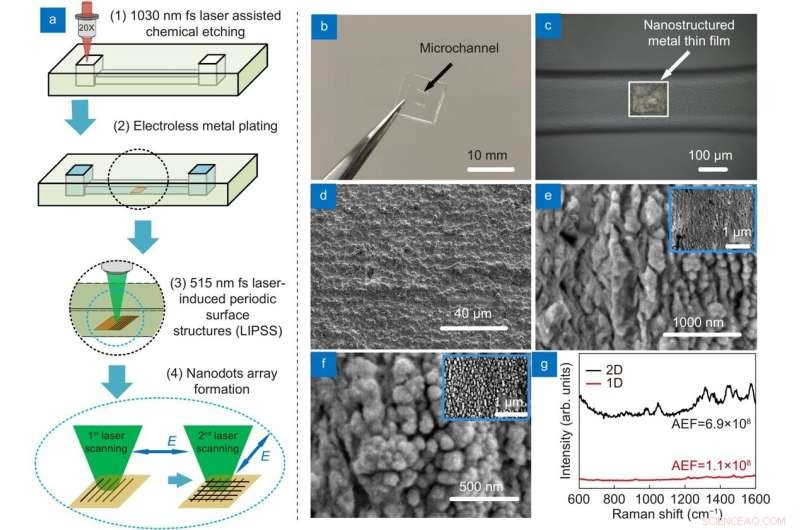
Figuur 2. (a) Schematische voorstelling van de fabricage (b) Foto van microfluïdische SERS-chip (c) Optische microscoopafbeelding die het SERS-substraat toont. SEM-afbeeldingen van (d) originele metaalfilm, (e) rimpelingen gegenereerd door 1e laserscanning en (f) nanodots gegenereerd door 2e laserscanning (insert:lage vergroting van SEM-afbeelding). (g) Raman-spectra van 10-9 M Rhodamine 6G (R6G) op 2-D (zwart) en 1-D (rood) nanogestructureerde SERS-substraten. Krediet:Compuscript Ltd
Het onderzoeksteam stelde LI-SERS voor, waarmee een SERS-verbeteringsfactor van meer dan 10 14 wordt bereikt , veel hoger dan de reguliere SERS-methode. De microfluïdische SERS-chip bevatte een Ag-Cu SERS-substraat geïntegreerd in een ingebed glazen microkanaal. Hybride femtoseconde (fs) laserverwerking creëerde het microkanaal van gras.
De hybride fs-laserverwerking maakt het mogelijk om meer gecompliceerde 3D-structuren te creëren met verbeterde functionaliteiten voor biochips, sensoren en micro-elektronische apparaten. Toen de interface tussen de analytoplossing en lucht op het SERS-substraat in het microfluïdische kanaal werd bestraald door de Raman-excitatielaser, werd de LI-SERS-intensiteit verhoogd met zes ordes van grootte in vergelijking met reguliere SERS. Het mechanisme van LI-SERS werd toegeschreven aan het synergetische effect van de Marangoni-stroom veroorzaakt door laserbestraling en optische trapping. Die laserbestraling zou de analytmoleculen naar de hotspots leiden waar de verzamelde moleculen door optische kracht worden gevangen. Bijgevolg werden de analytmoleculen geïmmobiliseerd op het SERS-substraat met het bereiken van sterke Raman-verstrooiing.
Deze studie toonde aan dat de LI-SERS-methode toepasbaar is voor meer praktisch gebruik. Het is met name nuttig voor sporendetectie van labelvrije biomoleculen met grote molecuulmassa's, waaronder DNA-basen, DNA-sequenties en β-Amyloïde (Aβ). Dankzij de ultrahoge gevoeligheid en zelfimmobilisatie van LI-SERS werd discriminatie van DNA-basen en DNA-sequenties met een detectielimiet van 1 fM verkregen zonder dat aanvullende behandelingen met koppelings- of verknopingsmiddelen nodig waren. Bovendien kan de LI-SERS-techniek labelvrij Aβ, een biomarker van de ziekte van Alzheimer, detecteren bij niveaus onder 1 pM, en met een lineaire correlatie tussen het Raman-signaal en de Aβ-concentratie in het bereik van 1 nM–1 pM. De labelvrije bio-sensing-capaciteit van LI-SERS biedt een groot potentieel voor de vroege diagnose van ziekten in klinieken.
Concluderend hebben de onderzoekers een overzicht gegeven van de reikwijdte van de LI-SERS-methode voor sporendetectie van biomoleculen in microfluïdische SERS-chips, met bijzondere verwijzing naar ultraspoordetectie van DNA-basen en Aβ. Men liet zich een vloeistofgrensvlak vormen in het microkanaal. De door LI-SERS geïnduceerde Marangoni-flow- en optische trapping-effecten toonden een detectielimiet van 1 fM aan voor labelvrije DNA-basen. Opmerkelijke kenmerken van de LI-SERS-methode, waaronder de ultrahoge gevoeligheid en veelzijdigheid die gepaard gaat met het verzamelen en zelf-immobiliserende analytmoleculen op de hotspots, zullen gunstig zijn voor ziektediagnoses in een vroeg stadium, zoals virale infecties en de ziekte van Alzheimer. + Verder verkennen
Nieuwe SERS-methode ontwikkeld om doelmoleculen te vangen
 Hoe een Green New Deal ontwikkelingslanden zou kunnen exploiteren
Hoe een Green New Deal ontwikkelingslanden zou kunnen exploiteren Plastic afval valt uiteen in nanodeeltjes, studie vondsten
Plastic afval valt uiteen in nanodeeltjes, studie vondsten Huidige metingen van klimaatverandering maskeren afwegingen die nodig zijn voor beleidsdebatten
Huidige metingen van klimaatverandering maskeren afwegingen die nodig zijn voor beleidsdebatten NASA-satellieten detecteren jaren voor uitbarstingen tekenen van vulkanische onrust
NASA-satellieten detecteren jaren voor uitbarstingen tekenen van vulkanische onrust NASA vindt sterk regenpotentieel in tropische storm Gordon
NASA vindt sterk regenpotentieel in tropische storm Gordon
Hoofdlijnen
- Genetische redding bevordert het herstel van de met uitsterven bedreigde Australische dwergbuidelmuizen
- Bacteriën levenscyclus
- In de winkel gekochte kroontjeskruidplanten kunnen monarchrupsen blootstellen aan schadelijke pesticiden
- Huilende olifanten en giechelende ratten - dieren hebben gevoelens, te
- Nauwkeuriger lezen van RNA-modificaties in een zakformaatapparaat
- Waarom is DNA de blauwdruk van het leven?
- Hoe Brain Mapping werkt
- Onderzoek naar de levensstijl van microben
- Kan inzicht in het gedrag van eigenaren de gezondheid en het welzijn van paarden verbeteren?
- Wetenschappers breken de link tussen een spin van kwantummaterialen en orbitale toestanden
- Nieuwe ontwerpprincipes voor op spin gebaseerde kwantummaterialen

- Betere beveiligingen voor gevoelige informatie

- Een kwantumkristal visualiseren:beeldvorming van het elektronische Wigner-kristal in 1-D
- De kosten van supergeleidende magneten laag houden met behulp van ultrageluid

 Welke elementen zijn Covalent?
Welke elementen zijn Covalent?  Een derde van het methaan in Californië herleid tot enkele superstralers
Een derde van het methaan in Californië herleid tot enkele superstralers Boeing verwacht MAX-productie voor medio 2020 te hervatten
Boeing verwacht MAX-productie voor medio 2020 te hervatten Sniff-cam om ziekte op te sporen
Sniff-cam om ziekte op te sporen Hoe een TI-34-calculator te bedienen
Hoe een TI-34-calculator te bedienen  Elektronenbiljart in circuits op nanoschaal:foto-elektronen karakteriseren met kwantumpuntcontacten
Elektronenbiljart in circuits op nanoschaal:foto-elektronen karakteriseren met kwantumpuntcontacten Voor Ghana recyclers van e-waste, een veiligere optie te midden van giftige dampen
Voor Ghana recyclers van e-waste, een veiligere optie te midden van giftige dampen Hoe werken torpedomotoren onder water?
Hoe werken torpedomotoren onder water?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

