
Wetenschap
Onderzoekers ontdekken hoe een algemeen additief lithium-ionbatterijen een boost geeft
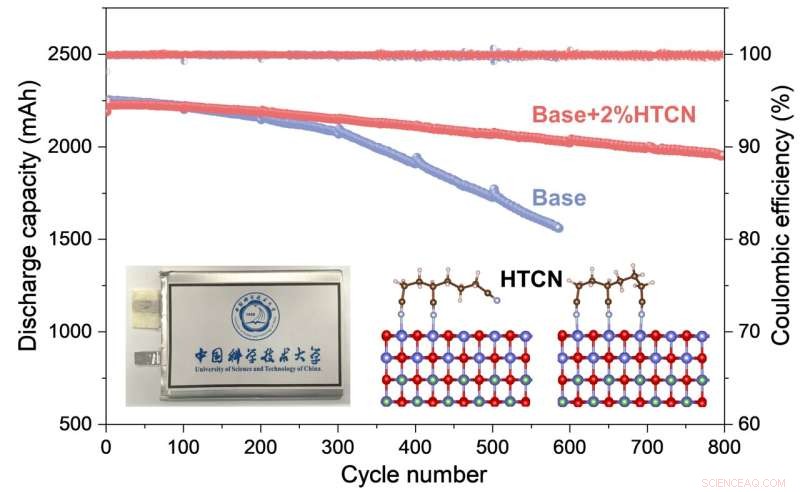
De elektrochemische prestaties en het werkmechanisme van HTCN-additief op hoogspannings LiCoO2 kathode voor praktische zakcellen worden uitgebreid bestudeerd. Krediet:Nano-onderzoek
Nitrillen - een organische verbinding met een koolstofatoom dat drievoudig is gebonden aan een stikstofatoom - worden vaak toegevoegd aan de elektrolytformule voor batterijen met behulp van een lithium-kobaltoxide-kathode, waardoor dergelijke batterijen veel dichter bij het realiseren van hun volledige theoretische prestaties komen. Tot nu toe hebben batterijonderzoekers niet echt begrepen waarom deze nitrillen op deze manier werken. Maar een groep elektrochemici heeft geavanceerde microscopietechnieken gebruikt om nauwkeuriger te kijken naar wat er op moleculaire schaal gebeurt en wat er aan de hand is, wat nieuwe wegen opent voor nog verdere verbeteringen van de batterijprestaties.
De studie werd gepubliceerd in het tijdschrift Nano Research op 22 sept. 2022..
Lithiumkobaltoxide (LiCoO2 , of gewoon "LCO") is het meest gebruikte materiaal voor kathoden - de positieve elektroden - in lithium-ionbatterijen. Dit geldt met name voor batterijen die worden gebruikt in draagbare elektronische apparaten dankzij de hoge bedrijfsspanning van LCO, de hoge capaciteit en de stabiliteit van de prestaties op de lange termijn.
Maar wat LCO-kathoden bijzonder aantrekkelijk heeft gemaakt, is dat ze meer energie bieden voor een kleinere hoeveelheid ruimte (grotere energiedichtheid), wat erg handig is voor kleinere consumentenapparaten zoals telefoons, smartwatches en gadgets die nog strengere ruimtebeperkingen hebben, zoals als huishoudelijke en industriële slimme sensoren.
Op dit moment kunnen LCO-kathoden echter slechts ongeveer de helft van hun theoretische specifieke capaciteit leveren. Dit betekent dat wat ze daadwerkelijk leveren veel minder is dan wat ze theoretisch zouden moeten kunnen produceren. En dus vinden ze het vaak moeilijk om te voldoen aan de toenemende energiedichtheidseisen van draagbare elektronica.
Een manier om deze hindernis te omzeilen zou zijn om de beperkte laadspanning van batterijen te verhogen met behulp van LCO-kathodes. De beperkte laadspanning beschrijft het punt waarop een batterij als volledig opgeladen wordt beschouwd. Voorbij dit punt kan de batterij worden beschadigd en zoveel apparaten worden gewoon uitgeschakeld wanneer de uitschakeldrempel wordt bereikt. Deze drempel is enigszins willekeurig ingesteld en zou dus kunnen worden verhoogd, en zo'n hoogspanningsbedrijf biedt veelbelovend voor het geven van een energiedichtheidsboost aan dergelijke batterijen.
Maar hier doet zich een nieuw probleem voor:werking met hoogspanning kan schadelijke chemische reacties op het grensvlak tussen de kathode en de elektrolyt verergeren. Dit kan scheuren en andere interne schade tot gevolg hebben, wat op zijn beurt het grensvlak tussen de elektroden verder kan verslechteren. Dit alles kan uiteindelijk leiden tot een radicale afname van de batterijcapaciteit en een sterke toename van veiligheidsproblemen. De werktemperatuur in deze apparaten kan oplopen tot 45℃ vanwege hun eigen warmteontwikkeling, wat de levensduur van de batterij verder verkort.
En dus al een tijdje, het mengen van extra verbindingen aan de elektrolytformule om de reactie-activiteit van de elektrolyt (het medium dat ionen bevat dat helpt een stroom te creëren via de beweging van positieve en negatieve ionen er doorheen) aan het grensvlak tussen de kathode te tweaken en elektrolyt is een zeer effectieve strategie gebleken om de activiteit van de elektrolytreactie te verminderen.
Er zijn een aantal verschillende verbindingen die als dergelijke elektrolytadditieven worden gebruikt, maar voor lithium-ionbatterijen zijn nitrillen misschien wel de meest gebruikte. Nitrillen zijn elke organische verbinding waarvan een deel van het molecuul (een functionele groep) bestaat uit een koolstofatoom dat drievoudig is gebonden aan een stikstofatoom.
Het werkingsmechanisme van nitriladditieven op hoogspanningskathoden is echter nog steeds niet volledig begrepen, met name in het soort praktische, alledaagse hoogspannings LCO-zakbatterijen. (Pouch-batterijen zijn een soort "zachte" batterij zonder een harde metalen behuizing, en in plaats daarvan zijn de componenten ingesloten in een met aluminium gecoate plastic film, die een beetje lijkt op een "etui" van kauwgom of losse tabak. Voor het eerst ontwikkeld in 1995 en waardoor een veel efficiënter gebruik van de ruimte mogelijk is, zijn zakbatterijen sindsdien een veelvoorkomende keuze geworden voor fabrikanten vanwege dit ontwerpvoordeel.)
Er zijn twee hoofdtheorieën die het mechanisme van nitriladditieven proberen te verklaren, maar beide hebben aanzienlijke tekortkomingen in hun verklarende kracht.
"Nitrillen werken goed, maar we weten niet echt waarom ze goed werken, waarom deze stabiliserende actie plaatsvindt. Wat er precies aan de hand is, is behoorlijk mysterieus gebleven", zegt Shuhong Jiao, een elektrochemicus aan de Universiteit van Wetenschap en Technologie van China (USTC). "En als we niet weten waarom wat we doen om batterijen te verbeteren werkt, dan weerhoudt dit ons ervan onze inspanningen om de zaken nog verder te verbeteren."
Dus namen de onderzoekers een veelgebruikt nitril-elektrolytadditief, tridentaatligand dat 1,3,6-hexaantricarbonitril (of eenvoudiger HTCN) bevat om te proberen licht te werpen op wat het mechanisme is van nitrillen bij het stabiliseren van hoogspannings-a LiCoO2 kathode.
Terwijl de batterij in bedrijf was en veel beter presteerde dan een equivalent zonder de HTCN-elektrolytadditieven, gebruikten de onderzoekers elektronenmicroscopie om nader te bekijken wat er gebeurde, gecombineerd met een analyse van de ionen- en elementaire samenstelling van het systeem. Ze ontdekten dat het HTCN-additief zeer effectief het ontstaan van scheuren en het oplossen van kobaltionen remde.
Vervolgens, met behulp van röntgenfoto-elektronspectroscopie gecombineerd met een reeks theoretische berekeningen, ontdekten ze dat de HTCN-moleculen efficiënt werden geadsorbeerd op (vastgehecht aan) het oppervlak van LCO en ingebed in het grensvlak tussen de kathode en de elektrolyt, die in turn sterk remmen een oxidatiereactie op het oppervlak van de LCO, waardoor een continue ontleding van de elektrolyt wordt voorkomen.
Al met al komt dit neer op een veel stabieler grensvlak tussen kathode en elektrolyt, wat de afbraak van componenten en de vorming van scheuren aanzienlijk onderdrukte. Het is deze stabiele en dichte kathode-elektrolytstructuur die de stabiliteit van de batterij verbetert door een groot aantal laad- en ontlaadcycli.
Met deze kennis op moleculair niveau van hoe nitriladditieven dergelijke batterijen een boost geven, kunnen onderzoekers nu op zoek gaan naar andere formuleringen van elektrolytadditieven die een vergelijkbare of betere interfacestructuur produceren. + Verder verkennen
Chemische additieven verbeteren de stabiliteit van lithium-ionbatterijen met hoge dichtheid
 Lipoproteïnen gedragen zich bijna als een kleine klittenbandbal
Lipoproteïnen gedragen zich bijna als een kleine klittenbandbal De forensische onbekenden van 3D-geprinte vuurwapens aanpakken
De forensische onbekenden van 3D-geprinte vuurwapens aanpakken HGF-remmend macrocyclisch peptide - mechanismen en potentiële kankertheranostica
HGF-remmend macrocyclisch peptide - mechanismen en potentiële kankertheranostica Röntgenexperimenten dragen bij aan studies van een medicijn dat nu is goedgekeurd om tuberculose te bestrijden
Röntgenexperimenten dragen bij aan studies van een medicijn dat nu is goedgekeurd om tuberculose te bestrijden Kookchemie minus hitte is gelijk aan nieuwe niet-giftige lijm
Kookchemie minus hitte is gelijk aan nieuwe niet-giftige lijm
 Bezorgd over de toekomst van de aarde? We zullen, de vooruitzichten zijn slechter dan zelfs wetenschappers kunnen bevatten
Bezorgd over de toekomst van de aarde? We zullen, de vooruitzichten zijn slechter dan zelfs wetenschappers kunnen bevatten Microplastics op Antarctica
Microplastics op Antarctica Welke menselijke activiteiten hebben een negatieve invloed op de oceaan?
Welke menselijke activiteiten hebben een negatieve invloed op de oceaan?  Ploegen, mulchen of direct zaaien:modellering van bodemstructuurveranderingen als belangrijk fundamenteel onderzoek
Ploegen, mulchen of direct zaaien:modellering van bodemstructuurveranderingen als belangrijk fundamenteel onderzoek Vogelinformatie voor kinderen
Vogelinformatie voor kinderen
Hoofdlijnen
- Hoe MRNA van een cel te isoleren
- Pyridine betrokken bij massale sterfte aan schaaldieren
- Met behulp van nieuwe techniek doen onderzoekers verrassende ontdekkingen over hoe vliegenhersenen reageren op smaken
- Verkoudheidsvirussen onthullen een van hun sterke punten
- Zeldzame fossiele tanden vernietigen lang gekoesterde opvattingen over de evolutie van gewervelde dieren
- Landbouwproductiviteit dreef de Euro-Amerikaanse nederzetting van Utah
- Een eerste blik op geografische variatie in ezelspinguïnoproepen
- Nieuw inzicht in unieke plantchemicaliën kan toekomstige medicijnontwikkeling informeren
- Zelfs wilde zoogdieren hebben regionale dialecten
- Air France zegt de capaciteit de komende twee maanden tussen 70 en 90% te verminderen

- Vier manieren waarop de Britse regering benzine moet uitfaseren, diesel- en hybride auto's tegen 2035

- AT&T-chef zegt dat fusie de waarde van Time Warner zou vergroten

- Het benutten van mariene energie op alle schalen, van een dorps microgrid tot een uitgestrekt zeegat

- Twitter-aandelen stijgen op terwijl de winst stijgt; Trump weegt mee

 Het co-evoluerende web van het leven als een netwerk begrijpen
Het co-evoluerende web van het leven als een netwerk begrijpen Welke soorten planten bevinden zich in het Midden-Amerikaanse tropische regenwoud?
Welke soorten planten bevinden zich in het Midden-Amerikaanse tropische regenwoud?  De technologie die Stephen Hawking een stem gaf, moet toegankelijk zijn voor iedereen die het nodig heeft
De technologie die Stephen Hawking een stem gaf, moet toegankelijk zijn voor iedereen die het nodig heeft Wetenschappers over het veiliger maken van de Large Hadron Collider
Wetenschappers over het veiliger maken van de Large Hadron Collider Het is overal een hel:Dorianen verzamelen in de verwoeste Bahama's
Het is overal een hel:Dorianen verzamelen in de verwoeste Bahama's Synthese van een bijna-infrarood lichtabsorberende macrocyclische aromatische verbinding
Synthese van een bijna-infrarood lichtabsorberende macrocyclische aromatische verbinding Eerste 3D-analyse van de stenen werktuigen van Afrikaanse jager-verzamelaars
Eerste 3D-analyse van de stenen werktuigen van Afrikaanse jager-verzamelaars Werkloosheid verhoogt aanzienlijk huiselijk geweld, nieuwe studie vondsten
Werkloosheid verhoogt aanzienlijk huiselijk geweld, nieuwe studie vondsten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

