
Wetenschap
HGF-remmend macrocyclisch peptide - mechanismen en potentiële kankertheranostica
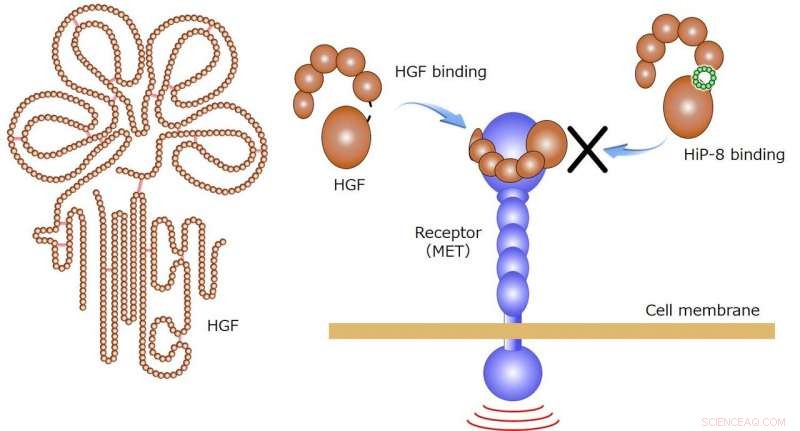
HGF oefent zijn fysiologische functies uit door te binden aan zijn receptor MET op het celmembraan. Na binding van HiP-8 aan HGF, HGF-binding aan de receptor MET wordt geremd (rechterkant van de figuur). Krediet:Kanazawa University
Hepatocytengroeifactor (HGF) is een eiwit dat fungeert als celgroeifactor. Door te binden aan zijn receptoreiwit MET op het celmembraan, het oefent zijn fysiologische functies uit, zoals proliferatie en migratie van cellen, evenals weefselherstel en regeneratie. Voor een kankerweefsel echter, omdat het de invasie en overleving van kankercellen bevordert, het kan een rol spelen bij de uitzaaiing van kanker en het verwerven van resistentie tegen geneesmiddelen tegen kanker. HGF bestaat in een voorlopervorm, inactieve HGF, in verschillende weefsels, maar de voorloper wordt alleen in de buurt van kankercellen omgezet in actief HGF. Om deze reden, moleculen die selectief actief HGF detecteren/remmen zijn zeer wenselijk, maar zijn tot nu toe niet beschreven.
Moleculair gerichte medicijnen die selectief specifieke moleculen remmen, zijn ontwikkeld en gebruikt voor de behandeling van kanker en voor andere ziekten. Onder andere, antilichamen vertonen een hoge specificiteit voor hun doelmoleculen, maar een van hun nadelen is hun zeer hoge kosten. Anderzijds, synthetische drugs zijn veel minder duur omdat ze chemisch kunnen worden gesynthetiseerd, maar hun specificiteit tegen hun doelmoleculen is niet hoog. Onlangs, veel aandacht is besteed aan macrocyclische peptiden, die een doelwitspecificiteit kunnen vertonen die zo hoog is als die van antilichamen en toch beschikbaar kan zijn door chemische synthese.
Het huidige onderzoeksteam van vijf instellingen, waaronder Kanazawa University, heeft met succes een macrocyclisch peptide ontdekt, HalloP-8, die zich bindt aan de actieve vorm van HGF om zijn activiteit te remmen, met behulp van de PaPID-methode. HiP-8 is een macrocyclisch peptide dat bestaat uit 12 aminozuurresiduen in een ringachtige geometrie (Figuur 1), binding aan actief HGF met een zeer hoge affiniteit en remming van HGF-binding aan zijn receptor, MET (Figuur 1).
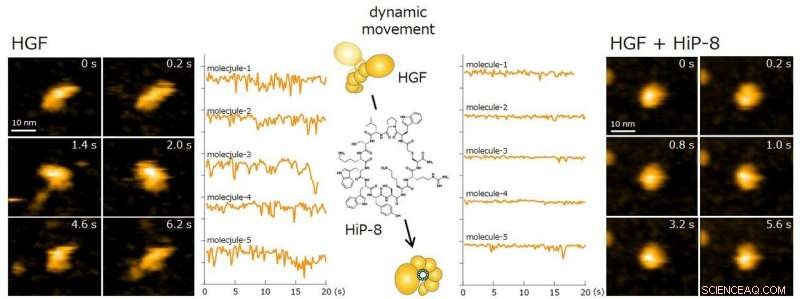
Gele lijnen tonen verandering in moleculaire vorm van HGF-moleculen. Terwijl HGF-morfologie dynamische beweging ondergaat, de dynamische beweging (moleculaire dynamica) werd sterk onderdrukt na binding van HiP-8. Krediet:Kanazawa University
In aanvulling, om de functionele interactie tussen HiP-8 en HGF op te helderen, deze studie maakte gebruik van snelle atoomkrachtmicroscopie (HS-AFM), ontwikkeld aan de Kanazawa University, waarmee visualisatie van de dynamiek en morfologie van biologische moleculen mogelijk is (Figuur 2). Dit onderzoek heeft met succes aangetoond dat, terwijl een actief HGF-molecuul dynamisch gedrag vertoonde, bij binding van HiP-8, de moleculaire dynamica van HGF werd sterk geremd. Deze nieuwe ontdekking toont aan dat de zeer dynamische aard van een eiwitmolecuul werd geremd door een klein molecuul.
Verder, beeldanalyse met behulp van positronemissietomografie (PET) en radioactief gelabeld HiP-8 toegediend aan muizen die gexenografeerd waren met menselijk longkankerweefsel, suggereren een mogelijke toepassing van HiP-8 bij de diagnose van kanker. HiP-8 accumuleerde selectief in kankerweefsel met actief HGF (Figuur 3), wat suggereert dat HiP-8 nuttig zou moeten zijn als een sonde voor de diagnose van PET-beeldvorming. Aangezien HiP-8 de HGF-activiteit remt, het zou ook kunnen worden gebruikt als een moleculair gericht medicijn tegen kanker dat selectief is voor actieve HGF.
De resultaten van de huidige studie zullen naar verwachting leiden tot de ontwikkeling van nieuwe diagnostische methoden voor PET met radiotracer HiP-8, een macrocyclisch peptide. HiP-8 is een kandidaat-molecuul van een nieuw moleculair gericht medicijn dat selectief alleen actief HGF remt.
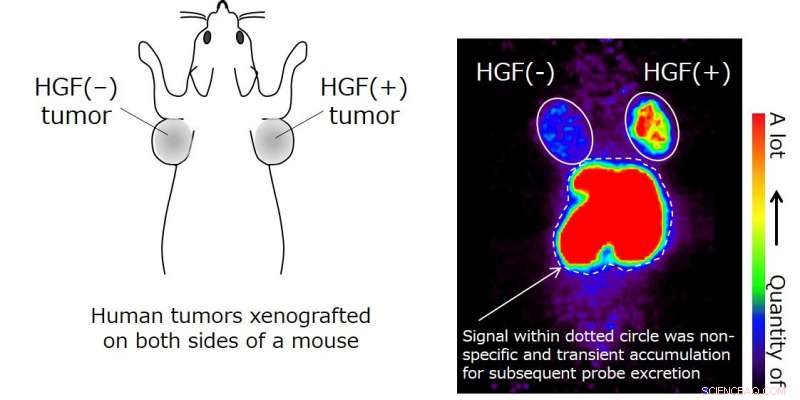
HiP-8 (probe) wordt waargenomen te worden geaccumuleerd in een HGF(+)-tumor (xenotransplantaat op een muis). Het HiP-8-signaal in de lever en de nieren duidt op de tijdelijke accumulatie van HiP-8 voor daaropvolgende uitscheiding. Het kankerweefsel waarin het HGF-gehalte hoger was, werd met een hoog contrast gevisualiseerd, vergeleken met HGF(?) tumor. Krediet:Kanazawa University
Hoofdlijnen
- Nieuwe bevindingen verduidelijken de rol van de schildklier bij seizoensveranderingen bij zoogdieren
- Achter de puppy-hondenogen
- Hoe schat ik de celgrootte met behulp van een microscoop?
- Nieuwe mechanismen ontdekt die bacteriën gebruiken om zichzelf te beschermen tegen antibiotica
- Kunnen planten denken?
- Noorwegen zet hek op om rendierslachting te stoppen
- Dominant Allele: wat is het? & Waarom gebeurt het? "(with Traits Chart)
- Wat is een allel?
- Difference Between Gap Junctions & Plasmodesmata
- Metaalreducerende bacteriën bieden een groenere route voor de productie van koperkatalysatoren
- Veranderingen in suikerachtige moleculen aan het oppervlak helpen kanker uitzaaien

- Heterometallische koper-aluminium superatoom ontdekt
- Extreem hard en toch metaalgeleidend:onderzoekers ontwikkelen nieuw materiaal met hightech-perspectieven
- Duurzame lijmen van de toekomst blijven niet plakken

 Natuurkundigen zien nucleair wiebelen in één isotoop van goud
Natuurkundigen zien nucleair wiebelen in één isotoop van goud De zeespiegel kan meer dan drie meter stijgen, toont nieuwe studie
De zeespiegel kan meer dan drie meter stijgen, toont nieuwe studie Vlucht van de levende doden:hoe animatie uitgestorven soorten weer tot leven brengt
Vlucht van de levende doden:hoe animatie uitgestorven soorten weer tot leven brengt Europa stikt in ijskoude smog
Europa stikt in ijskoude smog Levenscyclus van pinguïns
Levenscyclus van pinguïns  Nieuw materiaal gemaakt om de fossiele brandstofindustrie op te ruimen
Nieuw materiaal gemaakt om de fossiele brandstofindustrie op te ruimen Ierse drugsfabrikant Shire geconfronteerd met potentiële biedingsoorlog van $ 60 miljard
Ierse drugsfabrikant Shire geconfronteerd met potentiële biedingsoorlog van $ 60 miljard Wetenschappers kijken voor het eerst naar het geometrische fase-effect in een chemische reactie
Wetenschappers kijken voor het eerst naar het geometrische fase-effect in een chemische reactie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


