
Wetenschap
Hoeveel mol zitten er in 4,816 x 1024 formule-eenheden NaCl?
De atoommassa van Na is 22,99 g/mol en de atoommassa van Cl is 35,45 g/mol. Daarom is de molaire massa van NaCl:
$$22,99 \text{ g/mol} + 35,45 \text{ g/mol} =58,44 \text{ g/mol}$$
Nu kunnen we het aantal mol in 4,816 x 10^24 formule-eenheden NaCl berekenen met behulp van de volgende formule:
$$\text{Mollen} =\frac{\text{Massa in gram}}{\text{Molar massa}}$$
Als we de gegeven waarden in de formule vervangen, krijgen we:
$$\text{Moles} =\frac{4,816 \times 10^{24} \text{ formule-eenheden} \times 58,44 \text{ g/mol}}{6,022 \times 10^{23} \text{ formule-eenheden /mol}}$$
$$\text{Mollen} =4,01 \text{ mol}$$
Daarom zijn er 4,01 mol in 4,816 x 10^24 formule-eenheden NaCl.
 Het belang van milieubeheer
Het belang van milieubeheer  Nieuwe bronnen voor zeldzame metalen die essentieel zijn in moderne technologie
Nieuwe bronnen voor zeldzame metalen die essentieel zijn in moderne technologie Enorme behoefte aan groeiende bomen op boerderijen
Enorme behoefte aan groeiende bomen op boerderijen Great Barrier Reef-agentschap breekt met Australische gvt in klimaatwaarschuwing
Great Barrier Reef-agentschap breekt met Australische gvt in klimaatwaarschuwing Stikstofvervuilingsbeleid over de hele wereld loopt achter op wetenschappelijke kennis
Stikstofvervuilingsbeleid over de hele wereld loopt achter op wetenschappelijke kennis
Hoofdlijnen
- Wetenschappers ontdekken hoe bijen tijdens de bestuiving natuurlijke medicijnen tegen parasitaire infecties activeren
- Lab kweekt modulaire materialen op macroschaal uit bacteriën
- Saharastof:het goede,
- Optimale afstand bepaald voor geënte Primo Red hogetunneltomaat
- In het ei leren Amerikaanse brulkikkers hoe ze kunnen voorkomen dat ze een lunch worden
- Algoritmen gebruiken om het complexe fonetische alfabet van potvissen te decoderen
- Hoe lokale ecologische kennis bedreigde en zeldzame dieren kan redden
- Bloedmonsters tonen aan dat dodelijke kikkerschimmel in het wild aan het werk is
- Ecosysteemherstel is een integraal onderdeel van het herstel van de mensheid van COVID-19
- Fopspeenbiosensor kan helpen bij het bewaken van de gezondheid van pasgeborenen

- Nieuwe MD-simulatie werpt licht op het mysterie van de structuur van gehydrateerde elektronen

- Van nata de coco tot computerschermen:Cellulose krijgt een kans om te schitteren
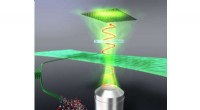
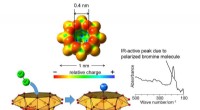
- Polarisatie van broommolecuul in vanadiumoxideclusterholte en nieuwe bromering van alkaan
- Levensrijk patroon:onderzoekers gebruiken geluid om de toekomst van printen vorm te geven

 Na de goudkoorts:mijnbouw in Kameroen laat open graven achter
Na de goudkoorts:mijnbouw in Kameroen laat open graven achter Merk-ID:is een auto mannelijk of vrouwelijk?
Merk-ID:is een auto mannelijk of vrouwelijk?  Hoe houdt de pH verband met de proliferatie van micro-organismen?
Hoe houdt de pH verband met de proliferatie van micro-organismen?  Celkarakteristieken
Celkarakteristieken Kunststof uit hout? Röntgenanalyse wijst de weg naar op maat gemaakte ligninegebaseerde componenten
Kunststof uit hout? Röntgenanalyse wijst de weg naar op maat gemaakte ligninegebaseerde componenten  Toen de dreiging van COVID-19 werd ervaren, werden mensen vrijgeviger
Toen de dreiging van COVID-19 werd ervaren, werden mensen vrijgeviger Andreev-chemie op een nanodraad:onderzoekers genereren supergeleidende paartoestanden, gescheiden door volwassen barrières
Andreev-chemie op een nanodraad:onderzoekers genereren supergeleidende paartoestanden, gescheiden door volwassen barrières  Astronomen hebben zojuist een komeet ontdekt die, als we hem volgend jaar zien, helderder zou kunnen zijn dan de meeste sterren. Of zal het?
Astronomen hebben zojuist een komeet ontdekt die, als we hem volgend jaar zien, helderder zou kunnen zijn dan de meeste sterren. Of zal het?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

