
Wetenschap
Hoe verschilt koolstof 14 van gewone koolstof?
Het belangrijkste verschil tussen koolstof 14 en gewone koolstof (koolstof 12) is dat koolstof 14 onstabiel is en na verloop van tijd vervalt. Dit betekent dat de hoeveelheid koolstof 14 in een object afneemt naarmate de tijd verstrijkt, wat het een waardevol hulpmiddel maakt voor radiometrische datering. De halfwaardetijd van koolstof 14 is 5.730 jaar, wat betekent dat het 5.730 jaar duurt voordat de helft van de koolstof 14 in een object is vergaan.
Het verval van koolstof 14 wordt ook gebruikt bij koolstof-14-datering, een wetenschappelijke techniek waarmee onderzoekers de ouderdom van een object tot ongeveer 50.000 tot 60.000 jaar oud kunnen bepalen. Koolstof-14-datering wordt veel gebruikt in de archeologie, paleontologie en andere gebieden die de ouderdom van oude artefacten en fossielen bestuderen.
Koolstof 14 wordt ook gebruikt in de geneeskunde en andere wetenschappelijke gebieden. Het wordt bijvoorbeeld gebruikt bij medische beeldvorming om artsen te helpen medische aandoeningen te diagnosticeren en te behandelen. Koolstof 14 wordt ook gebruikt in tracerstudies om de beweging van stoffen in het milieu of in biologische systemen te volgen.
 Wetenschappers reconstrueren het lente-hydroklimaat met behulp van levende en dode alpenjeneverbesstruiken
Wetenschappers reconstrueren het lente-hydroklimaat met behulp van levende en dode alpenjeneverbesstruiken NASA krijgt een kijkje in de regenval binnen Typhoon Kong-Rey
NASA krijgt een kijkje in de regenval binnen Typhoon Kong-Rey Oude vulkanen onthullen de gerecyclede aardkorst
Oude vulkanen onthullen de gerecyclede aardkorst Wat gebeurt er in de pop van een vlinder?
Wat gebeurt er in de pop van een vlinder?  Synchrotron werpt röntgenlicht op koolstofchemie op oceaanoppervlakken
Synchrotron werpt röntgenlicht op koolstofchemie op oceaanoppervlakken
Hoofdlijnen
- Ontdekking vergroot het begrip hoe bacteriën zich verspreiden
- Hoe slapende borststamcellen in de puberteit worden gewekt
- Hoe verslaving werkt
- Het gedrag van primaten veranderde toen dierentuinen gesloten waren wegens pandemie, suggereert onderzoek
- Hoe bacteriën omgaan met stress
- Brassica-ziekte verslaan:hoe behandeling met aminozuren ziekten kan voorkomen
- Onderzoekers tonen aan dat de besmetting met pesticiden verder gaat dan alleen de schil van de appel
- Onderzoekers streven naar een beter begrip van hoe cellen werken
- Hoe het markeren van genen vóór de celdeling hun daaropvolgende reactivering versnelt
- Studie effent de weg voor nieuwe lichtgevoelige materialen

- Wetenschappers ontdekken nieuwe oorsprong van chemische reacties van het leven

- Chemici ontwikkelen verschillende industrieel belangrijke synthetische processen

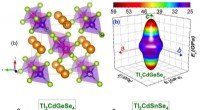
- Onderzoek naar nieuw gesynthetiseerde thalliumverbindingen voor opto-elektronische apparaten
- Unieke dendritische kleverige deeltjes gevormd door het benutten van vloeibare chaos
 Luchtvaartmaatschappijen rekenen op zakenreizigers om het herstel gaande te houden
Luchtvaartmaatschappijen rekenen op zakenreizigers om het herstel gaande te houden Welk instrument wordt gebruikt bij het bestuderen van cellen?
Welk instrument wordt gebruikt bij het bestuderen van cellen?  TVA controleert op gifstoffen uit steenkool bij de watervoorziening van Memphis
TVA controleert op gifstoffen uit steenkool bij de watervoorziening van Memphis Gerechtigheid voor iedereen:hoe ras en Amerikaanse identiteit de politiek kunnen beïnvloeden
Gerechtigheid voor iedereen:hoe ras en Amerikaanse identiteit de politiek kunnen beïnvloeden  Knoopjes in de resonator:elegante wiskunde in nederige natuurkunde
Knoopjes in de resonator:elegante wiskunde in nederige natuurkunde Mensen gebruikten noordelijke migratieroutes om Oost-Azië te bereiken
Mensen gebruikten noordelijke migratieroutes om Oost-Azië te bereiken Komt de gemanipuleerde 'Frankenfish' naar de tafel van het land?
Komt de gemanipuleerde 'Frankenfish' naar de tafel van het land?  Hoe overtuigend is een Y-chromosoomprofielmatch tussen verdachte en plaats delict?
Hoe overtuigend is een Y-chromosoomprofielmatch tussen verdachte en plaats delict?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

