
Wetenschap
Waarom hebben de bollen stikstof en zuurstof verschillende kleuren?
Over het algemeen wordt de kleur van een object bepaald door de manier waarop het met licht interageert. Wanneer licht een voorwerp raakt, wordt een deel van het licht geabsorbeerd en een deel gereflecteerd. De kleur van het object wordt bepaald door de golflengten van het licht dat wordt gereflecteerd.
In het geval van stikstof en zuurstof zorgt het verschil in elektronenconfiguratie ervoor dat de twee elementen verschillende golflengten van licht absorberen en reflecteren. Stikstofgas is kleurloos, terwijl zuurstofgas lichtblauw is. Dit komt omdat stikstofgas licht absorbeert in de rode en violette gebieden van het spectrum, terwijl zuurstofgas licht absorbeert in de rode en gele gebieden van het spectrum.
De verschillende kleuren stikstof en zuurstof worden ook weerspiegeld in hun fysieke eigenschappen. Stikstofgas is een kleurloos, geurloos en smaakloos gas dat lichter is dan lucht. Zuurstofgas is een kleurloos, geurloos en smaakloos gas dat iets zwaarder is dan lucht.
 Vergeleken met water heeft ijs een lagere waarde waardoor het kan blijven drijven.?
Vergeleken met water heeft ijs een lagere waarde waardoor het kan blijven drijven.?  Waarom neemt het kookpunt toe wanneer de atomaire radius toeneemt in halogenen?
Waarom neemt het kookpunt toe wanneer de atomaire radius toeneemt in halogenen?
De halogenen omvatten fluor, chloor, broom, jodium en astatine. Bij kamertemperatuur zijn de lichtere halogenen gassen, is broom een vloeistof en zijn de zwaardere ha
 Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren
Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren Superstaalproject bereikt grote doorbraak
Superstaalproject bereikt grote doorbraak Nieuwe simulatietool bevordert de moleculaire modellering van biomoleculaire condensaten
Nieuwe simulatietool bevordert de moleculaire modellering van biomoleculaire condensaten
 Jongeren gaan de straat op voor het klimaat:wie zijn zij?
Jongeren gaan de straat op voor het klimaat:wie zijn zij?  Ratten uitroeien om koraalriffen te versterken
Ratten uitroeien om koraalriffen te versterken Effecten van dag- en nachttemperaturen op de vegetatieproductiviteit in moerassen van het Qinghai-Tibet-plateau
Effecten van dag- en nachttemperaturen op de vegetatieproductiviteit in moerassen van het Qinghai-Tibet-plateau De effecten van straling op planten
De effecten van straling op planten Stroomgebiedgroepen hebben een positieve invloed op de lokale waterkwaliteit, studie vondsten
Stroomgebiedgroepen hebben een positieve invloed op de lokale waterkwaliteit, studie vondsten
Hoofdlijnen
- Waarom evolutie vaak de voorkeur geeft aan kleine dieren en andere organismen
- Belangrijke verbeteringen onthuld op Closer to Van Eyck webapplicatie
- Minimale zuurstofconcentratie voor menselijke ademhaling
- Bloem of vlees? Genetica verklaart de voorkeur van muggen
- De reputatie van een bedrijf is wat kapot gaat als zijn boeken gaar worden
- Welke celstructuur van de plant mist jouw dierlijke cel?
- Vogelambassadeurs en tribale perspectieven:een vogelperspectief van voorgeschreven vuur
- 5 manieren waarop je hersenen je emoties beïnvloeden
- Voorspellen wat er met een dierlijke cel kan gebeuren als je hem in gedestilleerd water stopt?
- Radiale synthese is baanbrekend voor chemisch onderzoek en productie

- Nieuwe technologie kan wetshandhavers helpen kleinere hoeveelheden fentanyl met een hogere mate van nauwkeurigheid te detecteren
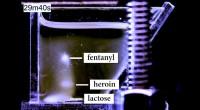
- Metaalionkatalysatoren en waterstofperoxide kunnen de plasticproductie groener maken

- Betere oplossingen voor het maken van waterstof liggen misschien net aan de oppervlakte

- Ontdekken hoe T-cellen het SARS-COV-2 virus spike-eiwit herkennen
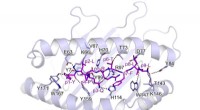
 Wat zit er achter de dramatische stijging van het aantal huishoudens van drie generaties?
Wat zit er achter de dramatische stijging van het aantal huishoudens van drie generaties? Wetenschappers onthullen een explosief geheim verborgen onder schijnbaar betrouwbare vulkanen
Wetenschappers onthullen een explosief geheim verborgen onder schijnbaar betrouwbare vulkanen Je brein op Mars:hoe wetenschappers de mentale prestaties van astronauten tijdens missies volgen
Je brein op Mars:hoe wetenschappers de mentale prestaties van astronauten tijdens missies volgen Wat stinkt maar kan een auto van brandstof voorzien?
Wat stinkt maar kan een auto van brandstof voorzien?  Wetenschappers maken alternatieve kunststoffen met alleen suikers en CO2
Wetenschappers maken alternatieve kunststoffen met alleen suikers en CO2  Onderzoekers vinden dat RNA-bewerkingssites waarschijnlijk een belangrijkere rol spelen bij genetische ziekten
Onderzoekers vinden dat RNA-bewerkingssites waarschijnlijk een belangrijkere rol spelen bij genetische ziekten  Kleine bossen zijn belangrijker dan eerder werd gedacht
Kleine bossen zijn belangrijker dan eerder werd gedacht Nieuw onderzoek bepaalt of politieke luchtoorlog of grondspel het meest effectief is
Nieuw onderzoek bepaalt of politieke luchtoorlog of grondspel het meest effectief is
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

