
Wetenschap
Welke functie heeft natriumhydroxide als oplosmiddel?
Natriumhydroxide is een polair oplosmiddel vanwege de aanwezigheid van het sterk elektronegatieve hydroxide-ion (OH-). Het kan verschillende polaire en ionische verbindingen oplossen, zoals zouten, metaaloxiden en sommige organische verbindingen die polaire functionele groepen bevatten (bijvoorbeeld alcoholen, carbonzuren en aminozuren).
Hoge oplosbaarheid van anorganische verbindingen :
Natriumhydroxide staat bekend om zijn vermogen om veel anorganische verbindingen op te lossen, zoals metaalhydroxiden, oxiden, carbonaten en fosfaten.
Dit komt omdat NaOH een sterke base is die met deze verbindingen kan reageren om oplosbare producten te vormen.
Wanneer bijvoorbeeld natriumhydroxide wordt toegevoegd aan koper(II)oxide, reageert het onder vorming van een oplosbaar natriumkoper(II)hydroxidecomplex.
Verzepingsreacties :
Natriumhydroxide wordt veel gebruikt bij de vervaardiging van zepen via een proces dat verzeping wordt genoemd. Verzeping omvat de reactie van vetten en oliën (triglyceriden) met natriumhydroxide om glycerol en natriumzouten van vetzuren te produceren, wat zepen zijn.
Deze reactie vormt de basis voor het maken van verschillende schoonmaakproducten, waaronder zeep, vloeibare zeep en wasmiddelen.
Cellulose oplossen :
Natriumhydroxide is in staat cellulose op te lossen, een hoofdbestanddeel van plantencelwanden. Deze eigenschap is van cruciaal belang in verschillende industrieën, waaronder de papierproductie, de textielproductie en de productie van biologisch afbreekbare verpakkingsmaterialen. Natriumhydroxide wordt gebruikt om cellulosevezels af te breken, waardoor ze zachter en beter hanteerbaar worden voor verwerking.
Productie van andere chemicaliën :
Natriumhydroxide dient als voorloper voor de productie van talrijke anorganische en organische chemicaliën. Het wordt bijvoorbeeld gebruikt bij de vervaardiging van natriumhypochloriet (bleekmiddel), natriumnitraat (kunstmest) en natriummetaal. Het wordt ook gebruikt bij de synthese van verschillende organische verbindingen zoals natriumacetaat, natriumformiaat en natriumfenoxide.
 Geleidt vast natriumchloride een elektrische stroom?
Geleidt vast natriumchloride een elektrische stroom?  Leg uit waarom de houder met water moet worden omgekeerd wanneer een gas wordt opgevangen door waterverplaatsing?
Leg uit waarom de houder met water moet worden omgekeerd wanneer een gas wordt opgevangen door waterverplaatsing?  Een virtueel substraat opent de weg naar oxidefilms op silicium voor toepassing in 5G, MEMS, sensoren en kwantumberekening
Een virtueel substraat opent de weg naar oxidefilms op silicium voor toepassing in 5G, MEMS, sensoren en kwantumberekening Nieuwe sneltest detecteert kwaliteit en authenticiteit van olijfolie
Nieuwe sneltest detecteert kwaliteit en authenticiteit van olijfolie Waarom zijn er 4 NH3's in de volgende vergelijking Cu2 plus (aq) NH3(aq) Cu(NH3)42 (aq)?
Waarom zijn er 4 NH3's in de volgende vergelijking Cu2 plus (aq) NH3(aq) Cu(NH3)42 (aq)?
 Greenpeace vindt koraalrif in boorgebied Totals Amazon
Greenpeace vindt koraalrif in boorgebied Totals Amazon Verbeterde naleving van het gemeenschappelijk landbouwbeleid met openbaar beschikbare en door gebruikers gegenereerde gegevens
Verbeterde naleving van het gemeenschappelijk landbouwbeleid met openbaar beschikbare en door gebruikers gegenereerde gegevens Hoe vliegvissen onze band met wilde dieren versterkt en inspanningen voor natuurbehoud bevordert
Hoe vliegvissen onze band met wilde dieren versterkt en inspanningen voor natuurbehoud bevordert  Onderzoekers ontdekken dat hoe meer overstromingsfactoren er zijn, hoe extremer een overstroming is
Onderzoekers ontdekken dat hoe meer overstromingsfactoren er zijn, hoe extremer een overstroming is  Slimme krimp in kleine steden gedreven door sterke sociale infrastructuur, uit onderzoek blijkt
Slimme krimp in kleine steden gedreven door sterke sociale infrastructuur, uit onderzoek blijkt
Hoofdlijnen
- Keizerspinguïns kunnen record snel inkorten door te snacken
- Kleine dierenharen kunnen werken als gevoelige kompasnaalden
- Zonneboerderijen een smet op het landschap? Onderzoek toont aan dat ze dieren in het wild ten goede kunnen komen
- Onderzoeker ontdekt wat atleten nodig hebben om goed te presteren
- Burn-out eist zware financiële tol van diergeneeskunde
- Verschil tussen een eencellige protoctist en bacterie?
- Hoe cellen hun afval afvoeren
- Computersimulaties visualiseren hoe een essentieel stamceleiwit verpakt DNA opent
- Waarom herkristalliseert ghb?
- Zeewier:van superfood tot supergeleider
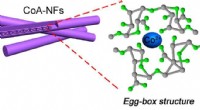
- Adsorberend materiaal ontwikkeld uit PET-flessen voor het verwijderen van antibiotica uit water
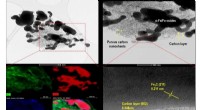
- Onderzoek details regulering van een multi-drug transporter

- Uraniumchemie en geologische berging van radioactief afval

- Plasticvervuiling:Chemische recycling kan een oplossing bieden

 Meiosis 1: Stadia & belang in celdeling
Meiosis 1: Stadia & belang in celdeling  Hoe COVID-19 heeft veranderd waar we naar kijken en hoe we ernaar kijken
Hoe COVID-19 heeft veranderd waar we naar kijken en hoe we ernaar kijken Nieuw rapport werpt licht op grensoverschrijdende ontheemding
Nieuw rapport werpt licht op grensoverschrijdende ontheemding Rapport over seismische contextmetingen voor geïnduceerde seismiciteit
Rapport over seismische contextmetingen voor geïnduceerde seismiciteit Magnetische T-Budbots gemaakt van theeplanten doden en reinigen biofilms
Magnetische T-Budbots gemaakt van theeplanten doden en reinigen biofilms Wat zal de toestand van natriumchloride zijn bij 100 graden Celsius?
Wat zal de toestand van natriumchloride zijn bij 100 graden Celsius?  Crime-scene techniek identificeert asteroïde sites
Crime-scene techniek identificeert asteroïde sites Hoe liter om te zetten naar kilogram bij het berekenen van massa
Hoe liter om te zetten naar kilogram bij het berekenen van massa
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

