
Wetenschap
Onderzoek details regulering van een multi-drug transporter

(van links naar rechts):Reza Dastvan, doctoraat, Smriti Mishra, doctoraat, en Hassane Mchaourab, doctoraat, bestuderen de innerlijke werking van een eiwitpomp die bijdraagt aan de resistentie tegen kankerchemotherapie. Krediet:Vanderbilt University
Onderzoekers van Vanderbilt University hebben ontdekt hoe een eiwitpomp onderscheid maakt tussen chemicaliën die het uit een cel zal verdrijven en remmers die de werking ervan blokkeren.
De pomp, genaamd P-glycoproteïne, beschermt cellen door potentieel schadelijke chemicaliën te verwijderen, maar het draagt bij aan resistentie tegen geneesmiddelen wanneer die chemicaliën therapeutische medicijnen zijn - wat een bijzonder probleem vormt voor de behandeling van kanker. De nieuwe bevindingen, gerapporteerd in het journaal Wetenschap , zou de ontwikkeling van efficiëntere remmers kunnen leiden om resistentie van kankercellen tegen chemotherapie te voorkomen.
De onderzoeken beantwoordden een al lang bestaande vraag over P-glycoproteïne, zei Hassane Mchaourab, doctoraat, Louise B. McGavock Hoogleraar Moleculaire Fysiologie en Biofysica.
Mchaourab beschrijft P-glycoproteïne als een tweedelige moleculaire machine:een motor die ATP verbrandt en een transmembraandomein dat een doorgang biedt voor het substraat (een molecuul dat door de transporter wordt verplaatst). ATP-energie die door de motor wordt gebruikt, drijft de conformatieveranderingen aan die chemicaliën uit cellen verwijderen.
Wat niet duidelijk was, is "hoe de ATP-motor weet dat een chemische stof is gebonden in het transmembraandomein dat een moleculaire 'mijl' verwijderd is, ' zei Mchaourab.
"In mensen, deze transporter spuugt chemicaliën uit, waaronder antibiotica, geneesmiddelen tegen kanker chemotherapie, antidepressiva, opioïden … wat maakt een molecuul tot een substraat voor deze opmerkelijk diverse pomp, en wat maakt een molecuul tot een remmer?"
De huidige onderzoeken volgen bevindingen die Mchaourab en zijn collega's in het tijdschrift hebben gerapporteerd Natuur twee jaar geleden. P-glycoproteïne heeft twee ATP-verbrandingsplaatsen, en ontdekten de onderzoekers met behulp van een spectroscopiemethode (dubbele elektron-elektronenresonantie, DEER) dat de twee sites structureel asymmetrisch zijn:eerst één site en dan verbrandt de tweede site ATP. Ze ontdekten ook dat de twee opeenvolgende stappen verband houden met substraatherkenning.
Mchaourab herinnert zich de wetenschapsschrijver Bill Snyder van het Vanderbilt University Medical Center die een vraag stelde die hem deed stilstaan:waarom zou de natuur een asymmetrische motor ontwerpen?
"Ik antwoordde dat dit misschien de manier is waarop de transporteur weet of hij geladen is met substraat of niet, "Zei Mchaourab. "Maar we hadden al onze experimenten gedaan met aanwezig substraat, want zo werkt de transporter." De onderzoekers hadden de structuur van de ATP-verbrandingsplaatsen niet onderzocht in afwezigheid van substraat.
"Het was een vrijdag, en ik werd die nacht wakker met de vraag van Bill, "Mchaourab herinnerde zich. "Op maandag, Ik vroeg Reza (een postdoctoraal onderzoeker) om de experimenten te herhalen en het substraat te verwijderen. En voila, de motor werd symmetrisch - het maakte niet uit welke kant het eerst ATP verbrandde."
In aanvullende onderzoeken met P-glycoproteïneremmers van de derde generatie, de onderzoekers ontdekten dat deze remmers ook een symmetrische toestand stabiliseren, maar een die verschilt van de lege staat.
"Een remmer bindt de transporter vast zodat deze niet naar de asymmetrische toestand kan gaan en de krachtslag niet kan uitvoeren - de stap waarbij de transporter zich verplaatst van wat we naar binnen gericht naar naar buiten kijken en de substraat, ' zei Mchaourab.
Het kennen van de verschillende conformaties van P-glycoproteïne die worden gestabiliseerd door substraten versus remmers, zal het mogelijk maken om te screenen op effectievere remstofmoleculen. Het kan onderzoekers ook helpen begrijpen waarom bestaande remmers slecht presteerden in klinische onderzoeken.
"P-glycoproteïne is zo'n belangrijk klinisch doelwit, "Zei Mchaourab. "Nu realiseren we ons dat remmers ook werken op de asymmetrie van de motor. P-glycoproteïne weet of het leeg is, of als het is gebonden aan een substraat of remmer door het niveau van asymmetrie te moduleren."
 Ethyleensensor kan helpen bij het bewaken van de gezondheid van planten
Ethyleensensor kan helpen bij het bewaken van de gezondheid van planten Nieuwe schaal voor elektronegativiteit herschrijft het leerboek scheikunde
Nieuwe schaal voor elektronegativiteit herschrijft het leerboek scheikunde Polymeer afgeleid van materiaal in de schelpen van garnalen kan geneesmiddelen tegen kanker afleveren op tumorplaatsen
Polymeer afgeleid van materiaal in de schelpen van garnalen kan geneesmiddelen tegen kanker afleveren op tumorplaatsen Structuren in zeewier werpen licht op duurzaamheid
Structuren in zeewier werpen licht op duurzaamheid Onderzoekers ontwikkelen bionisch blad voor gedistribueerde landbouw
Onderzoekers ontwikkelen bionisch blad voor gedistribueerde landbouw
 NASA analyseert zware regenval in het middenwesten van de VS, zware stormen
NASA analyseert zware regenval in het middenwesten van de VS, zware stormen Onderzoekers gebruiken machine learning om olieproductie te ondersteunen
Onderzoekers gebruiken machine learning om olieproductie te ondersteunen Stedelijke geofoonarray biedt een nieuwe kijk op het noordelijke bekken van Los Angeles
Stedelijke geofoonarray biedt een nieuwe kijk op het noordelijke bekken van Los Angeles Soorten neerslag
Soorten neerslag Instorting van de Europese ijskap veroorzaakt chaos
Instorting van de Europese ijskap veroorzaakt chaos
Hoofdlijnen
- De sleutelrol van enzymen in de embryonale ontwikkeling begrijpen
- Structurele inzichten in processen op DNA-schadeplekken
- Afrikaanse pinguïns blijken samen te werken om vissen bijeen te jagen om te foerageren
- The Differences Between Kinetochore & Nonkinetochore
- Kwallen op het menu
- Gen-experts gaan ongediertebestrijding aanpakken
- Radartracking onthult hoe bijen een route tussen bloemen ontwikkelen
- Bio-ingenieurs ontdekken mechanisme dat krachtpatsers van cellen reguleert
- Welke soorten cellen delen door mitose en cytokinese?
- Nieuwe grieptest gemakkelijk als ademen, met sneller resultaat

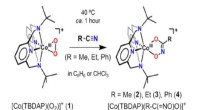
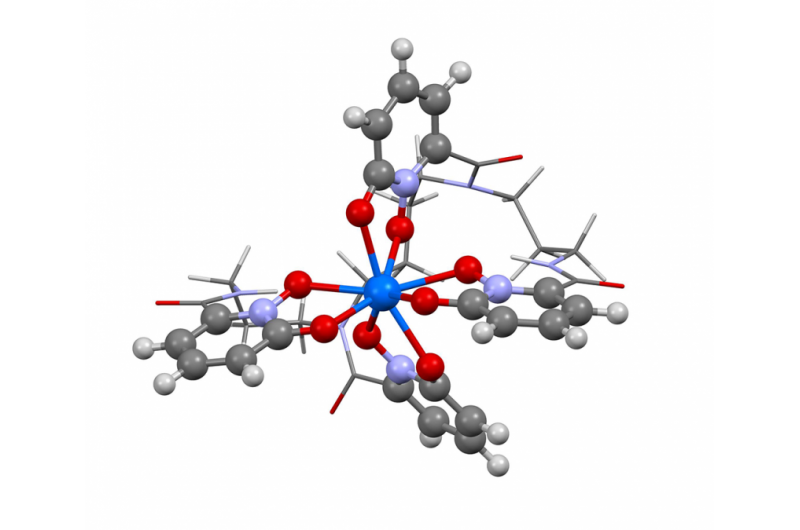
- Nieuw complex dat reageert met nitril - een sleutel om down-regulatie van kanker-enzymen mogelijk te maken
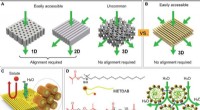
- Zelf-geassembleerd membraan met water-continue transportroutes voor nauwkeurige nanofiltratie
- Supercomputing bootst berkelium-experimenten na om nieuwe vondst te valideren
- Hoe beïnvloedt Temp de groeisnelheid van kristallen?

 Afbeelding:draagbaar apparaat voor ruimtegeneeskunde van EveryWear
Afbeelding:draagbaar apparaat voor ruimtegeneeskunde van EveryWear Meer stress en lagere overlevingskansen voor vogels bij jonge, beheerde bossen
Meer stress en lagere overlevingskansen voor vogels bij jonge, beheerde bossen Anti-vervalste vingerafdrukken gemaakt van zilveren nanodraden
Anti-vervalste vingerafdrukken gemaakt van zilveren nanodraden Facebook weigert opnieuw politieke advertenties te verbieden, zelfs valse
Facebook weigert opnieuw politieke advertenties te verbieden, zelfs valse Interessante feiten over driehoeken in Math
Interessante feiten over driehoeken in Math Licht verplaatsen over een halfgeleidende nanodraad via akoestische oppervlaktegolven
Licht verplaatsen over een halfgeleidende nanodraad via akoestische oppervlaktegolven Levende cellen en batterijen:met een beetje grafeen kom je een heel eind
Levende cellen en batterijen:met een beetje grafeen kom je een heel eind Oude mensen hebben mogelijk patronen en sculpturen gemaakt op de stranden van Zuid-Afrika
Oude mensen hebben mogelijk patronen en sculpturen gemaakt op de stranden van Zuid-Afrika
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Norway | Swedish | Danish |

-
Wetenschap © https://nl.scienceaq.com

