
Wetenschap
Onderzoekers onderzoeken waterstofbruggen met nieuwe techniek
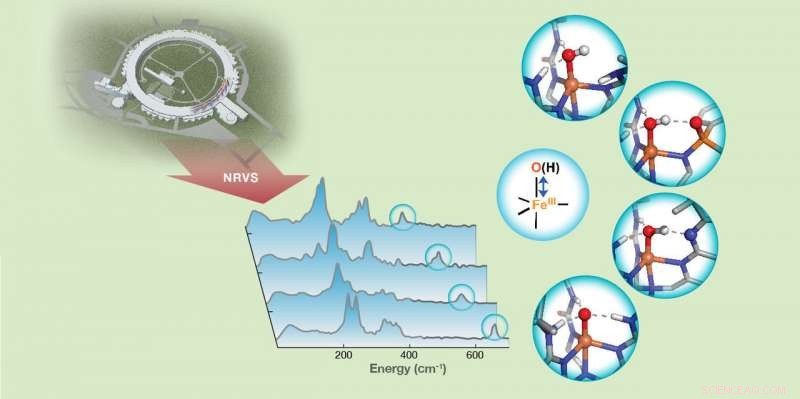
De sterkte van de waterstofbinding aan ijzer(III)-oxido/hydroxydo (FeIII-O/OH)-eenheden in niet-heem-ijzercomplexen wordt onthuld door FeIII-O/OH-rektrillingen gedetecteerd met 57Fe-kernresonantievibratiespectroscopie (NRVS). Krediet:Carnegie Mellon University
Onderzoekers van de Carnegie Mellon University hebben trillingsspectroscopie met kernresonantie gebruikt om de waterstofbruggen te onderzoeken die de chemische reactiviteit van enzymen moduleren, katalysatoren en biomimetische complexen. De techniek zou kunnen leiden tot de ontwikkeling van betere katalysatoren voor gebruik in een breed scala van gebieden. De bevindingen werden gepubliceerd als een "Very Important Paper" in het nummer van 3 december van Angewandte Chemie en vermeld op de achterkant van het tijdschrift.
Waterstofbindingen behoren tot de meest fundamentele interacties in de biologie en chemie. Ze zijn verantwoordelijk voor veel van de chemisch belangrijke eigenschappen van water, voor het stabiliseren van de structuren van eiwitten en nucleïnezuren, inclusief die gevonden in DNA en RNA, en dragen bij aan de structuur van natuurlijke en synthetische polymeren.
Onderzoek heeft aangetoond dat waterstofbruggen een belangrijke rol spelen bij het afstemmen van de reactiviteit van de metaalcentra van metallo-enzymen en metaalhoudende katalysatoren. Echter, er is weinig onderzoek gedaan om experimenteel aan te tonen hoe systematische veranderingen in waterstofbruggen binnen de secundaire coördinatiesfeer - moleculen die in de buurt van metaalcentra worden gevonden die geen directe bindingsinteracties met het centrum hebben - de katalytische activiteit beïnvloeden.
Bij katalyse, enzymen of synthetische katalysatoren stimuleren een keten van chemische reacties, die een aantal tussenliggende structuren of soorten voortbrengen. Het begrijpen van die structuren en hun chemische eigenschappen is de sleutel tot het begrijpen van de hele reactie.
"Het grondig begrijpen van de chemische reactiviteit van het reactieve tussenproduct is een belangrijke stap om te bepalen hoe zeer efficiënte en selectieve katalysatoren voor CH-functionalisatie kunnen worden ontworpen, " zei Yisong Guo, assistent-professor scheikunde aan Carnegie Mellon en de hoofdauteur van de studie. "In het geval van dizuurstof-activerende enzymen, de belangrijkste tussenproducten van katalyse zijn ijzer-oxo (Fe-O) en ijzer-hydroxo (Fe-OH) soorten, die betrokken zijn bij belangrijke biologische processen, zoals DNA-biosynthese, DNA- en RNA-reparatie, post-translationele modificatie van eiwitten, biosynthese van antibiotica en afbraak van toxische verbindingen."
Guo en collega's gebruikten 57Fe kernresonantie vibratiespectroscopie (NRVS), een nieuw ontwikkelde techniek op basis van synchrotronstraling, om de trillingsfrequentie te detecteren van Fe-O- en Fe-OH-eenheden van synthetische complexen die interageren met de secundaire coördinatiesfeer via waterstofbruggen. Veranderingen in de frequenties onthulden waardevolle informatie over de bindingssterkten van deze eenheden en verschaften verder een kwalitatieve maatstaf voor de waterstofbindingssterkte.
"Hieruit bleek dat NRVS een gevoelige techniek is om zeer kleine veranderingen in de sterkte van waterstofbruggen op te vangen, tot de veranderingen van een enkele waterstofbrug. Dit biedt ons een nieuwe methode om veranderingen in bindingssterkte van Fe-O- en Fe-OH-eenheden te koppelen aan hun chemische reactiviteit, ' zei Guo.
Guo zegt dat deze studie een proof-of-concept is voor het gebruik van NRVS om waterstofbruggen te onderzoeken. Hij is van plan deze methode te blijven gebruiken om meer ijzer-oxo- en ijzer-hydroxo-soorten in zowel synthetische complexen als enzymen te bestuderen om de hoeveelheid beschikbare gegevens op te bouwen om de chemische reactiviteit van deze soorten te correleren met de veranderingen van waterstofbruginteracties, in de hoop dat die informatie kan worden gebruikt om efficiëntere en effectievere katalysatoren te ontwikkelen.
 Als u azijn verdunt, hoe zal dit de pH-waarde beïnvloeden?
Als u azijn verdunt, hoe zal dit de pH-waarde beïnvloeden?  Vanadiumafhankelijke stikstofase kan twee CO-moleculen tegelijk binden
Vanadiumafhankelijke stikstofase kan twee CO-moleculen tegelijk binden Onderzoek kan ongewenste bijwerkingen bij nieuwe medicijnen minimaliseren
Onderzoek kan ongewenste bijwerkingen bij nieuwe medicijnen minimaliseren Moleculaire additieven verbeteren de mechanische eigenschappen van organisch zonnecelmateriaal
Moleculaire additieven verbeteren de mechanische eigenschappen van organisch zonnecelmateriaal Katoen maken dat brandveilig en comfortabel is
Katoen maken dat brandveilig en comfortabel is
Hoofdlijnen
- Is maretak meer dan alleen een excuus voor een kus?
- Medaka-vissen gebruiken gezichten om verschillende individuen te identificeren
- Wat zijn de belangrijkste functionele kenmerken van alle organismen?
- Soorten monomeren
- Muggen dragen bij warm weer vaker het denguevirus over
- Kan gezichtsblindheid verklaren waarom die persoon op het werk mij nooit gedag zegt?
- Onderzoek onthult hoe klimaatverandering de aquacultuur van Hawaiiaanse visvijvers kan beïnvloeden
- Maak kennis met Cheddar Man:Your New Stone Age Crush
- Gouden aardappel levert een overvloed aan vitamine A en E
- Video:Kan er leven zijn zonder koolstof?

- Groenere gebouwen 3D printen met lokale bodem

- Hoogenergetisch vormgeheugenpolymeer kan op een dag robots helpen hun spieren te buigen
- Enantioselectieve synthese van indoolderivaten
- Colloïdale gels, alomtegenwoordig in alledaagse producten, hun geheimen prijsgeven
 Bewijs toont aan dat algoritmen voor risicobeoordeling vooringenomenheid vertonen ten opzichte van de Spaanse bevolking
Bewijs toont aan dat algoritmen voor risicobeoordeling vooringenomenheid vertonen ten opzichte van de Spaanse bevolking Nieuw onderzoek toont aan dat mannen meer bruikbare feedback krijgen dan vrouwen op de werkplek
Nieuw onderzoek toont aan dat mannen meer bruikbare feedback krijgen dan vrouwen op de werkplek Plantaardige eiwitten voor vleesliefhebbers
Plantaardige eiwitten voor vleesliefhebbers Nieuwe duurzame productiemethode kan kunststoffen en geneesmiddelen vooruit helpen
Nieuwe duurzame productiemethode kan kunststoffen en geneesmiddelen vooruit helpen Hoe beïnvloedt verwering en temperatuur rotsen?
Hoe beïnvloedt verwering en temperatuur rotsen?  Wat zijn aardgashydraten?
Wat zijn aardgashydraten?  Zelfs in de best-case emissiescenario's, zeespiegel kan nog stijgen tot 2300
Zelfs in de best-case emissiescenario's, zeespiegel kan nog stijgen tot 2300 Hoe de afstand van een stad te vinden vanaf de Equator
Hoe de afstand van een stad te vinden vanaf de Equator
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

