
Wetenschap
Enantioselectieve synthese van indoolderivaten
Krediet:Wiley
indolen, en daaruit afgeleide structuren, zijn een bestanddeel van veel natuurlijke stoffen, zoals het aminozuur tryptofaan. Een nieuwe katalytische reactie levert zeer selectief en met de gewenste ruimtelijke structuur cyclopenta[b]indolen op - raamwerken gemaakt van drie ringen die aan de randen zijn verbonden. Zoals een onderzoeksteam rapporteert in het tijdschrift Angewandte Chemie , de snelheden van de verschillende stappen van de reactie spelen een cruciale rol.
Indoolderivaten zijn wijdverbreid in de natuur; ze maken deel uit van serotonine en melatonine, evenals veel alkaloïden, waarvan sommige als medicijn worden gebruikt, bijvoorbeeld, als behandelingen voor de ziekte van Parkinson. Indool is een aromatische zesledige ring die langs één rand is gefuseerd met een vijfledige ring. De vijfledige ring heeft een dubbele binding en een stikstofatoom. Het basisframe van indool kan worden uitgerust met een verscheidenheid aan zijgroepen of worden gebonden aan extra ringen. Indool en vele indolderivaten kunnen worden gemaakt door een indoolsynthesereactie ontwikkeld door en genoemd naar Emil Fischer (door zuur ondersteunde condensatie van ketonen met fenylhydrazinen).
De belangrijkste klasse van indoolderivaten zijn cyclopentaan[b]indolen - moleculen met een raamwerk gemaakt van één indooleenheid en een extra vijfledige ring. Deze vijfledige ring kan een chiraal koolstofcentrum bevatten, dat is een ringkoolstof die twee extra zijgroepen heeft, en het kan op twee manieren worden gerangschikt die spiegelbeelden van elkaar zijn. Slechts één van de twee enantiomeren, of spiegelbeelden, wordt gevonden in de natuur. Echter, de klassieke Fischer-indoolsynthese produceert een mix van beide enantiomeren.
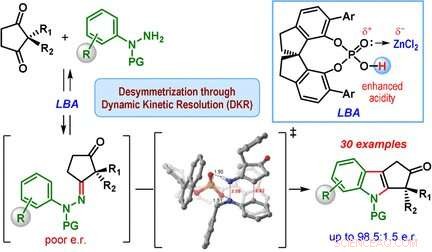
Een team onder leiding van Santanu Mukherjee en Garima Jindal van het Indian Institute of Science, Bangalore (India) heeft nu een katalytische versie van de Fischer-indoolsynthese ontwikkeld die voornamelijk een van de enantiomeren produceert (d.w.z. de reactie is enantioselectief). De uitgangsmaterialen zijn een klasse van diketonen (2, 2-digesubstitueerd cyclopentaan-1, 3-dionen) en fenylhydrazinederivaten uitgerust met speciale beschermende groepen. Het geheim van hun succes is een speciale katalysator:een chirale, cyclisch fosforzuur. De reactie wordt uitgevoerd in aanwezigheid van zinkchloride als co-katalysator en een zure kationenuitwisselingshars, die de ammoniak opvangt die zich als bijproduct vormt.
Het hart van het reactiemechanisme wordt een dynamische kinetische resolutie genoemd. Tijdens de reactie, een chiraal hydrazon wordt eerst gevormd als tussenproduct in beide enantiomere vormen. Deze stap is omkeerbaar, zodat beide enantiomere hydrazonen in de loop van de reactie in elkaar kunnen veranderen. De reactie van de hydrazonen om de indoolderivaten te maken is de eigenlijke katalytische reactie. Deze reactie is veel sneller voor een van de hydrazon-enantiomeren in vergelijking met de andere omdat de ene vorm een gunstigere geometrie heeft bij binding aan de chirale katalysator. Het andere hydrazon-enantiomeer reageert zeer langzaam en leidt tot slechts een kleine hoeveelheid van het indoolproduct. In plaats daarvan, het traag reagerende hydrazon-enantiomeer wordt omgezet in het snel reagerende hydrazon-enantiomeer, waardoor het evenwicht uiteindelijk verschuift naar het product cyclopentaan[b]indool.
Deze methode maakte het voor het team mogelijk om veel verschillende indoolderivaten te produceren met matige opbrengsten, maar met een goede tot uitstekende enantiomere selectiviteit.
 Marine Sri Lanka dicht brandstoflek op door brand getroffen tanker
Marine Sri Lanka dicht brandstoflek op door brand getroffen tanker De geschiedenis van de mensheid reconstrueren met behulp van fecale sterolen
De geschiedenis van de mensheid reconstrueren met behulp van fecale sterolen Onderzoekers vinden de uitstoot van nieuwe voertuigen bedrieglijk schoon
Onderzoekers vinden de uitstoot van nieuwe voertuigen bedrieglijk schoon Een van 's werelds meest afgelegen onbewoonde eilanden is letterlijk bedekt met onze prullenbak
Een van 's werelds meest afgelegen onbewoonde eilanden is letterlijk bedekt met onze prullenbak  Klimaat van schuldgevoel:vliegen voor sommigen niet langer de hoofdweg
Klimaat van schuldgevoel:vliegen voor sommigen niet langer de hoofdweg
Hoofdlijnen
- Wetenschappers vinden ontbrekende aanwijzing over hoe hiv cellen hackt om zichzelf te verspreiden
- Wanneer is lachen een medisch symptoom?
- Waarom zijn cellen belangrijk voor levende organismen?
- Het gebruik van kwallenbloei als oplossing voor het maken van nieuwe producten
- Monstervissen van de diepte
- Video:De aanval van invasieve soorten overleven
- Canadese kariboes, habitat blijft afnemen:rapport
- Genetische ontdekking nog een hulpmiddel in de strijd tegen tarweplagen
- Specialiteiten van de rechterkant van de hersenen
 Wat is industriële smog?
Wat is industriële smog?  NASA-wetenschappers onthullen details van het ijzige, verwarmde geologische verleden van Groenland
NASA-wetenschappers onthullen details van het ijzige, verwarmde geologische verleden van Groenland geen boerderijen, geen voedsel
geen boerderijen, geen voedsel NASA ziet Atlantische subtropische storm Melissa vormen voor de kust van New England
NASA ziet Atlantische subtropische storm Melissa vormen voor de kust van New England Onthulling van sterrenstelsels bij kosmische dageraad die zich achter het stof verschuilden
Onthulling van sterrenstelsels bij kosmische dageraad die zich achter het stof verschuilden Verzegeld, ondertekend en afgeleverd
Verzegeld, ondertekend en afgeleverd Wie is wie op de eerste bemande vlucht van Blue Origins?
Wie is wie op de eerste bemande vlucht van Blue Origins? Batavia's mysteries ontvouwen zich met ontdekking massagraf
Batavia's mysteries ontvouwen zich met ontdekking massagraf
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com






