
Wetenschap
Wetenschappers van Jefferson ontdekken nieuwe aanwijzingen over hoe cruciale moleculaire poortwachters werken
In een drietal artikelen gepubliceerd in het tijdschrift Nature Communications beschreven de onderzoekers de functie van een molecuul bekend als RAPTOR, dat de reactie van een cel op insuline orkestreert. Mutaties in RAPTOR resulteren in insulineresistentie en diabetes type 2.
"RAPTOR is de poortwachter die ervoor zorgt dat voedingsstoffen een cel binnendringen", zegt senior auteur Lewis C. Cantley, Ph.D., Meyer-directeur van het Sandra and Edward Meyer Cancer Center in Jefferson en een onderzoeker van het Howard Hughes Medical Institute. "Zonder RAPTOR kan het lichaam de glucose niet goed reguleren en ontstaat diabetes type 2. Het begrijpen van de rol van RAPTOR is van cruciaal belang voor de behandeling van insulineresistentie en diabetes type 2."
RAPTOR (regulatory Associated Protein of mTOR) controleert een essentieel cellulair proces dat eiwitsynthese wordt genoemd. Bij mensen met diabetes en obesitas gaat de RAPTOR-cellulaire route in overdrive, wat leidt tot overproductie van eiwitten die abnormale cel- en weefselgroei aandrijven.
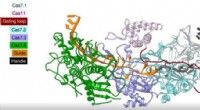
De artikelen beschrijven de atomaire structuur en interacties van RAPTOR terwijl het overschakelt van een uit- naar een aan-status, zoals het omdraaien van een schakelaar om een licht aan te doen, wanneer het wordt geactiveerd door insuline.
De onderzoekers bepaalden de structuur van de twee functioneel gescheiden domeinen van RAPTOR en ontdekten hoe ze interageren met andere eiwitten om deze moleculaire schakelaar te controleren. Dit mechanisme van allosterische regulatie vertegenwoordigt een algemeen concept dat op andere systemen zou kunnen worden toegepast.
"Allosterische regulatie is de manier waarop schakelaars worden omgedraaid; het is hoe RAPTOR aan en uit gaat", zegt eerste auteur Michael Hall, Ph.D., onderzoeksassistent-professor in de biochemie en moleculaire biologie aan de Thomas Jefferson University. "Als we erachter komen hoe RAPTOR de schakelaar reguleert, kunnen we leren hoe we deze met therapeutische middelen kunnen controleren."
"Bij diabetes komt de moleculaire schakelaar vast te zitten in de 'aan'-positie", vervolgde Hall. "Een potentiële therapeutische strategie zou kunnen zijn om de schakelaar in de 'uit'-positie te forceren, waardoor de ziekteprogressie wordt gestopt."
Andere auteurs zijn onder meer:Yanqin Zhao, Ph.D., Yi Zheng, M.D., Ph.D., en Jing Chen, Ph.D., allemaal van de Thomas Jefferson University.
Ondersteuning voor dit onderzoek werd gedeeltelijk verleend door het National Institute of Health (R01DK112064 en R01DK099545) en het Howard Hughes Medical Institute.
Artikelreferenties
Structuur en mechanisme van de TOR-kinasedomeinen in complex met het raptor WD40-domein. doi:10.1038/s41467-019-11372-1.
Moleculaire basis voor auto-inhibitie van menselijke roofvogel. doi:10.1038/s41467-019-11369-6.
Structuur en mechanisme van het RAPTOR ZnF-domein in menselijk mTORC1. doi:10.1038/s41467-019-11368-7.
 Wetenschappers lossen de gouden puzzel van calaveriet op
Wetenschappers lossen de gouden puzzel van calaveriet op Wetenschappers vinden zelfherstellende katalysator voor mogelijk grootschalig gebruik bij waterstofproductie
Wetenschappers vinden zelfherstellende katalysator voor mogelijk grootschalig gebruik bij waterstofproductie Cysteïnesynthese was een belangrijke stap in het ontstaan van leven:studie
Cysteïnesynthese was een belangrijke stap in het ontstaan van leven:studie Begrijpen hoe zwitterionische polymeren kunnen leiden tot veiligere medicijnen en ziektepreventie
Begrijpen hoe zwitterionische polymeren kunnen leiden tot veiligere medicijnen en ziektepreventie  Wetenschappers ontwikkelen een nieuw apparaat om geavanceerde kristallijne materialen te screenen
Wetenschappers ontwikkelen een nieuw apparaat om geavanceerde kristallijne materialen te screenen
 Onderzoekers ontdekken een over het hoofd gezien proces dat het koolstofverwijderingspotentieel van mangroven verbetert
Onderzoekers ontdekken een over het hoofd gezien proces dat het koolstofverwijderingspotentieel van mangroven verbetert Weerbaarheid tegen klimaatverandering kan op de lange termijn biljoenen besparen, maar nu miljarden vinden om ervoor te betalen is het moeilijkste deel
Weerbaarheid tegen klimaatverandering kan op de lange termijn biljoenen besparen, maar nu miljarden vinden om ervoor te betalen is het moeilijkste deel Zonlicht breekt polystyreen sneller af dan verwacht
Zonlicht breekt polystyreen sneller af dan verwacht Overleven op lange afstand:effecten van opslagtijd en milieublootstelling op bodembeestjes
Overleven op lange afstand:effecten van opslagtijd en milieublootstelling op bodembeestjes Geowetenschappers ontdekken dat Ancestral Puebloans overleefden van het smelten van ijs in lavabuizen in New Mexico
Geowetenschappers ontdekken dat Ancestral Puebloans overleefden van het smelten van ijs in lavabuizen in New Mexico
Hoofdlijnen
- Klimaatverandering die de migratiepatronen van gierende kraanvogels beïnvloedt, studie vondsten
- Jouw ochtendkoffie kan meer dan een half miljoen jaar oud zijn
- Het team vindt direct bewijs van rondtrekkende broedvogelsoorten aan de oostkust
- Noemen olifanten 'mensen!'?
- Geen hondenleven voor oudere dieren in Singapore Zoo
- Uit onderzoek blijkt hoe lichaamscellen in een weefsel bewegen
- Hoe celconcentratie te berekenen
- Nieuwe inzichten over hoe de vogelgriep de soortbarrière overschrijdt
- Avocado's zijn 'slecht' en veganisten belachelijk:hoe we het eten van te veel vlees rechtvaardigen
- Duurzaamheid van visserij gekoppeld aan genderrollen onder handelaren

- Europese topkoks schrappen elektrisch pulsvissen van het menu

- Microscopie onthult mechanisme achter nieuwe CRISPR-tool
- Tsunami onthult menselijke geluidsoverlast in Hawaiiaanse wateren
- Tonnen leven diep in het aardoppervlak gevonden
 Wetenschappers vinden bewijs voor alternatieve theorieën over hoe het leven is ontstaan
Wetenschappers vinden bewijs voor alternatieve theorieën over hoe het leven is ontstaan  Quantum dots schijnen helder om wetenschappers te helpen ontstekingscellen in vet te zien
Quantum dots schijnen helder om wetenschappers te helpen ontstekingscellen in vet te zien Deep Space Antenne 1
Deep Space Antenne 1 Tesla sluit winkels om kosten te verlagen voor $ 35 000 Model 3
Tesla sluit winkels om kosten te verlagen voor $ 35 000 Model 3 Ryanairs Laudamotion verdubbelt vloot volgend jaar
Ryanairs Laudamotion verdubbelt vloot volgend jaar Wie heeft de term virtual reality populair gemaakt?
Wie heeft de term virtual reality populair gemaakt?  Wat sprinkhanen eten
Wat sprinkhanen eten Onderzoek onthult hoe groene ruimte gewelddadige criminaliteit kan verminderen
Onderzoek onthult hoe groene ruimte gewelddadige criminaliteit kan verminderen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

