
Wetenschap
Beheersing van polyatomaire ionenladingen:een praktische gids

In de scheikunde kunnen ionen afzonderlijke atomen zijn of clusters van atomen die samenwerken, ook wel polyatomaire ionen genoemd. Elk ion heeft een afzonderlijke lading die wordt bepaald door de valentie-elektronen van de samenstellende atomen. Hoewel er talloze methoden bestaan om deze kosten te berekenen, is memoriseren de meest betrouwbare aanpak, ondersteund door systematische technieken en geheugensteuntjes.
Bereken de lading met behulp van oxidatiegetallen
- Wijs oxidatiegetallen toe voor elk atoom in het ion. In hydroxide (OH⁻) is zuurstof bijvoorbeeld –2 en waterstof +1.
- Tel de oxidatiegetallen op van alle atomen. In OH⁻, –2 + (+1) =–1.
- Schrijf de aanklacht als superscript rechts van de formule. Een enkele eenheid wordt geschreven als – of +, bijvoorbeeld OH⁻.
Bepaal de lading door een Lewis-structuur te tekenen
- Teken Lewis-punten voor elk atoom. Voor ammonium (NH₄⁺) wordt stikstof weergegeven met vijf stippen en elke waterstof met één stip.
- Vorm covalente bindingen tussen de atomen. De vier waterstofatomen binden zich aan stikstof, met behulp van de valentie-elektronen van stikstof.
- Gedeelde paren omzetten in lijnen om covalente bindingen aan te duiden.
- Tel de resterende elektronen na het bereiken van de octet-/duetregels. Overtollige elektronen duiden op een negatieve lading; een tekort duidt op een positieve lading. Ammonium heeft één extra elektron, waardoor het een +1 lading krijgt.
Mnemonische apparaten voor snelle herinnering
- Gebruik een gedenkwaardige zin waarin het achtervoegsel van het ion is verwerkt. 'Nick the Camel at a Clam for Supper in Phoenix' doet bijvoorbeeld denken aan de serie '-ate'.
- Identificeer het hoofdatoom uit het sleutelwoord van de zin:“Nick” → Stikstof voor nitraat.
- Tel de medeklinkers in het woord om het aantal zuurstofatomen te bepalen. “Nick” heeft drie medeklinkers → 3 O-atomen.
- Tel de klinkers om de negatieve lading te vinden. “Nick” heeft één klinker → –1 lading.
Essentiële hulpmiddelen
- Periodiek systeem (digitaal of gedrukt)
- Potlood en papier voor snel schetsen
TL;DR
Oxidatiegetallen zijn betrouwbaar voor eenvoudige ionen zoals NH₄⁺, OH⁻, CN⁻ en CH₃COO⁻. Voor ionen die elementen bevatten met variabele oxidatietoestanden (bijvoorbeeld S, N), gebruikt u geheugensteuntjes of geheugensteuntjes om de ladingen te bepalen.
Hoofdlijnen
- Wetenschappers geven 's werelds eerste DNA-kaart van een bedreigde Australische muis vrij, en het zal helpen om deze te redden
- Nieuwe krachtdetectiemethode onthult hoe cellen weefselstijfheid waarnemen
- Onderzoek toont aan hoe vrouwelijke immuuncellen hun tweede X-chromosoom uitgeschakeld houden
- Waar ontstaan sporen?
- Hoe noem je een organisme dat zowel autotrofe als heterotrof is?
- Uit een nieuwe methode voor het modelleren van vrij rondlopende dierpopulaties blijkt dat de aantallen makaken kleiner zijn dan verwacht
- Alleen structuren betrokken bij mitose van dierlijke cellen?
- Scheve vissen laten zien dat symmetrie slechts oppervlakkig is
- Welke cellen van het lichaam scheiden interferonen uit?
- Mildere ammoniaksynthesemethode zou het milieu moeten helpen

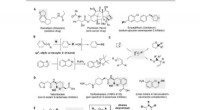
- Invoeging van boor in alkyletherbindingen via tandemkatalyse van zink/nikkel
- Robots geactiveerd door water kunnen de volgende grens zijn

- Nieuw synthetisch protocol om een 3D poreus organisch netwerk te vormen

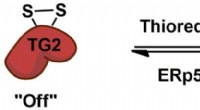
- Op zoek naar een uit-schakelaar voor coeliakie
 De religieuze strijd over anticonceptie en de onaangename motivatie die het aanwakkerde
De religieuze strijd over anticonceptie en de onaangename motivatie die het aanwakkerde Hoe een eenvoudige 1-minuten timer te maken
Hoe een eenvoudige 1-minuten timer te maken  Mysterie van amorf perovskiet opgelost
Mysterie van amorf perovskiet opgelost Hoe verschillen de binnen- en buitenplaneten in de atmosfeer?
Hoe verschillen de binnen- en buitenplaneten in de atmosfeer?  Wat voor soort energie is kerosine?
Wat voor soort energie is kerosine?  Astronomen presenteren een concept voor de volgende NASA-vlaggenschipmissie
Astronomen presenteren een concept voor de volgende NASA-vlaggenschipmissie Wanneer een veer wordt gecomprimeerd, brengt het elastische energie over naar de omgeving?
Wanneer een veer wordt gecomprimeerd, brengt het elastische energie over naar de omgeving?  Wat zou er gebeuren als de aarde echt plat was?
Wat zou er gebeuren als de aarde echt plat was?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com


