
Wetenschap
Berekening van het totale aantal elektronen van elk molecuul of ion
Door bijdragende schrijver • Bijgewerkt op 30 augustus 2022
Atomen binden zich door elektronen te delen, en het kennen van het aantal elektronen van een verbinding is de eerste stap om de chemie ervan te begrijpen. Met behulp van het periodiek systeem en de basisrekenkunde kun je bepalen hoeveel elektronen er in een molecuul of ion aanwezig zijn.
Stap 1:Identificeer de elementen en hun hoeveelheden
Schrijf elk element in de chemische formule op en noteer hoeveel atomen van elk voorkomen. Bijvoorbeeld:
- KNO3 – Kalium (1 atoom), Stikstof (1 atoom), Zuurstof (3 atomen)
- SO4 2‑ – Zwavel (1 atoom), Zuurstof (4 atomen)
Stap 2:Atoomnummers ophalen
Raadpleeg een betrouwbaar periodiek systeem (bijvoorbeeld het PubChem periodiek systeem ) om het atoomnummer van elk element te vinden:het gehele getal direct boven het symbool. In de bovenstaande voorbeelden:K=19, N=7, O=8, S=16.
Stap 3:Bereken de elektronensom
Vermenigvuldig het atoomnummer van elk element met het aantal atomen en tel vervolgens de producten op:
- KNO3 :(19×1)+(7×1)+(8×3)=50 elektronen
- SO4 2‑ :(16×1)+(8×4)=48 elektronen (vóór aanpassing van de lading)
Stap 4:Aanpassen voor ionische lading
Voor ionen wijzigt u het totaal uit stap 3 met de ladingswaarde:tel de lading voor negatieve ionen op, trek deze af voor positieve ionen en laat deze ongewijzigd voor neutrale soorten. Het sulfaation heeft een lading van 2, dus 48+2=50 elektronen.
Hulpmiddelen die je nodig hebt
- Wetenschappelijke rekenmachine (of spreadsheet)
- Toegang tot een actueel periodiek systeem
Referenties
- Whitten, KW; Davis, RE; Peck, L.; Stanley, G.G. Chemie , 2009.
 Een stap in de richting van een gevoelige en snelle glutendetectie
Een stap in de richting van een gevoelige en snelle glutendetectie Wat zijn twee elementen met eigenschappen die vergelijkbaar zijn met chloor?
Wat zijn twee elementen met eigenschappen die vergelijkbaar zijn met chloor?  Hoe beïnvloedt pH-niveau enzymactiviteit?
Hoe beïnvloedt pH-niveau enzymactiviteit?  Oplossing voor fout in synchrotron-onderzoek kan de resultaten verbeteren
Oplossing voor fout in synchrotron-onderzoek kan de resultaten verbeteren Door fotopolymerisatie geactiveerde moleculaire beweging voor flexibele weergave van vloeibare kristallen
Door fotopolymerisatie geactiveerde moleculaire beweging voor flexibele weergave van vloeibare kristallen
 Waarom zou je planten naar Mars brengen?
Waarom zou je planten naar Mars brengen?  Hoe zal klimaatverandering de kustgemeenschappen beïnvloeden? Een studie over de barrière-eilanden van Virginia
Hoe zal klimaatverandering de kustgemeenschappen beïnvloeden? Een studie over de barrière-eilanden van Virginia Onderzoekers onderzoeken verband tussen tropische gletsjers, water voorraad
Onderzoekers onderzoeken verband tussen tropische gletsjers, water voorraad Hoe bossen koolstof kunnen terugdringen, ecosystemen kunnen herstellen en banen kunnen creëren
Hoe bossen koolstof kunnen terugdringen, ecosystemen kunnen herstellen en banen kunnen creëren  Geüpgraded waterrisicofilter kan de reactie van bedrijven op waterrisico's helpen transformeren
Geüpgraded waterrisicofilter kan de reactie van bedrijven op waterrisico's helpen transformeren
Hoofdlijnen
- Het veredelen van zeer productieve maïs heeft zijn aanpassingsvermogen verminderd
- De evolutionaire geschiedenis van een soort kan worden weergegeven in een?
- Wat is het genetische materiaal dat van generatie op generatie is doorgegeven?
- Wat is een bevolkingswetenschap?
- Wat is een cytobioloog?
- Hoe demonstreert de celtheorie de definitie van deze theorie?
- Wat is het proces waarin een eukaryotische cel verdeelt?
- Wat is genetisch materiaal welke organismen van hun ouders erven?
- Leg uit waarom eiwitten als polymeren worden beschouwd, maar lipiden niet?
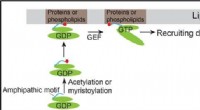
- Onderzoekers ontdekken een nieuw mechanisme voor het werven van ARF-familie-eiwitten
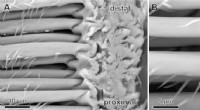
- Verrassende ontdekking van spinnenhaar kan leiden tot sterkere lijmen
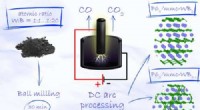
- Superharde materiaalsynthese goedkoper gemaakt
- Bio-sensing contactlens kan op een dag bloedglucose meten, andere lichaamsfuncties

- Nieuwe buigbare smartphonetechnologie kan monitoring gebruiken om levens van patiënten te redden

 Wie heeft de controle? Onderzoeker onderzoekt waarom het zo moeilijk is om de verbinding met sociale media te verbreken
Wie heeft de controle? Onderzoeker onderzoekt waarom het zo moeilijk is om de verbinding met sociale media te verbreken Wat zijn de uitgangsmaterialen van cellulaire ademhaling?
Wat zijn de uitgangsmaterialen van cellulaire ademhaling?  Hoe creëren erosie en verwering de Cave -systemen van Kentucky?
Hoe creëren erosie en verwering de Cave -systemen van Kentucky?  Hoe de man en vrouw te vertellen Zebravis Apart
Hoe de man en vrouw te vertellen Zebravis Apart Wat gebeurt er met soorten die poging dezelfde niche bezetten?
Wat gebeurt er met soorten die poging dezelfde niche bezetten?  Hoe u een Bushnell-reflectortelescoop installeert en gebruikt voor heldere nachtelijke hemelbeelden
Hoe u een Bushnell-reflectortelescoop installeert en gebruikt voor heldere nachtelijke hemelbeelden  Hoe worden de mannelijke en vrouwelijke gameten genaamd wat het gevolg is van hun fusie?
Hoe worden de mannelijke en vrouwelijke gameten genaamd wat het gevolg is van hun fusie?  Nieuwe studie werpt licht op de langzame terugtrekking van de manen uit de bevroren aarde
Nieuwe studie werpt licht op de langzame terugtrekking van de manen uit de bevroren aarde
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

