
Wetenschap
Hoe de lading van overgangsmetaalionen te bepalen
Door Marie-Luise Blue
Bijgewerkt op 30 augustus 2022
Afbeelding tegoed:Leonid Eremeychuk/iStock/GettyImages
De lading van een overgangsmetaalion reflecteert de elektronen die het tijdens een chemische reactie heeft afgegeven. Het bepalen van die lading vereist kennis van het element, de ladingen van de omringende atomen en de algehele moleculaire lading. Alle oxidatiegetallen zijn gehele getallen, en de som van de atomaire ladingen is gelijk aan de nettolading van de soort.
Oxidatietoestanden van overgangsmetalen
Wanneer een atoom elektronen verliest, noemen scheikundigen dit proces oxidatie. Voor overgangsmetalen kan de oxidatietoestand – en dus de ionische lading – variëren van +1 tot +7. Deze elementen bezitten gedeeltelijk gevulde d-orbitalen die het elektronenverlies gemakkelijker maken dan bij hoofdgroepelementen. Sommige oxidatietoestanden zijn inherent stabieler en komen daarom vaker voor. IJzer (Fe) kan bijvoorbeeld +2, +3, +4, +5 of +6 toestanden aannemen, maar +2 en +3 domineren in natuurlijke en industriële contexten. In chemische formules wordt de oxidatietoestand aangegeven door een Romeins cijfer tussen haakjes (bijvoorbeeld ijzer(II)oxide, FeO, waarbij Fe een lading van +2 heeft).
Neutrale verbindingen
In een neutrale verbinding is de totale lading nul. Als u de oxidatietoestand van de ligandatomen kent, kunt u de lading van het metaal bepalen. In MnCl₂ dragen de twee chloride-ionen bijvoorbeeld elk –1. De gecombineerde lading van –2 dwingt mangaan tot +2 om de neutraliteit te behouden.
Geladen complexen
Overgangsmetaalionen vormen vaak complexe ionen die positief of negatief geladen zijn. Neem het permanganaat-ion, MnO₄ ⁻:elke zuurstof heeft een oxidatietoestand van –2, wat een totaal van –8 oplevert uit vier zuurstofatomen. De totale lading van –1 betekent dat mangaan +7 moet zijn.
Oplosbaarheidsoverwegingen
De meeste neutrale, oplosbare overgangsmetaalzouten in water hebben oxidatietoestanden van +3 of lager. Hogere oxidatietoestanden slaan gewoonlijk neer of hydrolyseren om zuurstofhoudende complexen te vormen. Vanadium(V)-zouten hydrolyseren bijvoorbeeld en produceren het hexaaquavanadaat(IV)-ion, [V(OH)₆]⁺, of het aquavanadaat(V)-ion, [VO₄]⁻, afhankelijk van de omgeving.
 Nieuwe studie:Fracking veroorzaakt wereldwijde piek in methaan in de atmosfeer
Nieuwe studie:Fracking veroorzaakt wereldwijde piek in methaan in de atmosfeer De meeste aardverschuivingen in het westen van Oregon veroorzaakt door hevige regenval, geen grote aardbevingen
De meeste aardverschuivingen in het westen van Oregon veroorzaakt door hevige regenval, geen grote aardbevingen Een plant die reageert op aanraking, laat zien wat?
Een plant die reageert op aanraking, laat zien wat?  Reconstructie toont toegenomen trends in opwarming van de aarde sinds 1850
Reconstructie toont toegenomen trends in opwarming van de aarde sinds 1850 Wat is het belang van bomen in het menselijk leven?
Wat is het belang van bomen in het menselijk leven?
Hoofdlijnen
- Nieuw onderzoek laat zien hoe sommige kippen gestreepte veren kregen
- Wetenschappers leren hoe ze een wegversperring kunnen vermijden bij het herprogrammeren van cellen
- Korte biografie:definitie, doel en voorbeelden | [Uw merk/website]
- Welke van de volgende vergelijken cladistische taxonomen niet vergelijken bij het veronderstellen van evolutionaire relaties tussen organismen?
- Onthulling van natuurbeheerders:studie benadrukt de cruciale rol van aaseters in wetlands
- Hebben alle planten celwanden?
- Wiskundigen en biologen leggen uit waarom de darmen van gewervelde dieren zo voorspelbaar krom zijn
- Hoeveel ATP -moleculen worden gebruikt om één run van de Calvin -cyclus te voltooien en 1 glucosemolecuul te produceren?
- Q.State verschillende structurele modificatie in een cel die secretie betreft?
- Wetenschappers publiceren een compleet overzicht van sulfonimide-dendrimeren

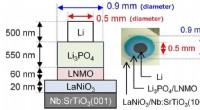
- De limieten van Li-ion-batterijen uitbreiden - elektroden voor volledig solid-state batterijen
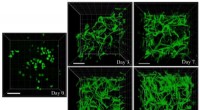
- Biopolymeren voor wondtherapie leveren stamcellen om de genezing te verbeteren
- Nieuwe batterij slokt kooldioxide op

- Uitwisbare inkt voor 3D-printen
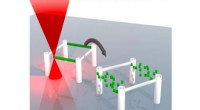
 Wat is een watermolecuul dat waterstofion verliest?
Wat is een watermolecuul dat waterstofion verliest?  Aardgas benutten om water uit de lucht te halen, kan twee grote problemen tegelijk oplossen
Aardgas benutten om water uit de lucht te halen, kan twee grote problemen tegelijk oplossen Wat is het energieprofiel van een chemische reactie, inclusief activering vrije verandering en overgangstoestand?
Wat is het energieprofiel van een chemische reactie, inclusief activering vrije verandering en overgangstoestand?  Hoe laat ging de maan vandaag onder?
Hoe laat ging de maan vandaag onder?  Moleculaire dispersie verbetert quasi-dubbellaagse organische zonnecellen
Moleculaire dispersie verbetert quasi-dubbellaagse organische zonnecellen Wat moet er gebeuren om een elektromagnetische golf te laten vormen?
Wat moet er gebeuren om een elektromagnetische golf te laten vormen?  Levensverwachting daalt voor volwassenen zonder bachelordiploma
Levensverwachting daalt voor volwassenen zonder bachelordiploma Het prototype van de niet-giftige zoutwaterbatterij kan in enkele seconden worden opgeladen
Het prototype van de niet-giftige zoutwaterbatterij kan in enkele seconden worden opgeladen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

