
Wetenschap
Chemische bindingen begrijpen:wat houdt moleculen bij elkaar?
* Covalente bindingen: Dit is het sterkste type binding en omvat het delen van elektronen tussen twee atomen. Covalente bindingen worden doorgaans aangetroffen in moleculen die zijn samengesteld uit niet-metalen, zoals water (H₂O) en methaan (CH₄).
* Ionische bindingen: Deze bindingen omvatten de overdracht van elektronen van het ene atoom naar het andere, wat resulteert in de vorming van ionen (atomen met een positieve of negatieve lading). Ionische bindingen worden doorgaans aangetroffen in verbindingen die zijn samengesteld uit een metaal en een niet-metaal, zoals natriumchloride (NaCl).
* Metaalverbindingen: Deze bindingen omvatten het delen van elektronen tussen een groot aantal atomen in een metaalrooster. Deze ‘zee’ van elektronen geeft metalen hun karakteristieke eigenschappen, zoals geleidbaarheid en maakbaarheid.
Naast deze drie primaire typen zijn er ook zwakkere interacties die intermoleculaire krachten worden genoemd die het gedrag van moleculen ten opzichte van elkaar beïnvloeden, maar ze houden de atomen niet bij elkaar binnen een molecuul.
Het is belangrijk op te merken dat veel moleculen een combinatie van deze bindingstypen hebben. Het bicarbonaatmolecuul (HCO₃⁻) heeft bijvoorbeeld covalente bindingen tussen de waterstof-, koolstof- en zuurstofatomen, en een ionische binding tussen het bicarbonaation en een ander ion.
 Metalen die minder reactief zijn dan alkali-metalen en alkalische aardrichting?
Metalen die minder reactief zijn dan alkali-metalen en alkalische aardrichting?  Chemici maken een sensor die nauwkeurig de speeksel-pH van mensen detecteert
Chemici maken een sensor die nauwkeurig de speeksel-pH van mensen detecteert Wat is een speciaal soort diffusie dat water ondergaat?
Wat is een speciaal soort diffusie dat water ondergaat?  Antibacteriële prodrug door zich te richten op intracellulaire metaboliet
Antibacteriële prodrug door zich te richten op intracellulaire metaboliet Hoeveel gram lidocaïne bevindt zich in 150 ml een oplossing van 2,5 m?
Hoeveel gram lidocaïne bevindt zich in 150 ml een oplossing van 2,5 m?
 Radar onthult smeltwater het hele jaar door leven onder Groenlands ijs
Radar onthult smeltwater het hele jaar door leven onder Groenlands ijs Voedsel verspillen kan veilig zijn, redelijke beslissing voor sommigen, studie zegt:
Voedsel verspillen kan veilig zijn, redelijke beslissing voor sommigen, studie zegt: Hoe te vertellen of een pauw mannelijk of vrouwelijk is
Hoe te vertellen of een pauw mannelijk of vrouwelijk is Hoe beschermen kreeftachtigen zichzelf?
Hoe beschermen kreeftachtigen zichzelf?  Door de mens veroorzaakte klimaatverandering achter de dodelijke hittegolf in de Sahel:studie
Door de mens veroorzaakte klimaatverandering achter de dodelijke hittegolf in de Sahel:studie
Hoofdlijnen
- Een nieuwe genetische bemonsteringstechniek voor kwelderoogstmuizen en andere kleine zoogdieren
- Wat is de drijvende kracht achter de menselijke evolutie?
- Een nieuwe kijk op hoe genen zich ontvouwen om hun expressie mogelijk te maken
- Wat hebben cellen de neiging om in een hypertone oplossing van zuiver water te worden geplaatst?
- Wat ervaren totaal blinde mensen visueel? Een complexe realiteit
- Wat doet Mitchochondria?
- Hoe worden alle reacties in het lichaam geroepen?
- Hoe een bacteriële virulentiefactor zijn eigen secretie bevordert
- 10 geweldige dingen die de hersenen van mensen hebben gedaan
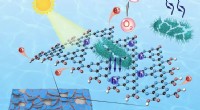
- Wetenschappers ontwikkelen metaalvrije fotokatalysator om pathogeenrijk water binnen enkele minuten te zuiveren
- Nucleair gaan op de maan en Mars

- Begrijpen wat Tennessee whisky uniek maakt

- Nieuwe katalysatormethode belooft beter gebruik van syngas, steenkool

- Nieuwe methode om uit forensisch bewijs teruggevonden zaadcellen te detecteren en te visualiseren
 Welke apparatuur is nodig voor hydro -elektrische energie?
Welke apparatuur is nodig voor hydro -elektrische energie?  Waarom zijn astronomen geïnteresseerd in het orbitale patroon van de aarde?
Waarom zijn astronomen geïnteresseerd in het orbitale patroon van de aarde?  Waar is een ribosoom van gemaakt?
Waar is een ribosoom van gemaakt?  AI-model om gecompliceerde grootschalige tropische instabiliteitsgolven in de Stille Oceaan te voorspellen
AI-model om gecompliceerde grootschalige tropische instabiliteitsgolven in de Stille Oceaan te voorspellen Wat is de klasse voor dieren?
Wat is de klasse voor dieren?  Hoe de afmetingen van een vierkant te vinden met het gebied
Hoe de afmetingen van een vierkant te vinden met het gebied  Economist publiceert onderzoek naar effectiviteit van verkeerscamera's
Economist publiceert onderzoek naar effectiviteit van verkeerscamera's Wat is het nut voor fylogenetische bomen?
Wat is het nut voor fylogenetische bomen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

