
Wetenschap
Boor-stikstofbinding:covalente binding uitgelegd
Dit is waarom:
* Elektronegativiteit: Borium heeft een elektronegativiteit van 2,04, terwijl stikstof een elektronegativiteit van 3,04 heeft. Het verschil in elektronegativiteit is aanzienlijk, wat aangeeft dat stikstof sterker elektronen aantrekt dan boor.
* Het delen van elektronen: In plaats van dat het ene atoom een elektron volledig van het andere overneemt, delen boor en stikstof elektronen om een stabiele binding te vormen. Dit delen van elektronen is het bepalende kenmerk van een covalente binding.
In het bijzonder vormen boor en stikstof vaak een gecoördineerde covalente binding , waarbij één atoom (in dit geval stikstof) beide elektronen levert voor het gedeelde paar.
Voorbeelden:
* Borazine (B3N3H6): Deze verbinding wordt vaak "anorganisch benzeen" genoemd vanwege de structurele gelijkenis met benzeen. Het bevat afwisselend boor- en stikstofatomen verbonden door covalente bindingen.
* Boornitride (BN): Dit materiaal bestaat in verschillende vormen, waaronder hexagonaal boornitride (vergelijkbaar met grafiet) en kubisch boornitride (vergelijkbaar met diamant). De bindingen tussen boor en stikstof in deze structuren zijn ook covalent.
 Het mobiliseren van wereldwijd kapitaal in de nasleep van een ramp is essentieel voor economisch herstel
Het mobiliseren van wereldwijd kapitaal in de nasleep van een ramp is essentieel voor economisch herstel Welke planten groeien in een ravijn?
Welke planten groeien in een ravijn?  Klimaatverandering bedreigt afbrokkelend erfgoed van Afghanistan
Klimaatverandering bedreigt afbrokkelend erfgoed van Afghanistan Interactie tussen klimatologische factoren en tijdschema beïnvloeden de beoordeling van extreme droogte in China
Interactie tussen klimatologische factoren en tijdschema beïnvloeden de beoordeling van extreme droogte in China Hoe beheer je de biodiversiteit?
Hoe beheer je de biodiversiteit?
Hoofdlijnen
- Is Cynobacteria het eerste levende organisme op aarde?
- Hoe dodelijke parasieten ervoor kiezen mannelijk te zijn:Onderzoekers onthullen genexpressie gedurende de levenscyclus van Cryptosporidium
- Hoe kunt u vrij aminozuur isoleren van eiwitten?
- Voedingsvormen van bacteriën
- Nieuwe mitochondriaal afgeleide peptiden laten zien wat ze kunnen doen
- Wat gebeurt er als een organisme stopt met evolueren?
- Wat voor soort vlekken worden gebruikt om cellen te planten en dieren?
- Wat is een eigenschap die alle organismen hebben?
- Wat de wetenschappelijke naam voor sekscel?
- Kunstmatig synaptisch apparaat simuleert de functie van het menselijk brein
- 3D-microstructuren in realtime vastleggen

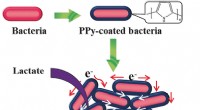
- Geleidende schaal voor bacteriën
- Wetenschappers ontdekken mogelijke methode om de bacteriën die tuberculose veroorzaken uit te hongeren
- Wetenschappers melden voor het eerst zware ionenoverdracht in geladen vdW-cluster

 Wat is de functie en het gebruik van stikstof in uw lichaam?
Wat is de functie en het gebruik van stikstof in uw lichaam?  Op welke manieren lijkt de bloem vergelijkbaar met reproductieve organen van dieren?
Op welke manieren lijkt de bloem vergelijkbaar met reproductieve organen van dieren?  Wat vertellen wetenschappers ons over het tijdperk van het universum en de planeet?
Wat vertellen wetenschappers ons over het tijdperk van het universum en de planeet?  Waarom stijgen champagnebellen in een recht traject?
Waarom stijgen champagnebellen in een recht traject?  Door de klimaatverandering verschuiven de zones waar planten groeien. Dit is wat dat voor uw tuin kan betekenen
Door de klimaatverandering verschuiven de zones waar planten groeien. Dit is wat dat voor uw tuin kan betekenen  Wetenschappers speuren het verleden af op zoek naar toekomstige klimaataanwijzingen
Wetenschappers speuren het verleden af op zoek naar toekomstige klimaataanwijzingen Hoe helpt Mimicry de kans op het overleven van een organismen te vergroten?
Hoe helpt Mimicry de kans op het overleven van een organismen te vergroten?  Maaltijd delen voor een langer leven? Insecten kunnen het geheim bevatten
Maaltijd delen voor een langer leven? Insecten kunnen het geheim bevatten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

