
Wetenschap
Wat betekent het om een sterke of zwakke zuurbase te zijn?
De sterkte van een zuur wordt gemeten aan de hand van de zuurdissociatieconstante (Ka). De Ka is de evenwichtsconstante voor de dissociatie van een zuur in water. Hoe hoger de Ka, hoe sterker het zuur.
De sterkte van een basis wordt gemeten aan de hand van de basisdissociatieconstante (Kb). De Kb is de evenwichtsconstante voor de dissociatie van een base in water. Hoe hoger de Kb, hoe sterker de basis.
Sterke zuren en basen hebben Ka- en Kb-waarden die veel groter zijn dan 1, terwijl zwakke zuren en basen Ka- en Kb-waarden hebben die veel kleiner zijn dan 1.
Hier is een tabel met een samenvatting van de eigenschappen van sterke en zwakke zuren en basen:
| Eigendom | Sterk zuur | Zwak zuur | Sterke basis | Zwakke basis |
|---|---|---|---|---|
| Dissociatie | Dissocieert volledig in water | Dissocieert gedeeltelijk in water | Dissocieert volledig in water | Dissocieert gedeeltelijk in water |
| Ka | Ka>> 1 | Ka <<1 | KB>> 1 | KB <<1 |
| pH | pH <7 | pH> 7 | pH> 7 | pH <7 |
| Voorbeelden | HCl, H2SO4, HNO3 | CH3COOH, H2CO3, HF | NaOH, KOH, Ca(OH)2 | NH3, CH3NH2, pyridine |
Sterke zuren en basen zijn doorgaans bijtend en kunnen ernstige brandwonden veroorzaken. Zwakke zuren en basen zijn over het algemeen minder schadelijk, maar kunnen toch irritatie veroorzaken.
 Zomerse dode zones in Chesapeake Bay vallen eerder uiteen
Zomerse dode zones in Chesapeake Bay vallen eerder uiteen Het verwijderen van grasgras bespaart water. Maar zal het de stedelijke hitte doen toenemen?
Het verwijderen van grasgras bespaart water. Maar zal het de stedelijke hitte doen toenemen?  Blootstelling aan Tsjernobyl verandert de darmbacteriën van wilde dieren
Blootstelling aan Tsjernobyl verandert de darmbacteriën van wilde dieren Onkruidbedekking in olijfboomgaarden vergroot de capaciteit van ecosystemen als CO2-put
Onkruidbedekking in olijfboomgaarden vergroot de capaciteit van ecosystemen als CO2-put Wetenschappers bestuderen kwikvergiftiging in Peruaans bos op reisroute paus
Wetenschappers bestuderen kwikvergiftiging in Peruaans bos op reisroute paus
Hoofdlijnen
- Experimenten verklaren waarom bijna alle meercellige organismen hun leven als een enkele cel beginnen
- Wat zijn de belangrijkste functies van Cilia & Flagella?
- Klasactiviteiten op het ademhalingssysteem
- Nieuwe inzichten in de belangrijkste oorzaak van een miskraam, geboorteafwijkingen ontdekt
- Hoe herhaalbaar is de evolutionaire geschiedenis?
- Onderzoekers ontdekken hoe wombats kakblokjes uitscheiden
- Wat jager-verzamelaars ons kunnen vertellen over fundamentele menselijke sociale netwerken
- Wat zijn de functies van natriumperchloraat bij de isolatie van genomisch DNA uit menselijk bloed?
- Welke structuur van elke soort lichaamscel is geschikt voor wat?
- Hoe een kristallijne spons watermoleculen afstoot

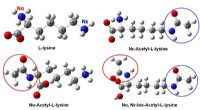
- Raman- en infraroodspectroscopie helpen bij het identificeren van verschillende geacetyleerde lysines
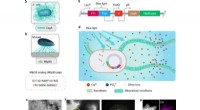
- Lichtgevoelige E. coli functionele biofilms als steigers voor hydroxyapatietmineralisatie
- Nieuwe inzichten kunnen de ontwikkeling van natuurlijke en veiligere fungiciden bevorderen

- Sous-vide kookmethode maakt rundvleeseiwit beter verteerbaar

 Onderzoek:Technologie verandert de manier waarop bedrijven zaken doen
Onderzoek:Technologie verandert de manier waarop bedrijven zaken doen  Science Project on Why Bones krijgt Rubbery in Azijn
Science Project on Why Bones krijgt Rubbery in Azijn  Nieuw mysterie ontdekt over actieve asteroïde Phaethon
Nieuw mysterie ontdekt over actieve asteroïde Phaethon NASA en SpaceX gaan geschiedenis schrijven met bemande ruimtelancering
NASA en SpaceX gaan geschiedenis schrijven met bemande ruimtelancering  Koperionen kunnen een sleutelrol spelen wanneer het vouwen van peptiden fout gaat
Koperionen kunnen een sleutelrol spelen wanneer het vouwen van peptiden fout gaat Wetenschappers ontdekken genomische voorouders van Noord-Afrikanen uit het stenen tijdperk uit Marokko
Wetenschappers ontdekken genomische voorouders van Noord-Afrikanen uit het stenen tijdperk uit Marokko Onderzoek verklaart waarom seksuele opwinding mannen kan afschrikken van langdurige relaties
Onderzoek verklaart waarom seksuele opwinding mannen kan afschrikken van langdurige relaties  Hoe veilig is uw eigen feed nadat CyberJihad de Twitter van het Amerikaanse Centrale Commando heeft gehackt?
Hoe veilig is uw eigen feed nadat CyberJihad de Twitter van het Amerikaanse Centrale Commando heeft gehackt?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

