
Wetenschap
Hoe bereid je een 0,25 molaire oplossing van HCl?
De formule voor het berekenen van de hoeveelheid opgeloste stof die nodig is om een oplossing met een specifieke concentratie te bereiden is:
```
Mol opgeloste stof =Molariteit (M) × Volume oplossing (L)
```
In dit geval willen we 1 liter van een 0,25 M HCl-oplossing bereiden. Het aantal benodigde mol HCl is dus:
```
Mol HCl =0,25 M × 1 L =0,25 mol
```
Stap 2:Bepaal de benodigde massa HCl.
De molaire massa van HCl is 36,46 g/mol. De massa HCl die nodig is om 0,25 mol oplossing te bereiden is dus:
```
Massa HCl =Mol HCl × Molaire massa HCl
=0,25 mol × 36,46 g/mol =9,115 g
```
Stap 3:Bereid de oplossing voor.
- Voeg 9,115 g HCl toe aan een maatkolf van 1 liter.
- Voeg ongeveer 500 ml gedeïoniseerd water toe aan de kolf.
- Draai de kolf voorzichtig rond om de HCl op te lossen.
- Voeg meer gedeïoniseerd water toe tot het volume de 1L-markering bereikt.
- Meng de oplossing grondig.
De resulterende oplossing zal 0,25 M HCl zijn.
 Wat gebeurt er als natriumsulfaat met water wordt gemengd?
Wat gebeurt er als natriumsulfaat met water wordt gemengd?  Kan een kopje zout en water beide een oplossing zijn?
Kan een kopje zout en water beide een oplossing zijn?  Onderzoekers ontwikkelen nieuwe technologie die de commercialisering van brandstofcelvoertuigen kan versnellen
Onderzoekers ontwikkelen nieuwe technologie die de commercialisering van brandstofcelvoertuigen kan versnellen Waarom is vloeibare ammoniak een niet-elektrolyt, maar waterig een elektrolyt?
Waarom is vloeibare ammoniak een niet-elektrolyt, maar waterig een elektrolyt?  Is K2O een ionische binding of een covalente binding?
Is K2O een ionische binding of een covalente binding?
 Opwarming van de aarde vergroot kans op vorstschade aan bomen
Opwarming van de aarde vergroot kans op vorstschade aan bomen Veranderen grote kikkervisjes in kikkers? Het is ingewikkeld, blijkt uit onderzoek
Veranderen grote kikkervisjes in kikkers? Het is ingewikkeld, blijkt uit onderzoek  Stads- en vervoersplanning gekoppeld aan 2, 000 vroegtijdige sterfgevallen per jaar in Barcelona en Madrid
Stads- en vervoersplanning gekoppeld aan 2, 000 vroegtijdige sterfgevallen per jaar in Barcelona en Madrid Gezonde koralen in Biscayne Bay verrasten wetenschappers. Ze kunnen riffen helpen overleven
Gezonde koralen in Biscayne Bay verrasten wetenschappers. Ze kunnen riffen helpen overleven Er zijn dringend nieuwe regels nodig om onze oceanen te beschermen, wetenschappers waarschuwen
Er zijn dringend nieuwe regels nodig om onze oceanen te beschermen, wetenschappers waarschuwen
Hoofdlijnen
- Hoe ontstaan genetische aandoeningen bij mensen?
- Waarom fruitvliegjes de eerste dieren in de ruimte waren
- Hoe eiwitten gist helpen zich aan te passen aan veranderende omstandigheden
- Vloeistofdruppeltjes bepalen hoe cellen reageren op verandering, blijkt uit onderzoek
- Wat zijn de voordelen van Ribosomes?
- De vrouwelijke gameten ontwikkelen zich in structuren die follikels worden genoemd. Wat is een follikel?
- Machine learning toont verbanden tussen de groei van de bacteriële populatie en de omgeving
- Hoe een klein deel van de oceanen in de wereld aan de mondiale vraag naar zeevruchten zou kunnen voldoen
- Onderzoekers ontwikkelen een systeem om te beoordelen hoe effectief soorten zijn bij het bestuiven van gewassen
- Gemodificeerde spons kan olieverontreinigingen uit Arctische wateren terugwinnen

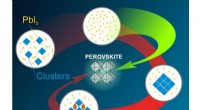
- Chemici bepalen hoe bijproducten bij de synthese van perovskieten kunnen worden vermeden
- Proces verwijdert tegelijkertijd giftige metalen en zout om schoon water te produceren

- Lab-on-a-chip helpt bij het zoeken naar menselijk DNA op plaats delict

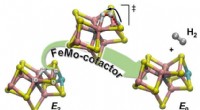
- Chemici onthullen één mechanisme van diwaterstofproductie door stikstofase
 Langste non-stop passagiersvlucht arriveert in Sydney
Langste non-stop passagiersvlucht arriveert in Sydney Hoe bioarcheologie werkt
Hoe bioarcheologie werkt  China lanceert eerste privéraket die satellieten kan vervoeren
China lanceert eerste privéraket die satellieten kan vervoeren Wie beoordeelt jou op basis van merkkeuzes?
Wie beoordeelt jou op basis van merkkeuzes?  Deep learning democratiseert beeldvorming op nanoschaal
Deep learning democratiseert beeldvorming op nanoschaal Zijn de meeste voedingsmiddelen zuren of basen?
Zijn de meeste voedingsmiddelen zuren of basen?  Begrijpen hoe overmatige aanpassing van spieren aan omgevingsomstandigheden wordt onderdrukt
Begrijpen hoe overmatige aanpassing van spieren aan omgevingsomstandigheden wordt onderdrukt  Vervuild Libanonmeer spuwt tonnen dode vis uit
Vervuild Libanonmeer spuwt tonnen dode vis uit
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

