
Wetenschap
H2 identificeren en de eigenschappen ervan beschrijven?
1. Atomische structuur :Waterstof heeft één proton, één elektron en geen neutronen. Het is het enige element met één enkel proton in de kern. Het elektron draait rond de kern in een bolvormige atomaire orbitaal.
2. Diatomisch molecuul :Waterstof bestaat doorgaans als een diatomisch molecuul (H2) waarbij twee waterstofatomen covalent aan elkaar gebonden zijn. De H-H-binding is een van de sterkste chemische bindingen en vereist een aanzienlijke hoeveelheid energie om te breken.
3. Lage dichtheid :Waterstof heeft een zeer lage dichtheid, waardoor het het lichtste element is. Bij kamertemperatuur en druk heeft waterstofgas een dichtheid van ongeveer 0,09 gram per liter.
4. Hoge thermische geleidbaarheid :Waterstof heeft de hoogste thermische geleidbaarheid van alle gassen. Dit betekent dat het zeer efficiënt warmte kan overdragen.
5. Ontvlambaar :Waterstof is licht ontvlambaar en kan gemakkelijk ontbranden in de aanwezigheid van een ontstekingsbron. Het brandt met een lichtblauwe vlam, waarbij grote hoeveelheden warmte en waterdamp vrijkomen.
6. Reactiviteit :Waterstof is een reactief element dat gemakkelijk verbindingen vormt met andere elementen. Het kan reageren met zuurstof om water te vormen, met koolstof om koolwaterstoffen te vormen en met metalen om hydriden te vormen.
7. Brandstof :Waterstof wordt beschouwd als een veelbelovende brandstofbron voor diverse toepassingen, waaronder brandstofcellen in voertuigen en energieopwekking. Het heeft een hoge energie-inhoud per massa-eenheid en produceert bij verbranding alleen water als bijproduct.
8. Overvloed :Waterstof is het meest voorkomende element in het universum en vormt ongeveer 92% van alle atomen in het universum. Het wordt voornamelijk aangetroffen in de moleculaire waterstofvorm (H2) in sterren en reuzenplaneten.
9. Isotopen :Waterstof heeft drie natuurlijk voorkomende isotopen:protium (gewone waterstof met één proton), deuterium (zware waterstof met één proton en één neutron) en tritium (radioactieve waterstof met één proton en twee neutronen).
10. Toepassingen :Waterstof heeft verschillende toepassingen, waaronder brandstof voor raketten en brandstofcellen, bij de productie van kunstmest, bij de raffinage van aardolie, bij de productie van kunststoffen en chemicaliën, en in de metallurgie.
Over het geheel genomen is waterstof een veelzijdig en essentieel element met unieke eigenschappen die het belangrijk maken op verschillende wetenschappelijke, industriële en technologische gebieden.
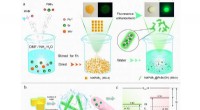
 Wetenschappers vereenvoudigen het proces om polymeren te maken met door licht geactiveerde nanodeeltjes
Wetenschappers vereenvoudigen het proces om polymeren te maken met door licht geactiveerde nanodeeltjes Wat is het proces waarbij vloeistoffen veranderen in vaste stoffen?
Wat is het proces waarbij vloeistoffen veranderen in vaste stoffen?  Onderzoeker helpt bij het classificeren van nieuwe vormen van duurzame lichtenergie
Onderzoeker helpt bij het classificeren van nieuwe vormen van duurzame lichtenergie Een kleur verven
Een kleur verven Upcycling van kunststoffen door dynamische cross-linking
Upcycling van kunststoffen door dynamische cross-linking
 Alles wat u moet weten over giftige algenbloei
Alles wat u moet weten over giftige algenbloei Complex, oerbossen kunnen sommige vogelsoorten beschermen in een opwarmend klimaat
Complex, oerbossen kunnen sommige vogelsoorten beschermen in een opwarmend klimaat Waterinfrastructuur ontwerpen voor klimaatonzekerheid
Waterinfrastructuur ontwerpen voor klimaatonzekerheid Verdienen vulkanen of een asteroïde de schuld voor het uitsterven van dinosauriërs?
Verdienen vulkanen of een asteroïde de schuld voor het uitsterven van dinosauriërs? Uitbreiding van cannabisgewas naar bossen bedreigt leefgebied voor wilde dieren, veroorzaakt andere milieuschade
Uitbreiding van cannabisgewas naar bossen bedreigt leefgebied voor wilde dieren, veroorzaakt andere milieuschade
Hoofdlijnen
- Welke drie factoren beïnvloeden de eigenschap van het organisme?
- Onderzoekers modelleren voordelen van bosherstel aan rivieroevers
- Grootte is belangrijk - hoe trips hun partners kiezen
- Wat doen alle delen van een cel?
- Wat hebben plantencellen die mens?
- Wetenschappers ontdekken hoe gistcellen fysieke spanningen waarnemen op de membranen die hen beschermen
- Stille soorten worden met uitsterven bedreigd:onderzoek wijst op vooringenomenheid in onderzoek naar natuurbehoud
- Wat zijn de onderdelen van de celcyclus?
- Herprogrammering van buiten naar binnen:antilichaamonderzoek suggereert een betere manier om stamcellen te maken
- Osteoblastisch lysosoom speelt een centrale rol bij mineralisatie
- Bij veldproeven, apparaat haalt water uit woestijnlucht

- Goedkope waterbehandeling

- Loodhalogenide perovskieten met verbeterde luminescentie en stabiliteit
- Nieuw chemisch proces een eerste stap naar het maken van nucleaire brandstof met vuur

 Sferische weergave brengt virtuele samenwerking dichter bij de realiteit
Sferische weergave brengt virtuele samenwerking dichter bij de realiteit Ontdekken van de verblijfplaats van de inclusieve zuidelijke rechtse walvis tijdens de warmere maanden
Ontdekken van de verblijfplaats van de inclusieve zuidelijke rechtse walvis tijdens de warmere maanden Zelfgemaakte spindroger
Zelfgemaakte spindroger  Eerste nauwkeurige simulatie van een virus dat een cel binnendringt
Eerste nauwkeurige simulatie van een virus dat een cel binnendringt De meeste handcarwashers zijn onderhevig aan een vorm van arbeidsuitbuiting, zegt nieuw rapport
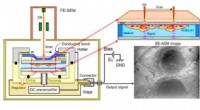
De meeste handcarwashers zijn onderhevig aan een vorm van arbeidsuitbuiting, zegt nieuw rapport Een biosensor voor het meten van extracellulaire waterstofperoxideconcentraties
Een biosensor voor het meten van extracellulaire waterstofperoxideconcentraties Waarom de intentie om een gebied slechts 25 jaar te behouden niet mag meetellen in de Australische doelstelling van 30% landbescherming
Waarom de intentie om een gebied slechts 25 jaar te behouden niet mag meetellen in de Australische doelstelling van 30% landbescherming  Een 500 jaar oude wet legde de basis voor hoe de Noren het heden begrijpen – en vertrouwen
Een 500 jaar oude wet legde de basis voor hoe de Noren het heden begrijpen – en vertrouwen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

