
Wetenschap
Osteoblastisch lysosoom speelt een centrale rol bij mineralisatie
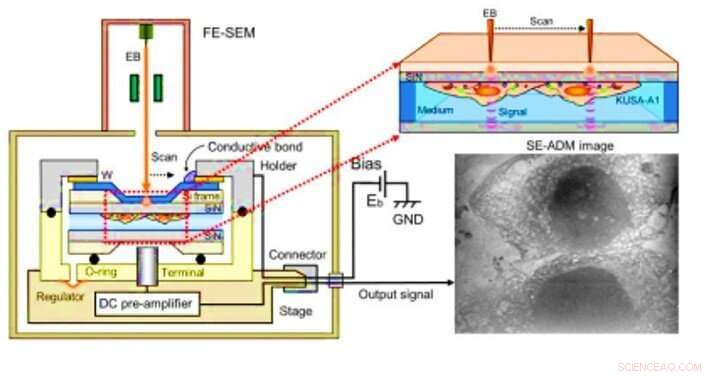
Scanning-elektronen-geassisteerde diëlektrische microscopie (SE-ADM) observatie van osteoblasten. (A) SE-ADM met hoge resolutie opgezet voor observatie van osteoblasten. Vloeistofmonsterhouder inclusief osteoblasten is gemonteerd op de aan de voorversterker bevestigde fase, die in de monster SEM-kamer wordt ingebracht. De aftastelektronenbundel wordt met een lage versnellingsspanning op de W-gecoate SiN-film aangebracht. Meetterminal onder de houder detecteert elektrische signalen door vloeibare monsters. Duidelijke intracellulaire structuren zijn zichtbaar (rechter afbeelding). Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aax0672
Mineralisatie wordt gemedieerd door osteoblasten, die minerale voorlopers afscheiden via matrixblaasjes (MV's) als een fundamenteel proces bij gewervelde dieren. De blaasjes zijn rijk aan calcium en fosfaat, met organische materialen zoals zure eiwitten. In een nieuwe studie die nu is gepubliceerd in wetenschappelijke vooruitgang , Tomoaki Iwayama en collega's van de afdelingen parodontologie, biomedisch onderzoek, orale wetenschap, Bij de ontwikkeling van biomaterialen en orale anatomie werd gebruik gemaakt van scanning-elektronenondersteunde diëlektrische microscopie (SE-ADM) en superresolutiemicroscopie (SRM) om levende osteoblasten te beoordelen tijdens mineralisatiecondities met een resolutie op nanoniveau. Ze ontdekten dat de calciumbevattende blaasjes multi-vesiculaire lichamen zijn die mineraliserende nanoblaasjes of matrixblaasjes (MV's) bevatten. Volgens de waarnemingen de MV's kunnen samen met lysosomen worden getransporteerd en worden uitgescheiden door exocytose. Iwayama et al. gepresenteerd bewijs dat de lysosomen amorf calciumfosfaat kunnen transporteren in mineraliserende osteoblastcellen.
Tijdens het fysiologische proces van botmineralisatie, de afzetting van calciumfosfaatkristallen vindt plaats in de extracellulaire matrix als een fundamenteel proces bij alle gewervelde dieren. In 1967, biologen Clarke Anderson en Ermanno Bonucci, individueel gevisualiseerde mineraalgerelateerde deeltjes in de extracellulaire ruimte met behulp van elektronenmicroscopie (EM). Wetenschappers herkenden deze deeltjes later als mineraliserende nanoblaasjes of matrixblaasjes (MV's). Tijdens de afgelopen 50 jaar van EM-onderzoeken naar MV's, biologen hebben geworsteld om het mechanisme van MV-vorming en -afscheiding te begrijpen, die grotendeels onbekend blijft.
Het verduidelijken van het mineralisatieproces van levende cellen met EM is een uitdaging, aangezien de monstervoorbereiding voor EM stappen vereist voor zowel chemische fixatie als alcoholische uitdroging. De stappen kunnen artefacten veroorzaken en zelfs onstabiele minerale voorlopers oplossen of verwijderen, waardoor een organische steiger achterblijft die bekend staat als een "kristalgeest". Terwijl wetenschappers met succes het proces van EM hadden gebruikt met behulp van gefixeerd en gedehydrateerd weefsel om de structuur van gemineraliseerde collageenfibrillen in bot te bekijken, om minerale voorlopers te bestuderen, ze moeten cryo-EM-processen gebruiken om uitdroging te voorkomen en dure, extreem snelle afkoeling met kleine exemplaren.
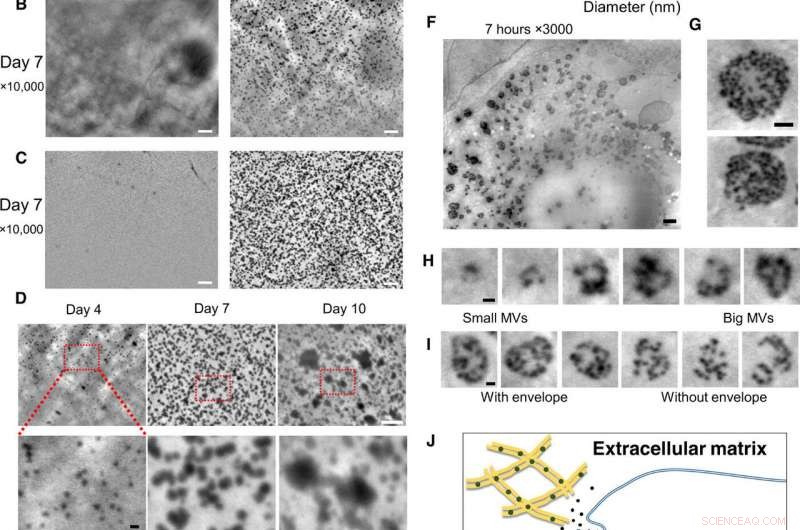
Observatie op nanoschaal van levende osteoblasten in kweekmedia, met behulp van het SE-ADM-systeem. (A) Representatieve SE-ADM-beelden met hoge resolutie van osteoblasten gekweekt met of zonder osteogene media gedurende 2 dagen. Zwarte deeltjes waren alleen duidelijk wanneer ze werden gekweekt in osteogene media (rechts, vierkant onderaan). (B) Representatieve SE-ADM-beelden met hoge resolutie van osteoblasten gekweekt met of zonder osteogene media gedurende 7 dagen. Er zijn veel zwarte deeltjes wanneer ze worden gekweekt in osteogene media (rechts). (C) Representatieve SE-ADM-beelden met hoge resolutie van de SiN-film na celverwijdering. In normale media, er worden geen deeltjes waargenomen (links). Het beeld van de film na verwijdering van cellen gekweekt in osteogene media toont veel heldere zwarte deeltjes verspreid over het hele gebied (rechts). (D) Vergelijking van deeltjesbeelden gedurende 4 tot 10 dagen cultuur in osteogene media. De deeltjesgrootte nam geleidelijk toe. (E) Verdeling van deeltjesgrootte gemeten gedurende 4 tot 10 dagen kweken in osteogene media. Ongeveer 900 tot 1100 deeltjes per tijdstip werden gemeten en uitgezet als een histogram. (F) Representatieve SE-ADM-beelden met hoge resolutie van osteoblasten die gedurende 7 uur zijn gekweekt met osteogene media. (G) MVB's hebben heldere grijze enveloppen. (H) Knip afbeeldingen van verschillende MVB-formaten, inclusief deeltjes. (I) Vergelijking van MVB's met of zonder grijze envelop. (J) Schematische weergave van intracellulaire vorming en transport van MVB in mineraliserende osteoblasten. Schaalbalken, 1 m in (A) tot (C) en (F); 500 nm in (G); 200 nm in (D, onderkant), (H), en ik). Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aax0672
Om deze beperkingen in het huidige werk te overwinnen, Iwayama et al. gebruikte een nieuw microscopisch systeem dat bekend staat als scanning electron-assisted diëlektrische microscopie (SE-ADM). De methode had eerder een resolutie op nanoschaal en beeldvorming met hoog contrast bereikt voor zoogdiercellen in waterige media zonder kleuring. De wetenschappers gebruikten dezelfde techniek (hoge resolutie SE-ADM) om de mogelijkheid te onderzoeken om MV's in intacte osteoblasten te bekijken om de biogenese van MV-handel te begrijpen. Voor de osteoblastcellijn gebruikten ze murine (muis) osteoblastische cellijn KUSA-A1, met hoge osteogene capaciteit in vitro en in vivo. Na celkweek onder adequate omstandigheden, Iwayama et al. observeerde de cellen met SE-ADM om normale intracellulaire structuren te identificeren. De wetenschappers observeerden dat MV's zich aanpasten aan collageenfibrillen na 4 tot 10 dagen celgroei in osteogene media en dat de uitgescheiden deeltjesgrootte toenam als gevolg van fusie of deeltjesgroei, met hun afmetingen in overeenstemming met eerdere rapporten om te suggereren dat het inderdaad MV's waren.
Bij nader onderzoek met SE-ADM, ze merkten de betrokkenheid op van de lysosomale route om intraluminale MV's te transporteren en uit te scheiden in een soortgelijk proces als exosomen. interessant, zowel exosomen als MV's worden gecategoriseerd als extracellulaire blaasjes met vergelijkbare afmetingen; ze worden beide uitgescheiden door osteoblasten en hebben gedeelde functies tijdens cel-celcommunicatie.

Karakterisering van mineraalhoudende blaasjes. (A en B) deeltjesafbeeldingen met hoge resolutie vóór (A) en na (B) verwijdering van cellen die gedurende 7 dagen in osteogene media zijn gekweekt. Pseudocolor-kaarten van vergrote deeltjesafbeeldingen aangegeven door rode pijlen worden weergegeven aan de rechterkant van (B). Deeltjes vertonen zeer gladde structuren zonder kristallen. (C) Scanning elektronenmicroscopie (SEM) beelden en EDX spectrometrische analyse van deeltjes op een SiN-film. SEM-afbeelding aan de linkerkant vertoont de SiN-film na verwijdering van cellen gekweekt in normale media, die geen deeltjes vertoont, en EDX-spectrometrische gegevens tonen geen pieken van fosfor en calcium. In tegenstelling tot, het SEM-beeld en de EDX-spectrometrische gegevens aan de rechterkant tonen deeltjes en scherpe pieken van fosfor en calcium na kweek in osteogene media. (D) Analyse van deeltjeselementen met behulp van EDX spectrometrische kaarten. Deeltjes bevatten fosfor, calcium, koolstof, en stikstof. (E) Raman-spectra verkregen uit osteoblasten die gedurende 23 dagen met of zonder osteogene media zijn gekweekt. Scherpe piek van 960 cm−1 was alleen duidelijk in osteogene media (rechterkant). a.u., willekeurige eenheden. (F) Vergelijking van SE-ADM-beelden van Alpl knock-out (KO) osteoblasten in normale en osteogene media. Deeltjes verdwenen volledig in osteogene media. (G) EDX-spectrum van deeltjes van Alpl KO osteoblasten op een SiN-film. Linker EDX-spectrometrische gegevens vertonen de SiN-film na verwijdering van cellen gekweekt in normale media, die geen pieken van fosfor en calcium vertonen. Bovendien, deeltjes in osteogene media van gegevens aan de rechterkant vertonen geen pieken in fosfor en calcium. Schaalbalken, 1 m in (A), (C, bovenkant), (NS), en (F); 200 nm in (B); 100 nm in (B, Rechtsaf). Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aax0672
In de volgende stap, Iwayama et al. onderzocht of deze deeltjes MV's waren die calcium en/of fosfaat bevatten. Voor deze, ze kweekten de cellen gedurende 7 dagen in osteogene media en observeerden ze met SE-ADM om zeer gladde structuren zonder kristalfacetten vast te leggen. Dit suggereerde dat de MV's niet kristalliseerden maar amorf bleven, zoals ook werd vastgelegd in een eerdere studie. Toen de wetenschappers de MV's op een SiN-film (siliciummononitride) onderzochten, ze observeerden scherpe pieken die overeenkomen met fosfor, calcium, koolstof- en zuurstofelementen. Ze bevestigden de bevindingen met behulp van Raman-spectroscopie om de aanwezigheid van calciumfosfaat in MV's aan te tonen.
De wetenschappers onderzochten ook de effecten van hypofosfatasie, een medische aandoening die wordt gecodeerd door de Alpl (alkalische fosfatase) gen , waarbij osteoblasten in vitro geen mineralisatie ondergaan. Voor deze, ze bewerkten het genoom van osteoblastcellen met behulp van de CRISPR-Cas9-technologie voor het bewerken van het genoom om Alpl-knock-out-osteoblastklonen te genereren. Toen Iwayama et al. onderzocht de knock-out-klonen met SE-ADM met hoge resolutie, ze hebben geen MV's waargenomen, wat verder werd bevestigd met behulp van spectrometrische analyse vanwege de afwezigheid van fosfor- en calciumpieken.
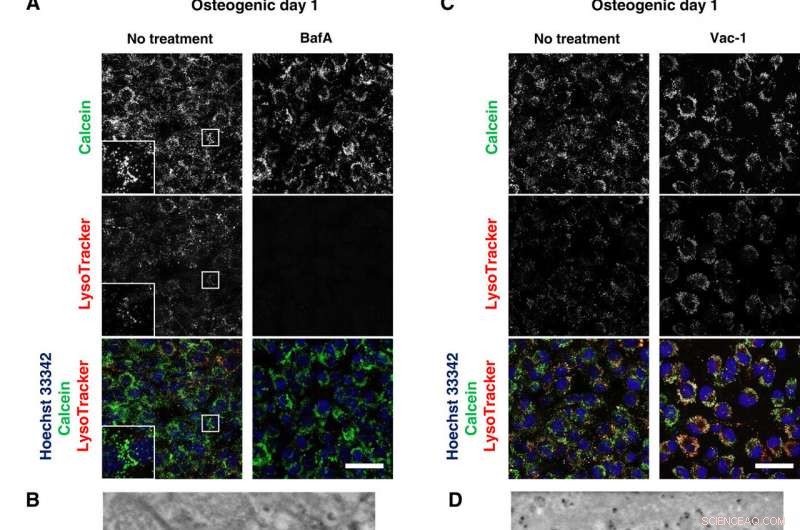
Lysosomale remmers blokkeren mineralisatie. (A en C) Confocale live-beeldvorming van 50 nM BafA- of 10 μM Vac-1-behandelde osteoblasten. Cellen werden gekweekt in osteogene media die BafA of Vac-1 bevatten en gekleurd met Hoechst 33342 en LysoTracker-inzetstukken vertonen een hogere vergroting en een omkaderd gebied van elk kanaal. (B en D) SD-ADM-afbeeldingen van met BafA of Vac-1 behandelde osteoblasten. Cellen werden gekweekt in osteogene media die BafA of Vac-1 bevatten. (E) Alizain Red S-kleuring uitgevoerd zonder fixatie. Cellen werden gekweekt in osteogene media die BafA of Vac-1 bevatten en gekleurd met Alizain Red S. Representatieve confocale beelden. Schaalbalken, 50 m in (A), (C), en (E); 2 m (B) en (D). Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aax0672
Na het direct observeren van de productie en secretie van MV's met SE-ADM, de wetenschappers onderzochten verder de betrokkenheid van lysosomen bij intracellulaire handel in MV's om levende osteoblastmineralisatie te observeren. Ze kweekten de cellen in calciumbevattende osteogene media en kleurden ze met LysoTracker om de intracellulaire componenten van belang te detecteren. Iwayama et al. lokaliseerde de met calceïne vervulde blaasjes die overeenkwamen met lysosomen om de biogenese van MV's in lysosomen te suggereren na hun fusie met calceïne + blaasjes. De wetenschappers volgden de experimenten met onderzoek naar functieverlies en functionele remming om de routes verder te deconstrueren en intracellulaire werkingsmechanismen tijdens mineralisatie van levende cellen in vitro te onderzoeken.
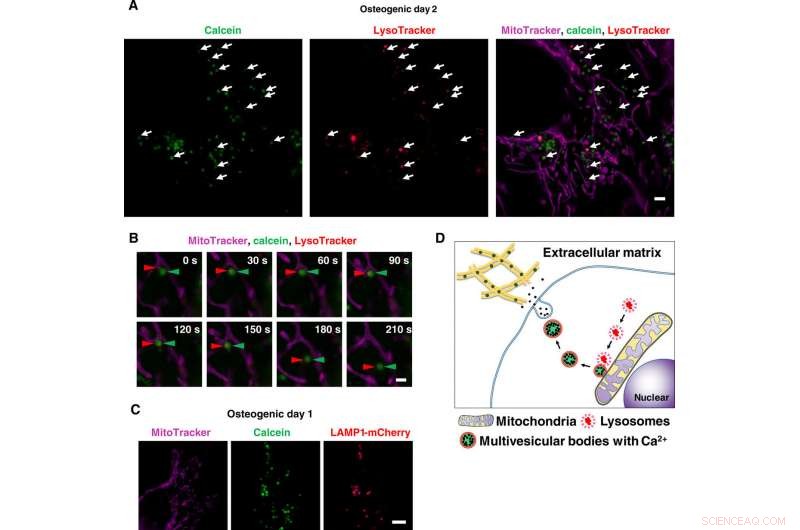
Live-beeldvorming met superresolutie van calciumbevattende vesikeltransporten via lysosomen. (A) Momentopname van time-lapse SRM-beelden van calceïne-gelabelde osteoblasten. Cellen werden gekweekt met calceïne en gekleurd met Lysotracker en MitoTracker. Witte pijlen geven colokalisatie van lysosomen en calceïne-positieve blaasjes aan. (B) Close-up van time-lapse SRM-beelden van calceïne-gelabelde osteoblasten. Rode pijlpunten geven lysosoom aan, en groene pijlpunten geven calceïne aan. Once lysosomes fused to calcein-positive vesicles adjacent to mitochondria, they started to move toward extracellular space. (C) Representative SRM image of LAMP1-mCherry–expressing cells. Cells were transfected with LAMP1-mCherry plasmid, cultured with calcein, and stained with MitoTracker. Calcein-positive vesicles matched to LAMP1-mCherry–positive lysosomes. (D) Schematic view of lysosomal involvement in transportation of calcium in mineralizing osteoblasts. Scale bars, 2 μm in (A), 1 μm in (B), and 10 μm in (C). Krediet:wetenschappelijke vooruitgang, doi:10.1126/sciadv.aax0672
Scientists had previously reported the involvement of mitochondria during mineralization due to the presence of electron-dense calcium and phosphorous-rich granules in osteoblast mitochondria. This was observed with a modified cryotechnique. Verder, reports also suggest the direct contact of lysosomes and mitochondria with functional significance. When Iwayama et al. stained cells with LysoTracker together with MitoTracker and observed the intracellular components under N-SIM structured illumination super-resolution microscopy (SRM). They observed the presence of most calcein-fulfilled vesicles next to mitochondria and matched with lysosomes. During SRM-time lapse imaging, the scientists further obtained views of intracellular transport of LysoTracker containing vesicles fused to static calcein vacuoles adjacent to mitochondria to validate their hypothesis.
Op deze manier, together with observations of other SRM systems and additional cell lines, Tomoaki Iwayama and colleagues proposed a mineralization mechanism. Wherein lysosomes played a central role in intracellular MV biogenesis and trafficking within osteoblasts. It was reasonable to involve lysosomes for osteoblasts to transport amorphous calcium phosphate without crystallization during its transport in the cytosol. The scientists aim to conduct further experiments to understand the regulatory molecules for MVs and investigate if MVs and exosomes have similar constitutions and mechanism underlying their generation, secretion and function. The SE-ADM strategy used in the present work can be installed into existing scanning electron microscopy apparatus at a low cost. The work developed in the study will offer non-invasive, high-resolution imaging at the nanoscale applicable to all scientific fields.
© 2019 Wetenschap X Netwerk
 Hoe het iso-elektrische punt van peptiden te berekenen
Hoe het iso-elektrische punt van peptiden te berekenen Bacteriefabrieken gebruikt om potentiële nieuwe malariamedicijnen te ontdekken
Bacteriefabrieken gebruikt om potentiële nieuwe malariamedicijnen te ontdekken Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen
Nieuwe behandelingstechnologie kan de belasting van nucleair afval in het VK verminderen Team lost tien jaar oud mysterie op in chemische transformaties
Team lost tien jaar oud mysterie op in chemische transformaties Nieuwe methode zet koolstofdioxide om in methaan bij lage temperaturen
Nieuwe methode zet koolstofdioxide om in methaan bij lage temperaturen
 Canadese ijsbergjager op het spoor van wit goud
Canadese ijsbergjager op het spoor van wit goud NASA-satelliet toont tropische cycloon Gelena bij Madagascar
NASA-satelliet toont tropische cycloon Gelena bij Madagascar CO2-uitstoot veroorzaakt verloren arbeidsproductiviteit, uit onderzoek blijkt
CO2-uitstoot veroorzaakt verloren arbeidsproductiviteit, uit onderzoek blijkt Ontdekking van parasitaire arseencyclus kan een glimp van leven in de toekomst bieden, warmere oceanen
Ontdekking van parasitaire arseencyclus kan een glimp van leven in de toekomst bieden, warmere oceanen Hoe ziet een basswood-boom eruit?
Hoe ziet een basswood-boom eruit?
Hoofdlijnen
- Passagiersduivengenoom toont effecten van natuurlijke selectie in een enorme populatie
- Nee,
- Niet zo koude eend? Man blijft zoeken naar uitgestorven vogel
- Waar voedsel beperkt is, guppy-moeders dragen hun jongen langer
- Hoe kunnen nieuwe cellen iemands gezichtsvermogen herstellen?
- Invasieve superschurkenkrab kan door zijn kieuwen heen eten
- Overeenkomsten tussen huidcellen en zenuwen
- Wat zijn de twee hoofdfasen van celdeling?
- Zijn er verschillen tussen mannelijke en vrouwelijke pesters?
- Met de steigermethode kunnen biochemici eiwitten in opmerkelijk detail zien

- Hydrogel baant weg voor biomedische doorbraak

- Gras vervangt plastic in meeneemverpakkingen

- Onderzoek toont potentieel aan om verven te verbeteren, coatings
- Licht gebruiken om de reikwijdte van carbonyleringsreacties uit te breiden

 NASA volgt bosbranden van bovenaf om brandweerlieden beneden te helpen
NASA volgt bosbranden van bovenaf om brandweerlieden beneden te helpen IJsberg doemt op boven Groenlands dorp gezien vanuit de ruimte
IJsberg doemt op boven Groenlands dorp gezien vanuit de ruimte Klein, snel, en zeer energiezuinig geheugenapparaat geïnspireerd op lithium-ionbatterijen
Klein, snel, en zeer energiezuinig geheugenapparaat geïnspireerd op lithium-ionbatterijen Hoe Finland omarmde om 's werelds gelukkigste natie te zijn
Hoe Finland omarmde om 's werelds gelukkigste natie te zijn Psychologen:vrouwen zijn niet verantwoordelijk voor loonkloof
Psychologen:vrouwen zijn niet verantwoordelijk voor loonkloof Een TRAP instellen voor pandemische virussen
Een TRAP instellen voor pandemische virussen Medewerkers spreken zich uit bij Wayfair, Googlen. Hebben millennials gedood omdat ze bang waren voor de baas?
Medewerkers spreken zich uit bij Wayfair, Googlen. Hebben millennials gedood omdat ze bang waren voor de baas? Conservatieve media domineerden de berichtgeving over de campagne van 2016, vondsten melden
Conservatieve media domineerden de berichtgeving over de campagne van 2016, vondsten melden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | German | Dutch | Swedish | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

