
Wetenschap
Welke heeft de sterkste intermoleculaire kracht NH3 of H20?
H2O heeft sterkere intermoleculaire krachten dan NH3.
Zowel H2O als NH3 zijn polaire moleculen. De elektronegativiteit van stikstof- en zuurstofatomen is respectievelijk 3,0 en 3,5. De zuurstof-waterstofbinding in H2O is dus polairder dan de stikstof-waterstofbinding in NH3. Als gevolg hiervan kunnen H2O-moleculen sterkere waterstofbruggen met elkaar vormen.
De sterkere waterstofbruggen in H2O leiden tot een hoger kookpunt, hoger smeltpunt en hogere oppervlaktespanning vergeleken met NH3.
 Hoe de lading van een ion te berekenen
Hoe de lading van een ion te berekenen  Een betere beoordeling van de gevoeligheid van bacteriën voor antibiotica kan de manier waarop medicijnen worden voorgeschreven veranderen
Een betere beoordeling van de gevoeligheid van bacteriën voor antibiotica kan de manier waarop medicijnen worden voorgeschreven veranderen Verschil tussen natriumchloriet en natriumchloride
Verschil tussen natriumchloriet en natriumchloride Waarom het faseveranderingsmateriaal ijzer-tellurium het beste elektriciteit geleidt in zijn ongeordende amorfe fase
Waarom het faseveranderingsmateriaal ijzer-tellurium het beste elektriciteit geleidt in zijn ongeordende amorfe fase  wat is de eenheid van zuiverheid van een chemische stof?
wat is de eenheid van zuiverheid van een chemische stof?
 Ziekenhuisopnames verminderden zodra elektriciteitscentrales met kolen stopten of betere emissiecontroles installeerden
Ziekenhuisopnames verminderden zodra elektriciteitscentrales met kolen stopten of betere emissiecontroles installeerden De strijd om de toekomst van de landbouw:wat u moet weten
De strijd om de toekomst van de landbouw:wat u moet weten  Methodologie voor de beoordeling van de geloofwaardigheid van historische wereldwijde LUCC-datasets
Methodologie voor de beoordeling van de geloofwaardigheid van historische wereldwijde LUCC-datasets Verschillen tussen noord- en zuidflank
Verschillen tussen noord- en zuidflank Wetenschap zegt:tijdperk van monsterlijke orkanen die de Atlantische Oceaan bestormen
Wetenschap zegt:tijdperk van monsterlijke orkanen die de Atlantische Oceaan bestormen
Hoofdlijnen
- Ethiek Research Paper Onderwerpen
- Wat zit er in een naam? Een taalkundige legt uit waarom sommige babynamen jaar later de hitlijsten domineren
- Wat is de brugfase van glycolyse?
- Dode vissen en depressies aan de oevers van de Oder
- Brazilië heeft twee populaties Amerikaanse brulkikkers, een exotische soort die een dodelijke schimmel overdraagt
- Heeft gonorroe ons grootouders gegeven?
- Wie zijn de verschillende biologen en hun bijdragen aan de ontwikkeling van de biologische biotechnologie?
- Nieuwe mierenvogelsoort ontdekt in Peru
- IJsberen die rendieren eten:normaal gedrag of gevolg van klimaatverandering?
- Video:Hoeveel weegt een wolk?

- Make like a leaf:onderzoekers ontwikkelen methode om koolstofdioxide om te zetten

- Onderzoekers rapporteren over live intracellulaire beeldvorming met nieuwe, voorwaardelijk actieve immunofluorescentieprobe
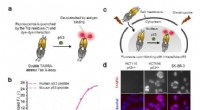
- Experimenten en analyses laten zien hoe elektronen en protonen samenkomen op een elektrodeoppervlak
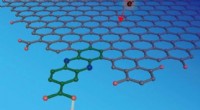
- Onderzoekers lossen 60 jaar oude puzzel op over superhard materiaal
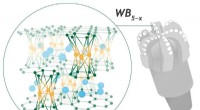
 Computerwetenschappers ontwikkelen een videogame die leert programmeren in Java
Computerwetenschappers ontwikkelen een videogame die leert programmeren in Java  Drie manieren waarop de fossiele brandstofindustrie vrouwen in de steek heeft gelaten, en hoe schone energie kan leren van haar fouten
Drie manieren waarop de fossiele brandstofindustrie vrouwen in de steek heeft gelaten, en hoe schone energie kan leren van haar fouten Inheemse kennis sleutel tot succesvol ecosysteemherstel
Inheemse kennis sleutel tot succesvol ecosysteemherstel Wat is een medische plant?
Wat is een medische plant?  Hoe wordt mechanische energie afgevoerd?
Hoe wordt mechanische energie afgevoerd?  Het hebben van klanten uit vele sectoren kan de effectiviteit van accountantskantoren schaden
Het hebben van klanten uit vele sectoren kan de effectiviteit van accountantskantoren schaden Een populatiedichtheidskaart maken
Een populatiedichtheidskaart maken  Hominide prenatale groeisnelheid bleek te zijn toegenomen nadat afstammingslijn van chimpansees was gescheiden
Hominide prenatale groeisnelheid bleek te zijn toegenomen nadat afstammingslijn van chimpansees was gescheiden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

