
Wetenschap
Hoe ontstaat een ionische verbinding?
Wanneer bijvoorbeeld natrium- (Na)- en chloor- (Cl)-atomen reageren, verliezen de natriumatomen elk één elektron aan de chlooratomen. Dit resulteert in de vorming van natriumionen (Na+) en chloride-ionen (Cl-). De natriumionen worden aangetrokken door de chloride-ionen en omgekeerd, waardoor de ionische verbinding natriumchloride (NaCl) ontstaat.
De vorming van ionische verbindingen wordt aangedreven door de volgende factoren:
* Elektronegativiteit: Elektronegativiteit is het vermogen van een atoom om elektronen aan te trekken. Hoe groter het verschil in elektronegativiteit tussen twee atomen, hoe waarschijnlijker het is dat ze een ionische verbinding vormen.
* Ionisatie-energie: Ionisatie-energie is de energie die nodig is om een elektron uit een atoom te verwijderen. Hoe lager de ionisatie-energie van een atoom, hoe waarschijnlijker het is dat het een positief ion vormt.
* Elektronenaffiniteit: Elektronenaffiniteit is de energie die vrijkomt wanneer een atoom een elektron verkrijgt. Hoe groter de elektronenaffiniteit van een atoom, hoe waarschijnlijker het is dat het een negatief ion vormt.
Ionische verbindingen hebben doorgaans hoge smelt- en kookpunten en zijn goede elektriciteitsgeleiders wanneer ze in water worden opgelost. Ze zijn doorgaans ook vaste stoffen bij kamertemperatuur.
 Hooggerechtshof in Europa zal baanbrekende klimaatvonnissen uitvaardigen
Hooggerechtshof in Europa zal baanbrekende klimaatvonnissen uitvaardigen  Oude verzwakking van de aardkorst verklaart ongebruikelijke aardbevingen in de plaat
Oude verzwakking van de aardkorst verklaart ongebruikelijke aardbevingen in de plaat We hebben meer mensen nodig:uitgeputte brandweerlieden bestrijden Siberische branden
We hebben meer mensen nodig:uitgeputte brandweerlieden bestrijden Siberische branden Door Indianen op het platteland te geven wat ze willen, neemt de vraag naar kooktoestellen toe
Door Indianen op het platteland te geven wat ze willen, neemt de vraag naar kooktoestellen toe Miljarden verspild aan Australische subsidies voor waterwinning, studie vondsten
Miljarden verspild aan Australische subsidies voor waterwinning, studie vondsten
Hoofdlijnen
- Onzekerheid vertroebelt VN-besprekingen over biopiraterijverdrag
- Onderzoek onthult dat controversiële insecticiden giftig zijn voor zangvogels
- Sucrose wordt gevormd wanneer glucose zich verbindt met fructose.
- Onderzoekers ontwikkelen een gel voor het kweken van grote hoeveelheden neurale stamcellen
- Nieuwe slangensoort verstopt zich in het volle zicht
- Hoe hersendood werkt
- Welke twee uitspraken verklaren hoe de orgaansystemen van een regenworm de cellen van zuurstof helpen voorzien?
- Hoe dieren hun juiste maat bereiken
- De vorming van de mannelijke geslachtscellen of sperma wordt een wat genoemd?
- Schone technologie om chitosan met laag molecuulgewicht te maken

- De strijd tegen moeilijk te behandelen schimmelinfecties

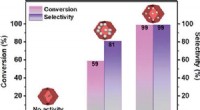
- Een katalytisch systeem van niet-edele metalen voor zeer efficiënte hydrogenering van nitroarenen
- Smartphonelab levert testresultaten in een oogwenk

- Ontwerpbehandeling van geavanceerde metalen voor betere beeldhouwkunst

 Mannen van kleur vermijden openbare plaatsen uit angst voor betrokkenheid bij strafrechtelijke agenten
Mannen van kleur vermijden openbare plaatsen uit angst voor betrokkenheid bij strafrechtelijke agenten Hoe zien genen eruit?
Hoe zien genen eruit?  Hadeda ibissen zesde zintuig werkt het beste op natte grond:nieuw onderzoek is een wake-up call voor het voortbestaan van waadvogels
Hadeda ibissen zesde zintuig werkt het beste op natte grond:nieuw onderzoek is een wake-up call voor het voortbestaan van waadvogels  Hoe is Earth Day geëvolueerd?
Hoe is Earth Day geëvolueerd?  Filipijnse Slangensoorten
Filipijnse Slangensoorten  Hoe houtalcohol te maken door destillatie
Hoe houtalcohol te maken door destillatie Onderzoek toont aan hoe machinaal leren sociaal verzorgingsgedrag kan identificeren aan de hand van versnellingssignalen bij wilde bavianen
Onderzoek toont aan hoe machinaal leren sociaal verzorgingsgedrag kan identificeren aan de hand van versnellingssignalen bij wilde bavianen  Vrouwen, werknemers van kleur die de meeste banen met een hoog risico / lage beloning in Washington vullen
Vrouwen, werknemers van kleur die de meeste banen met een hoog risico / lage beloning in Washington vullen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

