
Wetenschap
Wat gebeurt er als candelwas verandert van vast naar vloeibaar?
- Temperatuurstijging :Naarmate het kaarsvet wordt verwarmd, stijgt de temperatuur, waardoor de moleculen energie krijgen en krachtiger bewegen.
- Moleculaire beweging :De verhoogde energie zorgt ervoor dat de moleculen krachtiger trillen en roteren, waardoor de intermoleculaire krachten die ze in een vaste positie houden, worden verbroken.
- Structurele verandering :Naarmate de intermoleculaire krachten zwakker worden, raken de moleculen minder dicht opeengepakt en begint de geordende, kristallijne structuur van de vaste was af te breken.
- Overgang naar vloeistof :Op het smeltpunt worden de intermoleculaire krachten overwonnen en ondergaat de was een faseovergang van vast naar vloeibaar. De moleculen hebben nu voldoende energie om vrij te bewegen en worden niet langer in een vaste positie gehouden.
De vloeibare was kenmerkt zich door de volgende eigenschappen:
- Vloeiendheid :De vloeibare was kan vloeien en de vorm aannemen van zijn houder.
- Lagere dichtheid :De vloeibare was heeft een lagere dichtheid vergeleken met de vaste vorm, waardoor deze uitzet en meer ruimte in beslag neemt.
- Oppervlaktespanning :De vloeibare was vertoont oppervlaktespanning als gevolg van de cohesiekrachten tussen de moleculen, wat resulteert in de vorming van een gebogen oppervlak.
- Verdamping :Bij hogere temperaturen kan de vloeibare was verdampen, waardoor wasdampen in de lucht vrijkomen.
Bij afkoeling ondergaat de vloeibare was het omgekeerde proces van stollen, waarbij de moleculen energie verliezen, vertragen en de intermoleculaire krachten hervormen, wat leidt tot de overgang terug naar een vaste toestand.
 Waar is het universum van gemaakt?
Waar is het universum van gemaakt?  Een 3D-model laat zien hoe onzichtbare golven materialen binnen aquatische ecosystemen verplaatsen
Een 3D-model laat zien hoe onzichtbare golven materialen binnen aquatische ecosystemen verplaatsen  Goedkoop chloordoseerapparaat verbetert de veiligheid van kraanwater in regio's met weinig hulpbronnen
Goedkoop chloordoseerapparaat verbetert de veiligheid van kraanwater in regio's met weinig hulpbronnen Om het leven op aarde te redden, hier is de oplossing van $ 100 miljard per jaar
Om het leven op aarde te redden, hier is de oplossing van $ 100 miljard per jaar Recordbrekende temperaturen waarschijnlijker in bevolkte tropen
Recordbrekende temperaturen waarschijnlijker in bevolkte tropen
Hoofdlijnen
- Waarom sommige mensen flauwvallen als ze bloed zien
- Welke organismen profiteren van de relatie tussen ossenpikker en nijlpaard?
- Hoe vogelgriep werkt
- Onderzoekers bepalen hoe het SARS-CoV-2-virus menselijke longcellen kaapt en snel schade veroorzaakt
- Worden biologische groenten en fruit binnenkort goedkoper?
- Waarom het idee dat het Engels een gemeenschappelijke Angelsaksische oorsprong heeft, een mythe is
- Een kleine factor heeft een grote impact op genoombewerking
- Onderzoek toont aan dat menselijke activiteit het gedrag van bobcat beïnvloedt
- Wie is jouw papa? Als je een gorilla bent, maakt het niet uit
- Studie benadrukt belofte van galliumoxiden voor stralingsdetectoren van de volgende generatie

- Residu van stabilisator in inkten blijkt de geleidbaarheid in 3D-geprinte elektronica te remmen

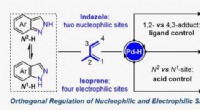
- Orthogonale regulatiestrategie biedt nieuwe kansen voor opbouw van moleculaire complexiteit
- Eenvoudige ruil voor een groenere toolkit
- Nieuwe topologische materialen kunnen meerdere elektrische eigenschappen hebben

 Is disulfurpentoxide covalent of ionisch?
Is disulfurpentoxide covalent of ionisch?  Planten die stikstof uit de lucht halen, gedijen goed in droge omgevingen
Planten die stikstof uit de lucht halen, gedijen goed in droge omgevingen Onderzoeker onderzoekt leergewoonten van skateboarders
Onderzoeker onderzoekt leergewoonten van skateboarders De Coloradowolf die vorige maand dood werd aangetroffen, is waarschijnlijk gedood door een bergleeuw, zeggen federale functionarissen
De Coloradowolf die vorige maand dood werd aangetroffen, is waarschijnlijk gedood door een bergleeuw, zeggen federale functionarissen  EU verliest bod om WTO Airbus-uitspraak ongedaan te maken
EU verliest bod om WTO Airbus-uitspraak ongedaan te maken Doneer je haar om ons water schoon te houden
Doneer je haar om ons water schoon te houden Wat zijn een atoom, elektron, neutron en proton?
Wat zijn een atoom, elektron, neutron en proton?  Indiase rechtbank daagt Delhi uit om aan te tonen dat het autoverbod de smog vermindert
Indiase rechtbank daagt Delhi uit om aan te tonen dat het autoverbod de smog vermindert
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

