
Wetenschap
Wat is de Bond-hoekstructuur en -vorm voor propaan?
1. Tetraëdrische koolstofatomen:Propaan bestaat uit drie koolstofatomen, die elk een tetraëdrische elektronenpaargeometrie hebben. Dit betekent dat de vier elektronenparen (drie enkele bindingen met waterstofatomen en één enkele binding met een ander koolstofatoom) rond elk koolstofatoom in een driedimensionale tetraëdrische vorm zijn gerangschikt.
2. C-C-C-bindingshoek:De bindingshoek tussen de drie koolstofatomen in propaan is ongeveer 109,5 graden. Dit is de ideale bindingshoek voor tetraëdrische geometrie, waarbij de elektronenparen elkaar afstoten om de afstand ertussen te maximaliseren.
3. Trigonale piramidevorm:De algemene moleculaire vorm van propaan is trigonaal piramidaal. Deze vorm is het resultaat van de tetraëdrische opstelling van de koolstofatomen. De drie waterstofatomen die aan elk koolstofatoom zijn bevestigd, bevinden zich op de hoeken van een driehoek, met het koolstofatoom bovenaan de piramide.
4. Vrije rotatie:De CC-bindingen in propaan zorgen voor vrije rotatie. Dit betekent dat het molecuul verschillende conformaties kan aannemen door rond de C-C-bindingen te roteren. De twee meest voorkomende conformaties zijn de verduisterde conformatie, waarbij de waterstofatomen op aangrenzende koolstofatomen uitgelijnd zijn, en de verspringende conformatie, waarbij de waterstofatomen op aangrenzende koolstofatomen zo ver mogelijk uit elkaar zijn geplaatst.
5. Symmetrische structuur:Propaan is een symmetrisch molecuul. De drie koolstofatomen en de daaraan verbonden waterstofatomen zijn symmetrisch rond het centrale koolstofatoom gerangschikt. Deze symmetrie draagt bij aan de stabiliteit van het molecuul en zijn karakteristieke eigenschappen.
 Zout smelt geen ijs - zo maakt het de winterse straten echt veilig
Zout smelt geen ijs - zo maakt het de winterse straten echt veilig Hoe gevangen radicalen uit carboxyl kunnen worden bevrijd
Hoe gevangen radicalen uit carboxyl kunnen worden bevrijd  Wetenschappers gebruiken licht om vetzuren om te zetten in alkanen
Wetenschappers gebruiken licht om vetzuren om te zetten in alkanen Studie werpt nieuw licht op productie van hydroxylradicalen, die helpen bij het afbreken van luchtverontreinigende stoffen
Studie werpt nieuw licht op productie van hydroxylradicalen, die helpen bij het afbreken van luchtverontreinigende stoffen Materiaalwetenschappers maken sterker kobalt voor brandstofcellen
Materiaalwetenschappers maken sterker kobalt voor brandstofcellen
Hoofdlijnen
- Forsyth-wetenschappers krijgen meer inzicht in hoe embryo's zich onderscheiden van links en rechts
- Wat gebeurt er als mitose fout gaat en in welke fase gaat het fout?
De meeste cellen groeien en delen voortdurend. Een proces dat de celcyclus wordt genoemd, laat een cel groeien, zijn DNA dupliceren en delen. Celdeling gebeurt via een ander proc
- Onderzoeken hoe antibioticaresistente bacteriën agressief worden
- Röntgenfoto's laten zien waarom zee-egels geen gemakkelijke prooi zijn
- Nu weten we waarom wortels oranje zijn
- Wat is clohrine?
- Hinderlaag in een petrischaal
- Wat zijn die microchips die mensen in hun honden stoppen?
- Als GGO-genen ontsnappen, hoe zullen de hybriden het dan doen?
- Het membraan in membraanloze organellen begrijpen
- Dansende materie:nieuwe vorm van beweging van cyclische macromoleculen ontdekt

- Peptide-hydrogels kunnen traumatisch hersenletsel helpen genezen

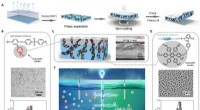
- Een efficiëntere op membraan gebaseerde generator voor het oogsten van osmotisch vermogen (update)
- Neutronen en röntgenstralen gebruiken om de veroudering van lithiumbatterijen te analyseren

 Een nieuwe lens op de wereld:de metalens verbeteren met vloeibaar kristal
Een nieuwe lens op de wereld:de metalens verbeteren met vloeibaar kristal Onderzoek laat zien wat er nodig is om een gigantische haai te zijn
Onderzoek laat zien wat er nodig is om een gigantische haai te zijn  Verschil tussen industriële smog en fotochemische smog
Verschil tussen industriële smog en fotochemische smog Microben onder het Groenlandse ijs kunnen een voorproefje zijn van wat wetenschappers op het oppervlak van Mars vinden
Microben onder het Groenlandse ijs kunnen een voorproefje zijn van wat wetenschappers op het oppervlak van Mars vinden  Hoe kunnen we de fotodegradatie van plastic versnellen?
Hoe kunnen we de fotodegradatie van plastic versnellen?  Franse wetgevers keuren 3% belasting op online reuzen goed
Franse wetgevers keuren 3% belasting op online reuzen goed Ontwikkeling van kern-schaal functionele composieten met uitstekende zelfsmerende eigenschappen
Ontwikkeling van kern-schaal functionele composieten met uitstekende zelfsmerende eigenschappen Hoe orgaantransplantaties werken
Hoe orgaantransplantaties werken
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

