
Wetenschap
Cellen construeren levende composietpolymeren voor biomedische toepassingen
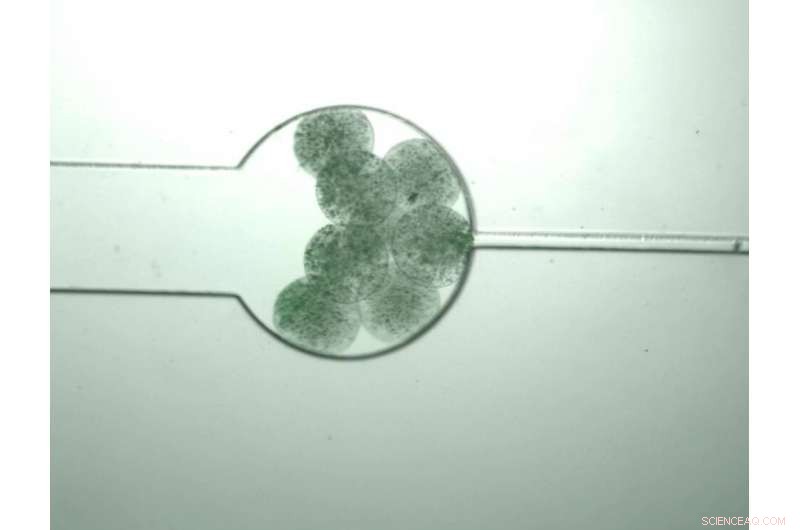
'Swarmbots, ' levende cellen die zijn ontworpen om monomeermoleculen te produceren, groeien totdat ze voelen dat hun bevolkingsdichtheid een bepaald niveau heeft bereikt, waarop ze openbarsten, waardoor de monomeren zich kunnen vermengen en zichzelf kunnen assembleren tot een composietpolymeer. Krediet:Zhuojun Dai
Biomedische ingenieurs aan de Duke University hebben aangetoond dat een klasse van verweven composietmaterialen die semi-interpenetrerende polymeernetwerken (sIPN's) worden genoemd, door levende cellen kan worden geproduceerd. De aanpak zou deze veelzijdige materialen biologisch meer compatibel kunnen maken voor biomedische toepassingen, zoals vertraagde medicijnafgiftesystemen.
Het onderzoek verschijnt 8 juni online in het tijdschrift Natuurcommunicatie .
Het concept van sIPN's bestaat al meer dan 100 jaar en wordt gebruikt in auto-onderdelen, medische apparatuur, vormmassa's en technische kunststoffen. Het algemene idee is dat een of meer polymeren zich zodanig rond een andere polymeersteiger assembleren dat ze in elkaar grijpen. Ook al zijn de polymeren niet chemisch gebonden, ze kunnen niet uit elkaar worden getrokken en vormen een nieuw materiaal met eigenschappen die groter zijn dan de simpele som der delen.
Traditionele methoden voor het vervaardigen van sIPN's omvatten doorgaans het produceren van de samenstellende delen die monomeren worden genoemd en deze onder de juiste chemische omstandigheden met elkaar te mengen om hun assemblage tot grote netwerken te regelen in een proces dat polymerisatie wordt genoemd.
"Als het werkt, het is een fantastisch platform dat verschillende functionaliteiten kan opnemen in de zelf-geassembleerde laag voor biomedische of milieutoepassingen, " zei Lingchong You, hoogleraar biomedische technologie aan Duke. "Maar het proces is vaak niet zo biocompatibel als je zou willen. Dus we dachten:waarom zouden we geen levende cellen gebruiken om de tweede laag te synthetiseren om het zo biocompatibel mogelijk te maken?"
In de nieuwe krant Zhuojun Dai, een voormalig postdoc in het You-lab die nu universitair hoofddocent is aan het Shenzhen Institute of Synthetic Biology, gebruikt daarvoor een platform dat het lab al enkele jaren ontwikkelt, 'swarmbots' genaamd.
De swarmbots zijn levende cellen die zijn geprogrammeerd om biologische moleculen binnen hun muren te produceren en vervolgens exploderen zodra hun populatie een bepaalde dichtheid bereikt. In dit geval, ze zijn geprogrammeerd om monomeren te produceren die elastine-achtige polypeptiden (ELP's) worden genoemd, gefuseerd met functionele kenmerken die SpyTag en SpyCatcher worden genoemd. Deze twee moleculaire structuren vormen een slot-en-sleutelsysteem, waardoor de ELP's zichzelf kunnen assembleren tot een polymeerketen wanneer ze worden gemengd. Naarmate ze groeien, deze polymeren verstrengelen zich met de polymere microcapsules die de cellen bevatten om sIPN's te vormen.
Elk monomeer kan meerdere SpyTags of SpyCatchers bevatten en kan ook worden gefuseerd met eiwitten die een uitlezing genereren of specifieke functies hebben. Het is net zoiets als het maken van een hek met kettingschakels van veel kleine bedelarmbanden die ruimte hebben voor sluitingen en bedels.
De onderzoekers programmeren eerst de cellen om deze toegankelijke functie te vullen met een fluorescerend eiwit om te bewijzen dat het systeem ze op hun plaats kan vergrendelen. Na die succesvolle demonstratie, ze richten hun aandacht op het ontwikkelen van een bruikbaar medicijnafgiftesysteem met hun nieuwe uitvinding.
"Je zou de fluorescerende marker kunnen vervangen door alles wat een functie heeft die je wilt laten zien, " zei You. "We hebben besloten om antibiotica aan te raken omdat het een van de andere aandachtspunten van ons laboratorium is."
Bèta-lactam antibiotica, zoals penicilline en zijn derivaten, behoren tot de meest gebruikte antibiotica ter wereld. Ze worden ook vaak te veel gebruikt en kunnen negatieve effecten hebben, zoals het vernietigen van het natuurlijke microbioom dat in onze ingewanden leeft.
Om één manier te demonstreren waarop hun nieuwe cel-gebouwde sIPN's nuttig zouden kunnen zijn, de onderzoekers vullen de accessorizable plek met beta-lactamase, die bètalactamantibiotica kunnen afbreken. Door de nieuw gefunctionaliseerde sIPN's in muizen te injecteren, de onderzoekers toonden aan dat het platform het anders kortstondige beschermende molecuul langzaam kon afgeven om de darmmicrobiomen van de muizen te helpen negatieve bijwerkingen van de antibiotica af te weren.
"Niemand heeft eerder levende cellen als fabriek gebruikt om in realtime monomeren te produceren voor sIPN's, " zei U. "De proof-of-principle demonstratie laat zien dat, niet alleen kunnen we dit soort functionele materialen fabriceren met levende cellen, maar ze kunnen medisch relevante functies vertonen."
 Wetenschappers ontwikkelen nieuwe aanpak om te voorspellen hoe vloeistoffen bevriezen
Wetenschappers ontwikkelen nieuwe aanpak om te voorspellen hoe vloeistoffen bevriezen Mengoplossingen in de kleinste reageerbuisjes ter wereld
Mengoplossingen in de kleinste reageerbuisjes ter wereld Uitzonderlijk efficiënte winning kan het beheer van nucleaire brandstof verbeteren
Uitzonderlijk efficiënte winning kan het beheer van nucleaire brandstof verbeteren Barsten in perovskietfilms voor zonnecellen zijn gemakkelijk te genezen, studie vondsten
Barsten in perovskietfilms voor zonnecellen zijn gemakkelijk te genezen, studie vondsten Een energiezuiniger katalytisch proces om olefinen te produceren
Een energiezuiniger katalytisch proces om olefinen te produceren
Hoofdlijnen
- Wat is de ergste uitsterving in de geschiedenis van de aarde?
- De functie van macromoleculen
- Wat bevindt zich aan de linkerkant van uw lichaam in menselijke anatomie?
- Sociale interacties hebben voorrang op genetica wanneer vogels nieuwe liedjes leren
- Hoe ribosomen het proteoom vormen
- Sterfgevallen chimpansees in Oeganda toegeschreven aan menselijk verkoudheidsvirus
- Wetenschappers volgen aseksuele kleine wormen - waarvan de afstamming 18 miljoen jaar teruggaat
- Studie:Grote witte haaien zwemmen steeds dieper
- Berekening van celconcentratie
- Onderzoekers rapporteren tweezijdige Janus-membraantoepassingen
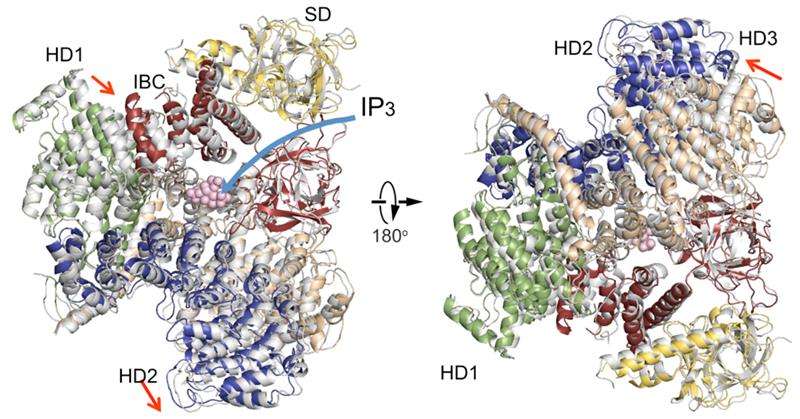
- Atoomstructuur onthult hoe cellen omgevingssignalen vertalen
- Niet zo snel:sommige batterijen kunnen te ver worden geduwd
- Efficiënte perovskiet-zonnecellen ontwikkeld door interface-gemedieerde recombinatie te verminderen
- Wat vertegenwoordigt het periodenummer?

 Waterflessen, andere gerecyclede 3D-printmaterialen kunnen problemen met militaire bevoorrading voorkomen
Waterflessen, andere gerecyclede 3D-printmaterialen kunnen problemen met militaire bevoorrading voorkomen Kwantumeffect veroorzaakt ongebruikelijke materiaaluitbreiding
Kwantumeffect veroorzaakt ongebruikelijke materiaaluitbreiding Hoe werkt het skelet met het ademhalingssysteem?
Hoe werkt het skelet met het ademhalingssysteem?  De begraven wetlands van de wereld terugbrengen uit de dood
De begraven wetlands van de wereld terugbrengen uit de dood Wat is een niet-lineaire relatie?
Wat is een niet-lineaire relatie?  De verschillende soorten lensdefecten
De verschillende soorten lensdefecten  Mijlpaal op weg naar het inschakelen van 's werelds grootste supergeleidende lineaire versneller
Mijlpaal op weg naar het inschakelen van 's werelds grootste supergeleidende lineaire versneller Experimenteel behandelregime effectief tegen hiv
Experimenteel behandelregime effectief tegen hiv
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com

