Wetenschap
Wat vertegenwoordigt het periodenummer?
Elementen in het periodiek systeem behoren tot groepen en periodes. De groepen van het periodiek systeem zijn de kolommen. De periodes van het periodiek systeem zijn de rijen.
TL; DR (te lang; niet gelezen)
Elementen van dezelfde periode delen hetzelfde hoofdkwantumnummer, dat zowel de grootte en energie van de buitenste elektronenschil van een atoom.
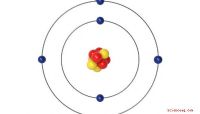
Elektronenschelpen
De elektronen van een atoom cirkelen rond de kern in een fuzzy wolk die wordt beheerst door waarschijnlijkheid. Het kan echter nuttig zijn om elektronenbanen te beschouwen als stijve omhulsels die een aantal verschillende mogelijke elektronenbanen bevatten. Naarmate het atoomnummer van een atoom toeneemt, moeten zijn omhulsels een toenemend aantal elektronen herbergen. De buitenste schaal wordt de valentieschaal genoemd; het periodegetal verwijst naar deze schaal.
Kwantumnummers
De lay-out van de mogelijke positie van een elektron in een atoom wordt bepaald door kwantumgetallen. Het hoofdkwantumgetal, n, komt overeen met de grootte en energie van elektronenschillen. Het kan niet-nul gehele getallen zijn: 1, 2, 3 enzovoort. Naarmate aantallen toenemen, nemen zowel de grootte als de energie van de elektronenschil toe. Het tweede kwantumgetal, l, komt overeen met de vorm van de orbitalen in een schaal. Deze nummers worden meestal aangeduid met hun overeenkomstige letters: 0 \u003d s, 1 \u003d p, 2 \u003d d en 3 \u003d f. De waarde van l kan variëren tussen nul en n-1. Als een elektron bijvoorbeeld een hoofdkwantumgetal van 2 heeft, kan het bestaan in een van twee verschillende orbitale vormen, s of p. Het derde kwantumgetal, m, komt overeen met de oriëntatie van de orbitalen. Het derde kwantumnummer moet altijd tussen -l en + l liggen. Daarom is er één s-orbitaal, drie p-orbitalen, vijf d-orbitalen en zeven f-orbitalen.
Elektronen toevoegen en over het periodiek systeem bewegen
Een enkel paar elektronen vult een orbitaal. Waterstof heeft één elektron, dus dat neemt de eerste baan in beslag: 1s. Helium heeft twee elektronen, die beide nog steeds in de 1s orbitaal passen. Het volgende element, lithium, heeft drie elektronen. De eerste twee passen in de 1s orbitaal. Het derde elektron moet echter in een nieuwe baan zijn. Het hoofdkwantumnummer 1 beperkt het tweede kwantumnummer tot nul, wat op zijn beurt betekent dat het derde ook nul moet zijn. Daarom wordt alle ruimte van de eerste schaal ingenomen. Het volgende elektron moet bestaan in een nieuwe schaal en orbitaal: de 2s orbitaal. Dit betekent dat het belangrijkste kwantumgetal is toegenomen; het element moet zich in een andere periode bevinden. Zoals verwacht begint lithium met groep 2 van het periodiek systeem, omdat de valentieschil een principaal kwantumgetal 2 heeft.
Atoomstraaltrends
Atomen veranderen de belangrijkste kwantumgetallen niet als u van links naar rechts beweegt over het periodiek systeem. Daarom bestaan de elektronen allemaal op ongeveer dezelfde afstand van de kern. Meer protonen worden echter toegevoegd. Dit creëert een grotere positieve lading in de kern, wat resulteert in een grotere inwendige aantrekkingskracht op elektronen. Daarom neemt de atomaire straal, of de afstand van de kern tot de buitenste rand van het atoom, af naarmate u een periode doorloopt. Aan de andere kant neemt het periodegetal toe naarmate u naar beneden beweegt in het periodiek systeem. Het belangrijkste kwantumgetal neemt toe en daarom wordt de elektronenwolk groter. Op zijn beurt neemt de atoomstraal toe naarmate je naar beneden beweegt in het periodiek systeem.
Hoofdlijnen
- Forensische wetenschapsprojecten voor middelbare scholieren
- DNA-onderzoekers roepen botverzamelaars op om toegang tot botten te delen
- Eerste Amerikaanse vrouw bevalt van getransplanteerde baarmoeder
- Functies van het bloedsomloopstelsel
- Gespecialiseerde cellen in het lichaam
- Wat doet ADP in de biologie?
- Wat is de rol van enzymen in het metabolisme?
- Is de Krebs-cyclus aëroob of anaëroob?
- Wat is het voordeel van het gebruik van vlekken om naar cellen te kijken?
 Voeten in miles omzetten
Voeten in miles omzetten Hoe de cumulatieve waarschijnlijkheden in SPSS berekenen
Hoe de cumulatieve waarschijnlijkheden in SPSS berekenen  Verschil tussen J20C & J20D vloeistof
Verschil tussen J20C & J20D vloeistof
Landbouwmachines, zoals tractoren, hebben specifieke oliën nodig om de bewegende tandwielassemblages van de transmissie goed te smeren. Trekkers die door John Deere zijn gefabriceerd, hebben transmissieoliën no
 Wie was de eerste archeoloog?
Wie was de eerste archeoloog?  Top 5 energiezuinige computers
Top 5 energiezuinige computers  Vier basiscomponenten van een ecosysteem
Vier basiscomponenten van een ecosysteem  Wie heeft eerst Viscositeit ontdekt?
Wie heeft eerst Viscositeit ontdekt?  Feiten over tropische regenwoudplanten
Feiten over tropische regenwoudplanten
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com