
Wetenschap
Probiotische hydrogels genezen darmwonden waar andere verbanden niet bij kunnen
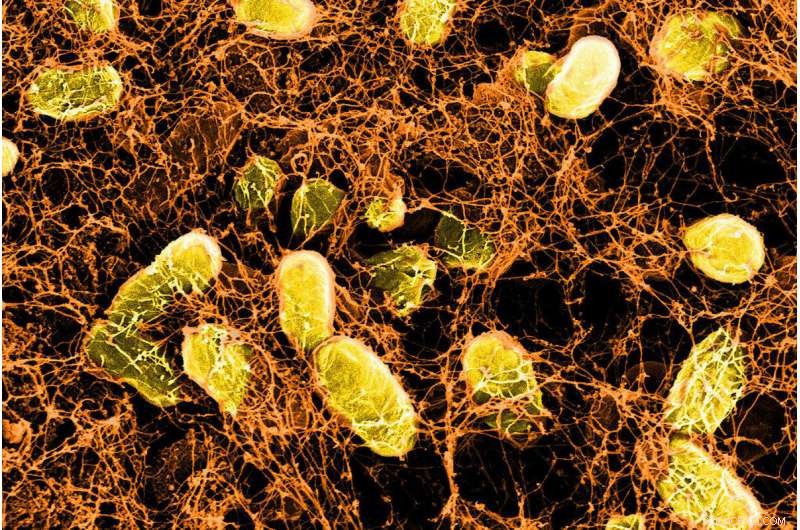
Microscopisch beeld van een bacteriële hydrogel die zich bindt aan slijmeiwitten op het oppervlak van de darmwand. Krediet:Wyss Institute aan de Harvard University
Externe wonden zoals snijwonden of schaafwonden kunnen vaak gemakkelijk worden afgedekt met een eenvoudige pleister of een grotere wondpleister om ze te beschermen en hun genezing te vergemakkelijken. Als het gaat om sommige interne oppervlakken zoals die van de darm die zijn bedekt met een slijmlaag, echter, dergelijke conventionele wondgenezende materialen zijn niet effectief omdat het slijm hun stevige aanhechting belemmert en ze snel wegvoert van de wondplaats.
Nutsvoorzieningen, onderzoekers van het Wyss Institute for Biologically Inspired Engineering van Harvard en de John A. Paulson School of Engineering and Applied Sciences (SEAS) hebben een oplossing voor dit probleem ontwikkeld in de vorm van probiotische hydrogels gemaakt van mucoadhesieve nanovezels en geproduceerd door een gemanipuleerde natuurlijke darmbacterie. De hydrogels kunnen gemakkelijk uit bacterieculturen worden geproduceerd en als zelfherstellende "levende gels" met een langere levensduur of "celvrije gels" met een kortere levensduur via injectiespuiten op het darmoppervlak worden aangebracht, spuiten, en endoscopische technieken om een afdichting te verschaffen. De studie is gepubliceerd in Geavanceerde materialen .
"Dit nieuwe type geconstrueerd levend materiaal met zijn gemak van productie en opslag, biocompatibiliteit, en mucoadhesieve eigenschappen kunnen een deuropener zijn voor bioactieve wondgenezingsstrategieën voor gebruik in het menselijke darmlumen, " zei Neel Joshi, die een kernfaculteitslid is bij het Wyss Institute en universitair hoofddocent bij SEAS. "We kunnen in wezen de normale nanovezel-producerende moleculaire machinerie van niet-pathogene" programmeren E coli om hydrogels te produceren die een viscositeit hebben die sterk lijkt op die van slijm, en met ingebouwde mucoadhesieve mogelijkheden; en hun modulariteit zou ons in staat kunnen stellen om ze af te stemmen op specifieke delen van het maagdarmkanaal met hun individuele slijmsamenstellingen en structuren."
Joshi's en andere laboratoria hebben eerder commensale stammen van E coli om biofilmvormende nanovezels af te scheiden, en als levende gieterijen voor de fabricage van geneesmiddelen, fijne chemicaliën, of stoffen die kunnen helpen bij milieusanering door het CsgA-eiwit te manipuleren dat de bacteriën afscheiden, die zichzelf assembleert tot curli-nanovezels in de extracellulaire omgeving. In deze eerdere toepassingen CsgA werd gemodificeerd om extra enzymatische of structurele functies mogelijk te maken, zoals de uitvoering van een chemische reactie die nodig is voor de synthese van een medicijn of chemische stof. Echter, curli op nanovezel gebaseerde materialen zijn tot nu toe niet ontwikkeld voor direct gebruik als therapieën.
"Het is bekend dat natuurlijk geproduceerde biofilms wondgenezingsprocessen belemmeren tot een punt waarop ze actief moeten worden beheerd door zorgverleners. We hebben in wezen een van de kernmachines gehackt die ze produceren met het langetermijndoel om precies het tegenovergestelde te doen , om materialen te produceren die wondgenezing kunnen ondersteunen in een omgeving die ontoegankelijk is voor andere materialen, " zei eerste auteur Anna Duraj-Thatte, die een postdoctoraal onderzoeker van de Graduate School of Arts and Sciences is in het team van Joshi.
Om de vorming van extracellulaire hydrogels mogelijk te maken, de onderzoekers programmeerden een niet-pathogene stam van de darmbacterie E coli om een variant van het CsgA curli-eiwit te synthetiseren dat is gefuseerd aan het slijmbindende domein van menselijke klaverbladfactoren (TFF's). TFF's worden mede uitgescheiden door slijmproducerende cellen om slijmvliesepitheel te beschermen tegen een reeks beledigingen, en hen helpen blessures te herstellen. Een eenvoudige filtratiestap maakt de schone scheiding van de levende bacteriënbevattende hydrogel van de rest van de cultuur mogelijk, terwijl de celvrije gels een extra stap vereisen waarin de bacteriën worden gedood met een eenvoudige chemische behandeling. "We denken dat de aanwezigheid van de TFF-domeinen verschillende curli-vezels in staat stelt om met elkaar te verknopen en een wateropslagmaas te vormen, en toonde aan dat de exacte hydrogeleigenschappen afhangen van het type TFF dat wordt gebruikt, ' zei Duraj Thatte.
In samenwerking met Jeffrey Karp en instructeur geneeskunde Yuhan Lee in Brigham and Women's Hospital, het team testte de specificiteit van weefseladhesie op basis van het type toegevoegde domeinen in de hydrogel. Toen TFF's op de hydrogels werden gepresenteerd, ze verbeterden de adhesie alleen aan het lumen-blootgestelde slijmvliesoppervlak van een weefselmonster van een geitencolon. Alternatief, when a domain binding to fibronectin protein—which is not found on the mucosa, but on the outward-facing serosal surface of the colon—the hydrogels instead preferentially stuck to the serosal side of the colon tissue sample.
"Since hydrogels with different TFF domains can be easily sprayed onto tissue surfaces with controllable adhesion and functional activity, we envision their potential use in endoscopic procedures to treat intestinal disorders, like a spray-on bandage, " said Karp, who is a professor of medicine at Brigham and Women's Hospital and Harvard Medical School.
When given orally to mice, the cell-containing live gels could withstand the harsh pH and digestive conditions of the stomach and small intestine to reach the cecum with the bacteria intact. The team also found that hydrogels bearing one particular TFF domain (TFF2) enhanced retention of the material in the colon. "The presence of bacteria in live gels prolonged their residency times in the gut from one day to at least five days due to the bacteria's ability to continuously regenerate the curli fiber networks that are decorated with TFFs, without affecting the health of mice in any obvious way, " said Joshi.
"This is a great example of synthetic biology-based jujutsu in which Joshi's team took a major problem created by bacteria—the biofilms they create that are so difficult to access and remove—and then flipped the problem on its head through genetic engineering so that the biofilm now essentially becomes a healing Band-aid for our gut. It's an amazing example of biologically inspired engineering at its best, " said Wyss Director Donald Ingber, the Judah Folkman Professor of Vascular Biology at HMS and the Vascular Biology Program at Boston Children's Hospital, as well as professor of bioengineering at SEAS.
Dit verhaal is gepubliceerd met dank aan de Harvard Gazette, De officiële krant van Harvard University. Voor aanvullend universiteitsnieuws, bezoek Harvard.edu.
 Assemblage van fluctuerende moleculen in kunstmatig celmembraan
Assemblage van fluctuerende moleculen in kunstmatig celmembraan Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal
Dynamiek van zijde-eiwitten is de sleutel tot uitstekende stabiliteit van spinzijde als biomateriaal Onderzoekers verkrijgen nieuwe resultaten over diëlektrische recombinatie-precisiespectroscopie
Onderzoekers verkrijgen nieuwe resultaten over diëlektrische recombinatie-precisiespectroscopie Wat is het verschil tussen zuivere stoffen en mengsels?
Wat is het verschil tussen zuivere stoffen en mengsels?  Warmtebehandeling kan chemotherapie effectiever maken
Warmtebehandeling kan chemotherapie effectiever maken
 Studie maakt gebruik van satellietgegevens om wijdverbreide affakkeling van de olie-industrie te lokaliseren
Studie maakt gebruik van satellietgegevens om wijdverbreide affakkeling van de olie-industrie te lokaliseren Waardoor wordt algenbloei giftig?
Waardoor wordt algenbloei giftig? NASA's Terra-satelliet legt de vulkanische aswolk van La Soufrière vast in 3D
NASA's Terra-satelliet legt de vulkanische aswolk van La Soufrière vast in 3D Studie vindt directe verbanden tussen oude koolstof, grafiet en hydrothermale ventilatieopeningen op de zeebodem
Studie vindt directe verbanden tussen oude koolstof, grafiet en hydrothermale ventilatieopeningen op de zeebodem Geen manier om explosie in chemische fabriek in Texas te voorkomen
Geen manier om explosie in chemische fabriek in Texas te voorkomen
Hoofdlijnen
- Typen cellijnen
- Jagen op ooien met dikhoornschapen zou meer trofeerammen kunnen opleveren
- Entomoloog ontdekt ongewervelde dieren die in meer kleurencombinaties voorkomen dan alle andere
- Welke soorten cellen zijn bacteriën?
- Kevers felle kleuren gebruikt voor camouflage in plaats van roofdieren te waarschuwen
- Hoe converteert ADP naar ATP?
- Dansgerelateerde wetenschapsprojecten
- Wat zijn drie primaire doelen van mitose?
- Ideeën voor het maken van een 3D-model van een cel
- Gekleurd borduurgaren op aanvraag bespaart tijd, geld en het milieu

- Minder zout, meer eiwit:aanpak van zuivelverwerking, milieu, duurzaamheidskwesties
- Nieuwe kijk op vreemde gaten die te maken hebben met smaak, Alzheimer, astma
- Watermoleculen gebruiken om elektrische activiteit in lipidemembranen te lezen

- Plastic-etende enzymcocktail luidt nieuwe hoop in voor plastic afval

 Honden snuffelden vroeger aan zeldzame soorten
Honden snuffelden vroeger aan zeldzame soorten Neuron en synaps-mimetische spintronica-apparaten ontwikkeld
Neuron en synaps-mimetische spintronica-apparaten ontwikkeld Hoe bomen naast elkaar bestaan:nieuwe bevindingen uit onderzoek naar biodiversiteit
Hoe bomen naast elkaar bestaan:nieuwe bevindingen uit onderzoek naar biodiversiteit Inflexibeler dan gedacht
Inflexibeler dan gedacht Australië biedt geld voor reddingsideeën Great Barrier Reef
Australië biedt geld voor reddingsideeën Great Barrier Reef Ryanair koopt startup Malta Air om zich te richten op Afrikaanse markten
Ryanair koopt startup Malta Air om zich te richten op Afrikaanse markten Sociale uitgaven aan kinderen leveren de meeste waar voor je geld op
Sociale uitgaven aan kinderen leveren de meeste waar voor je geld op De COVID-19-crisis gebruiken om kinderen te leren over voedsel en klimaatverandering
De COVID-19-crisis gebruiken om kinderen te leren over voedsel en klimaatverandering
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

