
Wetenschap
Chiraliteitsinversie in een spiraalvormig molecuul bij gecontroleerde snelheden
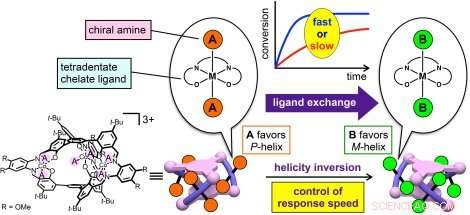
Schema 1 uit de krant. Krediet:Kanazawa University
Een strategie om de chiraliteit van een metaalbevattend spiraalvormig molecuul om te keren dat de snelheid van de respons regelt, wordt gerapporteerd in Chemistry, Een European Journal door onderzoekers van Kanazawa University.
Chirale moleculen kunnen niet worden gesuperponeerd op hun spiegelbeelden - zoals handen. De twee spiegelbeelden van een molecuul, een rechtshandige, de andere linkshandig, worden enantiomeren genoemd. De meeste moleculen die in medicijnen worden gebruikt, zijn chiraal, en slechts één enantiomeer is effectief (de andere kan zelfs giftig zijn), dus het kunnen controleren en manipuleren van de chiraliteit van moleculen is van het grootste belang voor een breed scala aan toepassingen.
Sommige moleculen kunnen een chiraliteitsverandering ondergaan als reactie op externe stimuli. Vooral, dynamische spiraalvormige moleculen, die in een dynamisch evenwicht zijn tussen de rechts- en linkshandige vormen, is aangetoond dat chiraliteit verandert bij blootstelling aan licht, warmte, redoxreacties, veranderingen in pH of binding met andere moleculen, bijvoorbeeld door organische moleculen in te voegen in het metaalcentrum van het spiraalvormige complex. Echter, deze laatste optie is moeilijk te implementeren en er zijn tot nu toe zeer weinig succesvolle gevallen gemeld.
Shigehisa Akine van de Universiteit van Kanazawa, in Japan, en collega's presenteren nu een spiraalvormig complex (een spiraalvormig kobalt (III) metallocryptand) waarin helixveranderingen kunnen worden geactiveerd door een verscheidenheid aan organische moleculen in de spiraalvormige structuur te introduceren. Door het ene ligand te vervangen door een geschikt ander ligand, de helix kan worden omgekeerd, en de snelheid van de verandering kan worden gecontroleerd door de reactiviteit van de liganden, wat in de praktijk veel eenvoudiger is dan wat in andere protocollen wordt voorgesteld.
Het door de auteurs gepresenteerde molecuul heeft een goed gedefinieerde drievoudige spiraalvormige structuur, en zes amineliganden die zijn gecoördineerd met drie octaëdrische kobalt(III)-centra. Kobalt(III)-ionen vormen normaal gesproken inerte complexen en ondergaan geen liganduitwisseling, maar de kobalt(III)-ionen in deze helixstructuur bleken liganduitwisseling tussen aminen te ondergaan. De auteurs toonden de afhankelijkheid van de responssnelheid aan van de combinatie van chirale en achirale amines als start- en binnenkomende liganden, respectievelijk, als gevolg van het verschil in de reactiviteit van de Co-bevattende groepen. Verschillende combinaties van amines werden getest, en verschillende chirale aminen bleken tegengestelde helicities te stabiliseren.

Voorblad van Chem. EUR. J. 10.1002/chem.201900297 met het onderzoek van Shigehisa Akine et al. dat in dit nummer wordt gepubliceerd. Krediet:Kanazawa University
"Wij geloven dat deze resultaten de weg zullen openen voor de ontwikkeling van nieuwe functionele materialen waarin de reactiesnelheden kunnen worden gecontroleerd en de gewenste functie in de tijd programmeerbaar is met behulp van een geschikte chemische stimulus, ", zeggen de auteurs.
chirale moleculen
Veel biologische moleculen zijn chiraal:voorbeelden zijn DNA en suikers. Twee moleculen met tegengestelde chiraliteit, twee enantiomeren, exact dezelfde samenstelling en functionele structuur hebben, maar vormen die spiegelbeelden van elkaar zijn. Ze hebben afzonderlijk dezelfde fysische en chemische eigenschappen, maar niet wanneer ze interageren met andere chirale moleculen. Om nog niet begrepen redenen, alle natuurlijk voorkomende aminozuren hebben chiraliteit verlaten, dus de menselijke biochemie is chiraliteitsspecifiek, dus we reageren anders, bijvoorbeeld, aan de twee enantiomeren van een geneesmiddel. Van sommige chirale moleculen wordt zelfs waargenomen dat ze heel verschillende geuren hebben.
Aminen
Aminen zijn verbindingen die een stikstofatoom en een eenzaam elektronenpaar bevatten. Aminozuren zijn een prominent voorbeeld van moleculen die amines bevatten. Amines vinden toepassingen in veel verschillende instellingen, inclusief het maken van rubbers, kleurstoffen en medicijnen. Sommige aminen staan bekend als goede liganden voor overgangsmetalen om coördinatieverbindingen te geven.
 Riskante goudkoorts:Indonesië pakt illegale mijnbouw aan
Riskante goudkoorts:Indonesië pakt illegale mijnbouw aan Een timmermansbijtje vinden
Een timmermansbijtje vinden Gepensioneerde booreilanden voor de kust van Californië kunnen een nieuw leven vinden als kunstmatige riffen
Gepensioneerde booreilanden voor de kust van Californië kunnen een nieuw leven vinden als kunstmatige riffen Waar komt de zware luchtvervuiling in Peking vandaan?
Waar komt de zware luchtvervuiling in Peking vandaan? Overheden kunnen niet worden vertrouwd om welzijnsnormen voor kippen te leveren
Overheden kunnen niet worden vertrouwd om welzijnsnormen voor kippen te leveren
Hoofdlijnen
- Research Paper Topics in Biochemistry
- Kan iemand zich herinneren dat hij geboren is?
- Begrijpen? Je hersensignalen zullen het vertellen
- Gezondheidsonderzoekers visualiseren een leven in silico
- Hoe een onbekende bacterie in de microbiologie te identificeren
- Anatomische structuren: homoloog, analoog & vestigiaal
- Overeenkomsten van mitose en meiose
- Robotapparaat volgt plantengroei op cellulair niveau
- Misplaatste monarchen:clusters van vlinders in het noorden
- CRISPR's groeipijnen

- Hoe gemeenschappelijke elementen een meer energiezekere toekomst kunnen maken

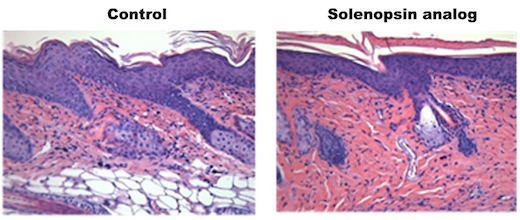
- Vuurmierengifverbindingen kunnen leiden tot huidbehandelingen
- Wetenschappers ontwikkelen katalysator om ethanol om te zetten in hoogwaardige chemicaliën en brandstoffen

- Krachtige nieuwe beeldvormingsmethode onthult in detail hoe deeltjes in oplossing bewegen
 Kleine micro-aardbevingen maken grondwater zuur
Kleine micro-aardbevingen maken grondwater zuur Vergeet joysticks - gebruik je romp om drones te besturen
Vergeet joysticks - gebruik je romp om drones te besturen Zelfgerolde buizen maken miniatuurelektronica
Zelfgerolde buizen maken miniatuurelektronica Mensen gaan ervan uit dat ze immuun zijn voor de dynamiek van sociale netwerken, maar andere mensen niet
Mensen gaan ervan uit dat ze immuun zijn voor de dynamiek van sociale netwerken, maar andere mensen niet Elektronen aan de rand:het verhaal van een intrinsieke magnetische topologische isolator
Elektronen aan de rand:het verhaal van een intrinsieke magnetische topologische isolator Het verlaten van flatland - quantum Hall-fysica in 4-D
Het verlaten van flatland - quantum Hall-fysica in 4-D March Madness 2019: What I Questioned, Loved and Learned
March Madness 2019: What I Questioned, Loved and Learned  Nieuwe warme Neptunus exoplaneet ontdekt
Nieuwe warme Neptunus exoplaneet ontdekt
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

