
Wetenschap
Chemici ontdekken onverwachte enzymstructuur
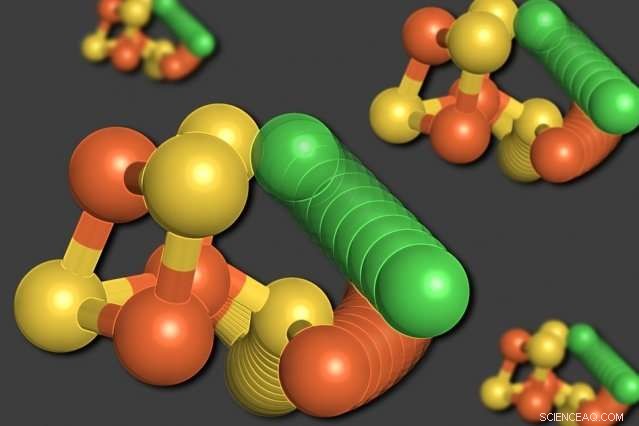
MIT-onderzoekers hebben aangetoond dat sommige atomen in een enzym dat koolmonoxidedehydrogenase wordt genoemd, zichzelf kunnen herschikken wanneer het zuurstofniveau laag is. Een nikkelatoom (groen) verlaat de kubusachtige structuur, het verplaatsen van een ijzeratoom (oranje). Een zwavelatoom (geel) beweegt ook uit de kubus. Krediet:Elizabeth Wittenborn
Veel microben hebben een enzym dat kooldioxide kan omzetten in koolmonoxide. Deze reactie is van cruciaal belang voor het bouwen van koolstofverbindingen en het opwekken van energie, vooral voor bacteriën die in zuurstofvrije omgevingen leven.
Dit enzym is ook van groot belang voor onderzoekers die nieuwe manieren willen vinden om broeikasgassen uit de atmosfeer te verwijderen en om te zetten in bruikbare koolstofhoudende verbindingen. De huidige industriële methoden voor het omzetten van kooldioxide zijn zeer energie-intensief.
"Er zijn industriële processen die deze reacties uitvoeren bij hoge temperaturen en hoge drukken, en dan is er nog een enzym dat hetzelfde kan doen bij kamertemperatuur, " zegt Catherine Drennan, een MIT hoogleraar scheikunde en biologie en een Howard Hughes Medical Institute Investigator. "Voor een lange tijd, mensen zijn geïnteresseerd in het begrijpen hoe de natuur deze uitdagende chemie uitvoert met deze assemblage van metalen."
Drennan en haar collega's van het MIT, Brandeis-universiteit, en de universiteit van Aix-Marseille in Frankrijk hebben nu een uniek aspect ontdekt van de structuur van de "C-cluster" - de verzameling metaal- en zwavelatomen die het hart vormt van het enzym koolmonoxidedehydrogenase (CODH). In plaats van een starre steiger te vormen, zoals verwacht, het cluster kan de configuratie daadwerkelijk wijzigen.
"Het was niet wat we verwachtten te zien, " zegt Elizabeth Wittenborn, een recente MIT Ph.D. ontvanger en de hoofdauteur van de studie, die verschijnt in het nummer van 2 oktober van het tijdschrift eLife .
Een moleculair radslagwiel
Metaalbevattende clusters zoals de C-cluster voeren vele andere kritische reacties uit in microben, inclusief het splitsen van stikstofgas, die moeilijk industrieel te repliceren zijn.
Drennan begon ongeveer 20 jaar geleden met het bestuderen van de structuur van koolmonoxidedehydrogenase en de C-cluster, kort nadat ze haar lab aan het MIT begon. Zij en een andere onderzoeksgroep bedachten elk een structuur voor het enzym met behulp van röntgenkristallografie, maar de structuren waren niet helemaal hetzelfde. De verschillen werden uiteindelijk opgelost en men dacht dat de structuur van CODH goed ingeburgerd was.
Wittenborn nam het project een paar jaar geleden op, in de hoop te achterhalen waarom het enzym zo gevoelig is voor inactivatie door zuurstof en te bepalen hoe het C-cluster in elkaar zit.
Tot verbazing van de onderzoekers hun analyse onthulde twee verschillende structuren voor de C-cluster. De eerste was een opstelling die ze hadden verwacht te zien - een kubus bestaande uit vier zwavelatomen, drie ijzeratomen, en een nikkelatoom, met een vierde ijzeratoom verbonden met de kubus.
In de tweede structuur echter, het nikkelatoom wordt uit de kubusachtige structuur verwijderd en neemt de plaats in van het vierde ijzeratoom. Het verplaatste ijzeratoom bindt zich aan een nabijgelegen aminozuur, cysteïne, die het op zijn nieuwe locatie houdt. Een van de zwavelatomen beweegt ook uit de kubus. Al deze bewegingen lijken samen te gebeuren, in een beweging beschrijven de onderzoekers als een 'moleculair radslagwiel'.
"De zwavel, het ijzer, en het nikkel verhuizen allemaal naar nieuwe locaties, Drennan zegt. "We waren echt geschrokken. We dachten dat we dit enzym begrepen, maar we ontdekten dat het deze ongelooflijk dramatische beweging doet die we nooit hadden verwacht. Toen kwamen we met meer bewijs dat dit eigenlijk iets is dat relevant en belangrijk is - het is niet zomaar een toevalstreffer, maar maakt deel uit van het ontwerp van dit cluster."
De onderzoekers geloven dat deze beweging, die optreedt bij blootstelling aan zuurstof, helpt het cluster te beschermen tegen volledig en onomkeerbaar uiteenvallen als reactie op zuurstof.
"Het lijkt alsof dit een vangnet is, waardoor de metalen kunnen worden verplaatst naar locaties waar ze veiliger zijn voor het eiwit, ' zegt Drennan.
Douglas Rees, een professor in de chemie aan Caltech, beschreef het artikel als "een prachtige studie van een fascinerend clusterconversieproces."
"Deze clusters hebben mineraalachtige kenmerken en men zou kunnen denken dat ze zo stabiel als een rots zouden zijn, ' zegt Rees, die niet bij het onderzoek betrokken was. "In plaats daarvan, de clusters kunnen dynamisch zijn, die hen eigenschappen verleent die cruciaal zijn voor hun functie in een biologische omgeving."
Geen starre steiger
Dit is de grootste metaalverschuiving die ooit is waargenomen in een enzymcluster, maar kleinere herschikkingen zijn gezien in sommige anderen, waaronder een metaalcluster gevonden in het enzym stikstofase, die stikstofgas omzet in ammoniak.
"Vroeger, mensen dachten dat deze clusters in werkelijkheid deze starre steigers waren, maar de laatste paar jaar komt er steeds meer bewijs dat ze niet echt rigide zijn, ' zegt Drennan.
De onderzoekers proberen nu te achterhalen hoe cellen deze clusters samenstellen. Meer informatie over hoe deze clusters werken, hoe ze zijn samengesteld, en hoe ze door zuurstof worden beïnvloed, zou wetenschappers kunnen helpen die hun actie proberen te kopiëren voor industrieel gebruik, zegt Drennan. Er is veel belangstelling voor het bedenken van manieren om de accumulatie van broeikasgassen tegen te gaan door, bijvoorbeeld, kooldioxide omzetten in koolmonoxide en vervolgens in acetaat, die kan worden gebruikt als bouwsteen voor vele soorten bruikbare koolstofhoudende verbindingen.
"Het is ingewikkelder dan mensen dachten. Als we het begrijpen, dan hebben we een veel betere kans om het biologische systeem echt na te bootsen, ' zegt Drennan.
Dit verhaal is opnieuw gepubliceerd met dank aan MIT News (web.mit.edu/newsoffice/), een populaire site met nieuws over MIT-onderzoek, innovatie en onderwijs.
 Nieuwe grieptest gemakkelijk als ademen, met sneller resultaat
Nieuwe grieptest gemakkelijk als ademen, met sneller resultaat Hoe Mole Fractions te berekenen met behulp van massapercentage
Hoe Mole Fractions te berekenen met behulp van massapercentage  Het maken van nepvlees roept vragen op over de gezondheid, ethiek en duurzaamheid voor een voormalige slager
Het maken van nepvlees roept vragen op over de gezondheid, ethiek en duurzaamheid voor een voormalige slager Nieuw geavanceerd materiaal vertoont buitengewone stabiliteit over een breed temperatuurbereik
Nieuw geavanceerd materiaal vertoont buitengewone stabiliteit over een breed temperatuurbereik Hoe veroorzaakt verdamping afkoeling?
Hoe veroorzaakt verdamping afkoeling?
 Opruimduiken, recycling:Libanezen reageren op afvalcrisis
Opruimduiken, recycling:Libanezen reageren op afvalcrisis Verborgen geheimen in steen geschreven:Hallett Cove decoderen met virtual reality
Verborgen geheimen in steen geschreven:Hallett Cove decoderen met virtual reality Voedselkeuzes van consumenten kunnen de uitstoot van broeikasgassen helpen verminderen en bijdragen aan klimaatverandering
Voedselkeuzes van consumenten kunnen de uitstoot van broeikasgassen helpen verminderen en bijdragen aan klimaatverandering Bewijs voor een enorme paleo-tsunami in het oude Tel Dor, Israël
Bewijs voor een enorme paleo-tsunami in het oude Tel Dor, Israël Sterke aardbeving treft eilandketen voor Nieuw-Zeeland; geen tsunami
Sterke aardbeving treft eilandketen voor Nieuw-Zeeland; geen tsunami
Hoofdlijnen
- Wetenschappers visualiseren de structuur van de belangrijkste DNA-reparatiecomponent met een bijna-atomaire resolutie
- Middeleeuwse kist levert fascinerend skelet op
- De genetica van Biracial-kenmerken
- Sorry,
- Hoe werkt ureum denatureiwitten?
- Taxonomie (biologie): definitie, classificatie en voorbeelden
- Jacht op herten beperkt in westelijke Amerikaanse staten na strenge winter
- Een RNA TREAT voor Halloween
- Hoe verschillen schimmelsporen van bacteriële endosporen?
- Slimme truc maakt 20 keer snellere beeldvorming mogelijk met elektronenmicroscopie
- Technieken voor het observeren van beton terwijl het hard wordt, kunnen de ontwikkeling van nieuw cement vergemakkelijken

- Huidgel laat wonden genezen zonder een litteken achter te laten

- Kristallisatie kristalhelder gemaakt

- Lieve schat, Ik heb de celcultuur gekrompen

 Stralend met het licht van miljoenen zonnen
Stralend met het licht van miljoenen zonnen Toekomstige opties voor het opslaan van koolstofdioxide:Synthese van anorganische heteroalkenen
Toekomstige opties voor het opslaan van koolstofdioxide:Synthese van anorganische heteroalkenen Hoe speciale systemen in Algebra op te lossen
Hoe speciale systemen in Algebra op te lossen  Functie van T-cellen in de Thymus Gland
Functie van T-cellen in de Thymus Gland Toegankelijke stages ondersteunen gelijkheid en diversiteit in techniek
Toegankelijke stages ondersteunen gelijkheid en diversiteit in techniek Californië wildvuur ontploft, brandend over 25 mijl in dag
Californië wildvuur ontploft, brandend over 25 mijl in dag NASA-NOAA-satelliet helpt Teddy te bevestigen dat het nu een tropische storm is die record zet
NASA-NOAA-satelliet helpt Teddy te bevestigen dat het nu een tropische storm is die record zet Nanomagneten voor toekomstige gegevensopslag
Nanomagneten voor toekomstige gegevensopslag
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | Italian |

-
Wetenschap © https://nl.scienceaq.com

