
Wetenschap
Neteldieren controleren bacteriën op afstand
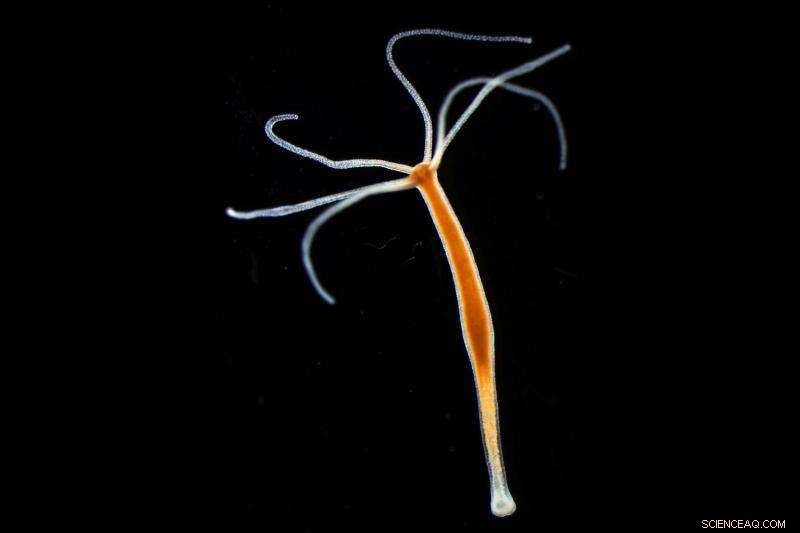
De zoetwaterpoliep Hydra. Krediet:Dr. Sebastian Fraune
In de moderne levenswetenschappen een paradigmaverschuiving wordt steeds duidelijker:levensvormen worden niet langer beschouwd als op zichzelf staande eenheden, maar in plaats daarvan zeer complexe en functioneel onderling afhankelijke gemeenschappen van organismen. De verkenning van de nauwe banden tussen meercellig en vooral bacterieel leven zal, in de toekomst, de sleutel zijn tot een beter begrip van levensprocessen als geheel, en in het bijzonder de overgang tussen gezondheid en ziekte. Echter, hoe de samenwerking en communicatie van de organismen in detail werkt, is op dit moment nog grotendeels onbekend. Een belangrijke stap voorwaarts in het ontcijferen van deze relaties tussen meerdere organismen is nu gemaakt door onderzoekers van de Cell and Developmental Biology-werkgroep van het Zoölogisch Instituut van de Universiteit van Kiel:de wetenschappers, geleid door Dr. Sebastian Fraune, voor het eerst hebben kunnen bewijzen dat gastheerorganismen niet alleen de samenstelling van hun koloniserende bacteriën kunnen controleren, maar ook hun functie. De CAU-onderzoekers publiceerden hun baanbrekende bevindingen - afgeleid van het voorbeeld van de zoetwaterpoliep Hydra en hun specifieke bacteriële symbionten - afgelopen maandag in het nieuwste nummer van het wetenschappelijke tijdschrift Proceedings van de National Academy of Sciences .
"Het startpunt van ons onderzoek was de observatie dat Hydra de samenstelling van soortspecifieke bacteriële kolonisatie kan beïnvloeden, door de vorming van bepaalde antimicrobiële stoffen, " verklaarde Dr. Cleo Pietschke, hoofdauteur van de studie. In principe, deze eenvoudige levensvormen vervullen daarbij dezelfde taak die hoger ontwikkelde organismen ook moeten volbrengen om een gezond microbioom tot stand te brengen:met behulp van hun immuunsysteem, ze zorgen voor kolonisatie door de "juiste" samenstelling van bacteriën, en moet tegelijkertijd voorkomen dat nuttige micro-organismen een schadelijk effect hebben. Het gepresenteerde werk was gericht op hoe dit kolonisatieproces wordt ondersteund door de communicatie tussen gastheer en bacteriën.
Zodra een bepaalde bevolkingsdichtheid is bereikt, bacteriële gemeenschappen kunnen samenwerken in teams, om bepaalde functies te vervullen. De coördinatie van deze functies is gebaseerd op een sensormechanisme, waarmee de individuele bacteriën met behulp van signaalmoleculen de totale bevolkingsdichtheid kunnen bepalen. Zodra een drempelwaarde is bereikt, deze signaalmoleculen activeren genen, en daardoor bepaalde cellulaire functies reguleren. Met behulp van dit proces, bekend als quorum sensing, bacteriën controleren functies zoals de kolonisatie van oppervlakken, of de productie van toxines.
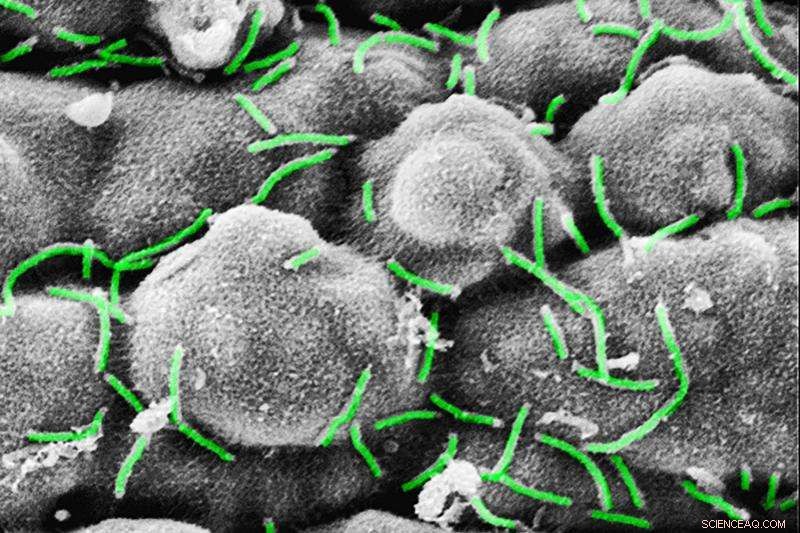
Elektronenmicroscopisch beeld van de bacteriële gemeenschappen (Curvibacter sp.) op het oppervlak van Hydra. Credit:Katja Schröder
Het onderzoeksteam van Kiel heeft nu aangetoond dat het gastheerorganisme het quorumdetectiemechanisme van de bacteriën kan veranderen. De neteldieren beïnvloeden daardoor direct de bacteriële signaalmoleculen, en zo het kolonisatieproces van hun eigen weefsel actief te bevorderen. "We hebben ontdekt dat Hydra niet alleen de aanwezigheid van hun bacteriële symbionten beïnvloedt, maar kan ook direct interfereren met hun functie, " benadrukte Fraune, onderzoeksmedewerker in de werkgroep Cel- en Ontwikkelingsbiologie. Het onderzoeksteam beschreef in detail, Voor de eerste keer, een gastheer die quorumquenching gebruikt om de moleculaire communicatie van bacteriën te remmen. Voorheen waren er slechts twee andere voorbeelden van dergelijke interventies door een gastheerorganisme. specifiek, de Kiel-onderzoekers bewezen dat een wijziging van bepaalde signaalmoleculen door de gastheer kolonisatie door Curvibacter bevordert, de meest voorkomende bacteriën geassocieerd met Hydra.
De CAU-onderzoekers bestudeerden de invloed van het gastheermechanisme op de bacteriële gemeenschap door het effect van een signaalmolecuul en zijn door de gastheer gemodificeerde bacteriële tegenhanger te observeren. Ten eerste, ze brachten kiemvrije Hydra mee, d.w.z. in het laboratorium gekweekte organismen zonder bacteriële kolonisatie, in contact komen met Curvibacter-bacteriën. Het was duidelijk dat de bacteriële kolonisatie slecht was, zolang niet-gemodificeerde signaalmoleculen aanwezig waren. Zodra deze door de invloed van het gastheerorganisme werden gewijzigd, de bacteriën koloniseerden het lichaam van de neteldieren in normale mate. De onderzoekers herhaalden het experiment vervolgens met organismen die al bacteriële kolonisatie vertoonden. Hier kwam hetzelfde patroon naar voren, ook:alleen de door de gastheer gemodificeerde signaalmoleculen stimuleerden consistente en typische kolonisatie van de Hydra door hun bacteriële symbionten. Verdere studies zijn nodig om te bepalen hoe deze resultaten, verkregen uit cnidarian modelorganismen, kan worden toegepast op andere levensvormen. Echter, aangezien Hydra primitieve evolutionaire organismen zijn, het is waarschijnlijk dat dit mechanisme ook op dezelfde manier aanwezig is in hoogontwikkelde organismen.
"Op het raakvlak tussen fundamenteel onderzoek en geneeskunde, het wordt steeds duidelijker dat de sleutel tot gezondheid ligt in de balans tussen het lichaam en bacteriële symbionten. In de toekomst hebben we de uitdagende taak om de zeer complexe relaties tussen gastheren en bacteriën te begrijpen. Met onze nieuwe bevindingen, we zijn een kleine stap dichter bij het bereiken van dit, ’ zei een optimistische Fraune.
 Wetenschappers ontdekken belangrijke oorzaak van resistentie in vaste elektrolyten
Wetenschappers ontdekken belangrijke oorzaak van resistentie in vaste elektrolyten Nieuwe aanpak stimuleert bacteriën om potentiële antibiotica te produceren, antiparasitaire verbindingen
Nieuwe aanpak stimuleert bacteriën om potentiële antibiotica te produceren, antiparasitaire verbindingen Bevestiging van de stamboom van uraniumkubussen van het mislukte nucleaire programma van nazi-Duitsland
Bevestiging van de stamboom van uraniumkubussen van het mislukte nucleaire programma van nazi-Duitsland Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren
Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren Nylons Eigenschappen & Gebruik
Nylons Eigenschappen & Gebruik
 Wat zijn de wintermoessons?
Wat zijn de wintermoessons?  Orka's:waarom orka's van meer dan de helft van de wereld worden bedreigd door overgebleven industriële chemicaliën
Orka's:waarom orka's van meer dan de helft van de wereld worden bedreigd door overgebleven industriële chemicaliën Ongebruikte bron, of de dreiging van broeikasgassen, gevonden onder de rifting-as voor de kust van Okinawa
Ongebruikte bron, of de dreiging van broeikasgassen, gevonden onder de rifting-as voor de kust van Okinawa Op welke boom groeien eikels?
Op welke boom groeien eikels?  De vorming van steenkool veranderde onze planeet bijna in een sneeuwbal
De vorming van steenkool veranderde onze planeet bijna in een sneeuwbal
Hoofdlijnen
- Verander je geliefde in een boom met Bios Urn
- Ademhaling bij zoogdieren
- Selenium zou de sleutel kunnen zijn tot het mysterie van kribbebijten bij paarden
- Zwavelademhaling bij zoogdieren
- Hoe erg is zwarte schimmel,
- Wat is een zuivere eigenschap en een hybride eigenschap?
- Op zoek naar het CRISPR Zwitsers zakmes
- Welke organellen zouden gevonden kunnen worden in een cel die zowel eukaryoot als autotroof was?
- Zijn mensen het slimste dier?
 Verticale pensioneringsdorpen zijn in opkomst, en ze zijn ook hightech
Verticale pensioneringsdorpen zijn in opkomst, en ze zijn ook hightech Wat is de Verzengende Zone?
Wat is de Verzengende Zone?
De verzengende zone verwijst naar het gebied van de aarde nabij de evenaar. Zoals de naam al doet vermoeden, is de verzengende zone over het algemeen warm. Het heeft een nat en droog seizoen, maar ervaart niet de vier se
 Bosbrandrook is slecht voor je ogen, ook - hier kun je ze beschermen
Bosbrandrook is slecht voor je ogen, ook - hier kun je ze beschermen Sniff-cam om ziekte op te sporen
Sniff-cam om ziekte op te sporen Gedachten aan God maken op angst gebaseerde reclame minder effectief
Gedachten aan God maken op angst gebaseerde reclame minder effectief Nieuw bewijs voor donkere materie maakt het nog exotischer
Nieuw bewijs voor donkere materie maakt het nog exotischer Alomtegenwoordige effecten van menselijke impact op het landschap van Engeland onthuld
Alomtegenwoordige effecten van menselijke impact op het landschap van Engeland onthuld De ontdekking van een nieuw type supernova verlicht een middeleeuws mysterie
De ontdekking van een nieuw type supernova verlicht een middeleeuws mysterie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com






