
Wetenschap
Op zoek naar het CRISPR Zwitsers zakmes
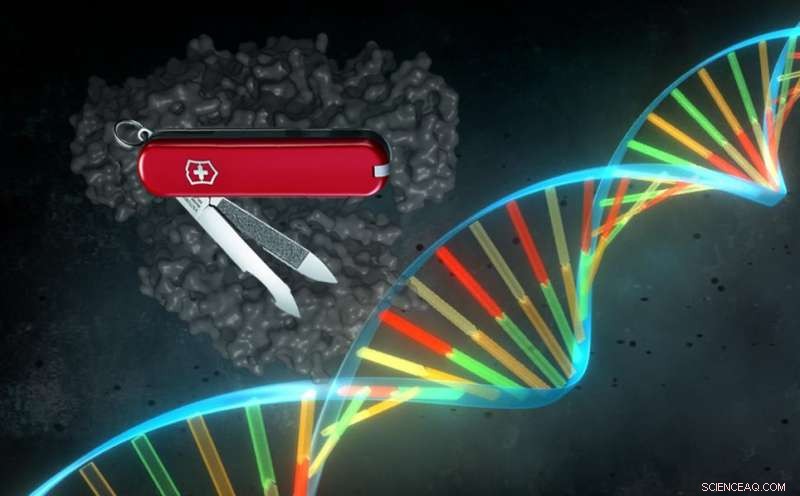
Vertegenwoordiging van CRISPR-eiwit Cpf1. De klasse 2 CRISPR Cas-complexen, inclusief Cas9 en Cpf1, hebben een grote veelzijdigheid, omdat een enkel eiwit geleid door een gids-RNA in staat is om een specifieke sequentie van het genoom te herkennen en te knippen. Krediet:Pablo Alcón / Universiteit van Kopenhagen
Wetenschappers van de Universiteit van Kopenhagen, onder leiding van de Spaanse professor Guillermo Montoya, onderzoeken de moleculaire kenmerken van verschillende moleculaire scharen van het CRISPR-Cas-systeem om licht te werpen op de zogenaamde "Zwitserse legermessen" van genoombewerking. Montoya's onderzoeksgroep heeft de atomaire structuren van de Cpf1- en Cas9-eiwitten gevisualiseerd om elk van hun eigenschappen en eigenaardigheden te analyseren, waardoor ze ideaal zijn voor verschillende toepassingen in genmodificatie.
Het team van professor Montoya van het Novo Nordisk Foundation Centre for Protein Research aan de Universiteit van Copenhaguen werkt actief op dit gebied. Onlangs, dit team verkreeg de moleculaire structuur van het CRISPR-Cpf1-complex na doelsplitsing. Dit eiwit uit de Cas-familie heeft het vermogen om specifiek het DNA af te wikkelen en te splitsen om het modificatieproces te starten.
"Deze eigenschap stelt ons in staat om de instructies in het genoom op een veiligere manier te bewerken, aangezien Cpf1 de specifieke DNA-sequentie met hogere precisie herkent, " legt Montoya uit aan SINC.
Nutsvoorzieningen, in een artikel gepubliceerd in Natuur Structurele en moleculaire biologie , de onderzoekers van de Deense instelling hebben de interne werking van deze moleculaire scharen geanalyseerd en vergeleken met CRISPR-Cas9, de baanbrekende technologie die een revolutie heeft veroorzaakt door een goedkope en gemakkelijke DNA-bewerkingstechnologie te bieden, ontdekt door Jennifer Doudna en Emmanuelle Charpentier in 2012.
Illustratie van het CRISPR-Cpf1-complex. Geleid door een RNA-molecuul, het Cpf1-eiwit kan worden geprogrammeerd om een specifieke sequentie in het genoom te herkennen en te knippen. Krediet:llusciences
Het gebruik van CRISPR-Cas9 voor genetische modificatie van planten en dieren is al in volle gang. In aanvulling, deze technologie wordt ook toegepast in de menselijke therapie van verschillende ziekten zoals kanker en het aantal toepassingen blijft groeien.
X-ray kristallografie
Door gebruik te maken van een biofysische techniek genaamd röntgenkristallografie, Montoya en collega's hebben de hoge-resolutiestructuur van Cpf1 en Cas9 onthuld om hun werkingsmechanisme beter te begrijpen, inclusief de doel-DNA-herkenning en splitsing.
Voor de moleculair bioloog de belangrijkste conclusie van de studie is dat "volgens hun moleculaire eigenaardigheden, afhankelijk van het resultaat dat we willen bereiken na het bewerkingsproces (dat wil zeggen, of we een DNA-fragment willen inactiveren of invoegen in een regio van het genoom), sommige van deze moleculaire hulpmiddelen zijn misschien meer geschikt dan andere."
"Bij het knippen van het DNA, Cas9 genereert stompe uiteinden, waardoor dit eiwit meer geschikt is voor gen-inactivatie. In tegenstelling tot, Cpf1 produceert verspringende complementaire uiteinden, waardoor het handiger is om een DNA-fragment in te voegen, " voegt Montoya toe.
Hij voegt toe, "Het is essentieel om het gedetailleerde apparaat van deze ingewikkelde moleculaire scalpels te onthullen, niet alleen om hun werkingsmechanisme te begrijpen, maar ook om rationeel veiligere en effectievere genoombewerkingstools te ontwerpen die zowel voor klinische of biotechnologische toepassingen als voor synthetische biologie kunnen worden gebruikt."
 Nieuwe studie onthult hoe ijzige oppervlaktevijvers op Himalaya-gletsjers de waterstroom beïnvloeden
Nieuwe studie onthult hoe ijzige oppervlaktevijvers op Himalaya-gletsjers de waterstroom beïnvloeden Waarom het verzamelen van water van miljoenen vrouwen tweederangsburgers maakt
Waarom het verzamelen van water van miljoenen vrouwen tweederangsburgers maakt Soorten Wespen die erg agressief zijn
Soorten Wespen die erg agressief zijn In de diepe zee, de laatste ijstijd is nog niet voorbij
In de diepe zee, de laatste ijstijd is nog niet voorbij drones, lasers om de mysteries van een mediterraan eiland te ontrafelen
drones, lasers om de mysteries van een mediterraan eiland te ontrafelen
Hoofdlijnen
- Neem een dosis Dickinson:poëzie als therapie
- Wat is een allel?
- Kenmerken van micro-organismen
- Bacteriële groei in petrischalen meten
- 5 stadia van mitose
- De leeftijd van een skelet bepalen
- Hoe verbeteren microscopen ons leven vandaag?
- Structurele kenmerken van blauwgroene algen
- Marihuanaboerderijen stellen gevlekte uilen bloot aan rattengif in Noordwest-Californië
 Wetenschappers stellen voor om elektronische apparaten te maken van koolerwten
Wetenschappers stellen voor om elektronische apparaten te maken van koolerwten Studie laat zien hoe bodembacteriën klaar zijn om broeikasgassen te consumeren
Studie laat zien hoe bodembacteriën klaar zijn om broeikasgassen te consumeren Studie werpt licht op de evolutie van de vroegste dinosauriërs
Studie werpt licht op de evolutie van de vroegste dinosauriërs Rook van Amerikaanse branden bereikt Europa, satellietgegevens laten zien
Rook van Amerikaanse branden bereikt Europa, satellietgegevens laten zien Japan bevestigt dat olie van vernielde tanker zijn stranden raakt
Japan bevestigt dat olie van vernielde tanker zijn stranden raakt Underwater Lost City is niet door mensen gebouwd,
Underwater Lost City is niet door mensen gebouwd,  Moeten we de aarde verhullen om het te verbergen voor kwaadaardige buitenaardse wezens?
Moeten we de aarde verhullen om het te verbergen voor kwaadaardige buitenaardse wezens?  Langlevende positroniumatomen maken voor zwaartekracht-experimenten met antimaterie
Langlevende positroniumatomen maken voor zwaartekracht-experimenten met antimaterie
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com






