
Wetenschap
Wetenschappers identificeren knelpunten in de toedieningsroutes van medicijnen in stamcellen
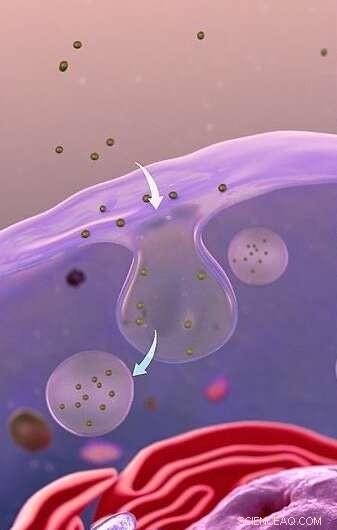
Om toegang te krijgen tot een cel, kunnen nanodeeltjes worden opgeslokt door het membraan dat de cel omringt, waardoor belachtige blaasjes worden gevormd - endocytose. Credit:Aangepast van www.scientificanimations.com CC BY-SA 4.0
Ons lichaam heeft formidabele barrières ontwikkeld om zichzelf te beschermen tegen vreemde stoffen - van onze huid tot onze cellen en elk onderdeel in de cellen, elk deel van ons lichaam heeft beschermende lagen. Deze verdedigingen, hoewel essentieel, vormen een grote uitdaging voor farmaceutische geneesmiddelen en therapieën, zoals vaccins, die meerdere barrières moeten omzeilen om hun doelen te bereiken.
Hoewel deze barrières van vitaal belang zijn in de farmaceutische wetenschap en het ontwerpen van geneesmiddelen, is er nog veel onbekend over hen en hoe ze te overwinnen.
In een recent onderzoek werpen onderzoekers van de Xi'an Jiaotong-Liverpool University en Nanjing University in China, en Western Washington en Emory University in de VS enig licht op waarom de afgifte van therapieën aan cellen zo moeilijk kan zijn.
Hindernissen overwinnen
Met COVID-19-vaccins, waarmee honderden miljoenen van ons zijn geïnjecteerd, moet mRNA worden ingesloten in beschermende vetbubbels - lipidenanodeeltjes - zodat het door de afweer van het lichaam kan gaan en het beoogde doelwit in onze cellen kan bereiken.
Sommige soorten cellen, zoals stamcellen, immuuncellen en zenuwcellen, hebben barrières die bijzonder moeilijk te overwinnen zijn, dus de afgifte van deeltjes in deze cellen is een nog grotere uitdaging.
In de studie, gepubliceerd in het tijdschrift ACS Nano , combineerden de onderzoekers geavanceerde microscopietechnieken om de levering van nanodeeltjes, die vaak worden gebruikt voor medicijnafgifte, in stamcellen in realtime te volgen.
Hun bevindingen suggereren dat nanodeeltjes in bepaalde soorten cellen "opgesloten" raken in belachtige blaasjes en zo worden verhinderd hun beoogde doelwit te bereiken.
Het team gebruikte hun bevindingen om een wiskundig model te maken dat kan voorspellen hoe efficiënt de levering van nanodeeltjes in cellen zal zijn, en dat kan helpen bij het ontwerpen van toekomstige therapieën.
Dr. Gang Ruan, een corresponderende auteur van de studie, zegt:"We hebben het leveringsproces van deeltjes in cellen opgesplitst in afzonderlijke stappen, zodat we elke stap kunnen visualiseren en een venster kunnen creëren in de mechanismen die door deze cellen worden gebruikt om zichzelf te beschermen.
"Om verbeterde toedieningsmethoden voor therapieën te ontwerpen, hebben we een kwantitatief begrip nodig van hoe delen van de cel en nanodeeltjes op elkaar inwerken. Zoals een geweldige bio-ingenieur die ik ooit kende, zei:als je een vliegtuig zou ontwerpen, zou je de aerodynamica moeten analyseren van elk onderdeel voordat je het vliegtuig bouwt.
"Door het knelpunt te vinden in de levering van nanodeeltjes in cellen, zullen onze bevindingen de weg vrijmaken voor meer gerichte en innovatieve therapieën die gebruik maken van op maat gemaakte levering, mogelijk voor individuele patiënten."
Weg bezorgd
Voorheen was beeldvorming van de levering van nanodeeltjes in cellen beperkt vanwege de vereiste hoge snelheid en kleinschaligheid. Het multidisciplinaire team was echter in staat om hun verschillende expertisegebieden te gebruiken om innovatieve manieren te creëren om deze hindernissen te overwinnen. Ze combineerden twee soorten microscopie-analyse, die voorheen alleen afzonderlijk werden gebruikt, zodat ze het hele leveringsproces konden bestuderen.
Xuan Yang, die samen met Dr. Xiaowei Wen het hoofdauteurschap van het onderzoek deelt, zegt:"We waren in staat om de beweging van de nanodeeltjes pixel voor pixel in realtime te volgen, en daardoor de beweging van de nanodeeltjes over membraanbarrières en wanneer ze elk compartiment van de stamcellen binnendringen."
Hoewel het proces van afgifte van nanodeeltjes in deze cellen complex is en bestaat uit verschillende mechanismen, heeft het team door visualisatie en vervolgens chemische modificatie van elke stap van het proces, de kritieke fase geïdentificeerd die de levering van de nanodeeltjes aan hun celdoelen verhindert.
Om toegang te krijgen tot een cel, kunnen nanodeeltjes worden opgeslokt door het membraan dat de cel omringt, waardoor belachtige blaasjes worden gevormd. In veel celtypen zouden de nanodeeltjes eenmaal in de cel uit deze bellen ontsnappen. In sommige extra beschermde cellen, zoals de stamcellen die in dit onderzoek zijn gebruikt, lijken de nanodeeltjes echter vast te komen te zitten in de blaasjes en kunnen ze niet ontsnappen. Dit betekent dat ze de cel niet kunnen binnengaan en hun doel kunnen bereiken.
De onderzoekers combineren hun waarnemingen en analyses in een wiskundig model dat kan voorspellen hoe efficiënt en snel deeltjes elke afleveringsstap zouden doorlopen en een cel zouden binnenkomen.
"Ons model kan worden gebruikt om te voorspellen wat de concentratie van de nanodeeltjes zal zijn, op een bepaalde locatie in de cel, op een bepaald moment", zegt Dr. Wen.
"De algemene methode van dit model kan worden gebruikt om verschillende soorten nanodeeltjes en cellen op te nemen om de leveringsmechanismen die worden gebruikt om in cellen over te gaan beter te begrijpen. Bijvoorbeeld, voorspellen hoe goed lipidenanodeeltjes in de COVID-19-vaccins mRNA in een cel zullen afleveren ."
Dr. Steven Emory, die ook een corresponderende auteur van de studie is, voegt eraan toe:"In staat zijn om de verschillende componenten en innerlijke werkingen die deel uitmaken van de leveringsroutes in realtime in kaart te brengen, leidt tot inzicht in hoe deze routes kunnen worden gecontroleerd. Dit zou kunnen openen een aantal echt opwindende dingen op het gebied van therapie.
"We hopen dat onze nieuwe tools en ons begrip een eerste houvast voor het systeem hebben gecreëerd, van waaruit wij, en andere onderzoekers, kunnen beginnen met klimmen en beginnen met verkennen." + Verder verkennen
Omhulsels van griepvirussen kunnen de levering van mRNA in cellen verbeteren
Hoofdlijnen
- Wat zijn Agar Slants?
- Hommels kunnen volgens de Californische instandhoudingswet als vissen worden geclassificeerd, zegt de rechtbank
- De rol van oxytocinen in relaties tussen mensen kan worden gedeeld met andere primaten
- Alfred Russel Wallace: Biography, Theory of Evolution & Facts
- Studie vindt paarden-DNA in 10 procent van vleesgerechten in Mexico
- Te veel zon is niet goed - voor mensen of planten
- Toch niet zo verschillend:menselijke cellen, winterharde microben delen een gemeenschappelijke voorouder
- Roept op tot einde aan Mexico's vangst van bedreigde bruinvis
- Skelet van enorme dinosaurus opgegraven in Portugal
- Bestrijding van uitbraken van ademhalingsvirussen door middel van snelle detectie op basis van nano-popcornsensoren
- Goede voedingsbodem voor germaneen
- Verbetering van de cyberbeveiliging in ruwe omgevingen
- De geboorte van een voetbal ter grootte van een subnanometer
- Grafeentapijten:zodat neuronen beter communiceren

 Big data en synthetische chemie kunnen klimaatverandering en vervuiling tegengaan
Big data en synthetische chemie kunnen klimaatverandering en vervuiling tegengaan Rusland wil terug naar Venus, herbruikbare raket bouwen
Rusland wil terug naar Venus, herbruikbare raket bouwen Planetaire wetenschapper werkt samen aan allereerste Mars-missie gelanceerd door Arabische wereld
Planetaire wetenschapper werkt samen aan allereerste Mars-missie gelanceerd door Arabische wereld Circulaire wateroplossingen toepassen van India tot Zweden
Circulaire wateroplossingen toepassen van India tot Zweden Sulphur biedt veelbelovend batterij-alternatief van de volgende generatie
Sulphur biedt veelbelovend batterij-alternatief van de volgende generatie Volkstuin is veiliger dan de nationale richtlijnen van het VK suggereren
Volkstuin is veiliger dan de nationale richtlijnen van het VK suggereren Lockdown-onderzoek toont aan dat thuiswerken loont
Lockdown-onderzoek toont aan dat thuiswerken loont Uitvinding van vormveranderend textiel dat alleen wordt aangedreven door lichaamswarmte
Uitvinding van vormveranderend textiel dat alleen wordt aangedreven door lichaamswarmte
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com


