
Wetenschap
Nieuwe nanodeeltjes leveren CRISPR-tools voor het bewerken van genen in de cel met een veel hogere efficiëntie
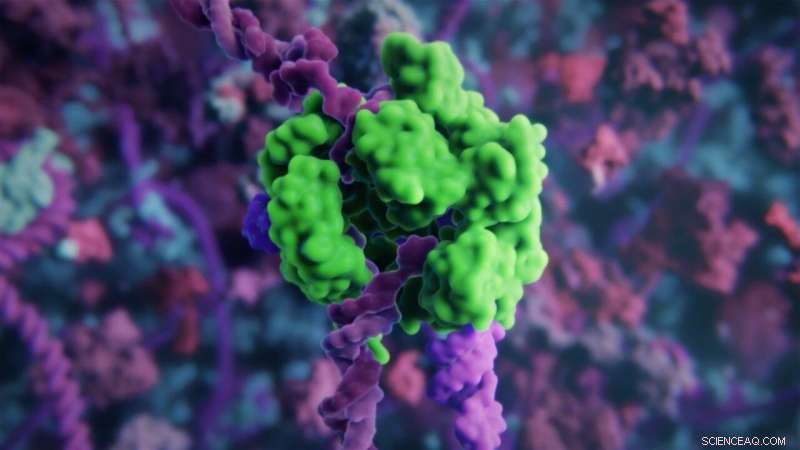
Het grote complex van moleculen voor het bewerken van genen is moeilijk van een externe toepassing in cellen af te leveren. Biologisch afbreekbare lipidenanodeeltjes leveren mRNA-codering voor de genbewerkingsmoleculen in de cel Credit:Van animatie door Visual Science en Skoltech, visual-science.com/crispr
Een onderzoekssamenwerking tussen Tufts University en de Chinese Academie van Wetenschappen heeft geleid tot de ontwikkeling van een aanzienlijk verbeterd leveringsmechanisme voor de CRISPR/Cas9-genbewerkingsmethode in de lever, volgens een onderzoek dat onlangs in het tijdschrift is gepubliceerd Geavanceerde materialen . De levering maakt gebruik van biologisch afbreekbare synthetische lipidenanodeeltjes die de moleculaire bewerkingstools in de cel brengen om de genetische code van de cellen nauwkeurig te veranderen met een efficiëntie van maar liefst 90 procent. De nanodeeltjes vormen een van de meest efficiënte CRISPR/Cas9-leveringstools die tot nu toe zijn gerapporteerd, volgens de onderzoekers en zou kunnen helpen technische hindernissen te overwinnen om genbewerking in een breed scala van klinische therapeutische toepassingen mogelijk te maken.
Het CRISPR/Cas9-genbewerkingssysteem is een krachtig onderzoeksinstrument geworden dat de functie van honderden genen blootlegt en wordt momenteel onderzocht als een therapeutisch hulpmiddel voor de behandeling van verschillende ziekten. Echter, er zijn nog enkele technische hindernissen voordat het praktisch kan zijn voor klinische toepassingen. CRISPR/Cas9 is een groot moleculair complex, met zowel een nuclease (Cas9) die door beide strengen van een gerichte genomische sequentie kan snijden, en een geconstrueerd 'single-guide' RNA (sgRNA) dat het genoom scant om de nuclease te helpen die specifieke sequentie te vinden die moet worden bewerkt. Omdat het een groot moleculair complex is, het is moeilijk om CRISPR/Cas9 rechtstreeks in de celkern af te leveren, waar het zijn werk kan doen. Anderen hebben de bewerkingsmoleculen in virussen verpakt, polymeren, en verschillende soorten nanodeeltjes om ze in de kern te krijgen, maar de lage efficiëntie van overdracht heeft hun gebruik en potentie voor klinische toepassingen beperkt.
De lipidenanodeeltjes die in het onderzoek worden beschreven, kapselen boodschapper-RNA (mRNA) in dat codeert voor Cas9. Zodra de inhoud van de nanodeeltjes - inclusief het sgRNA - in de cel wordt vrijgegeven. De eiwit-makende machine van de cel neemt het over en maakt Cas9 van de mRNA-sjabloon, het voltooien van de genbewerkingskit. Een uniek kenmerk van de nanodeeltjes is dat ze gemaakt zijn van synthetische lipiden die disulfidebindingen in de vetketen bevatten. Als de deeltjes de cel binnenkomen, de omgeving in de cel breekt de disulfidebinding open om de nanodeeltjes uit elkaar te halen en de inhoud wordt snel en efficiënt in de cel afgegeven.
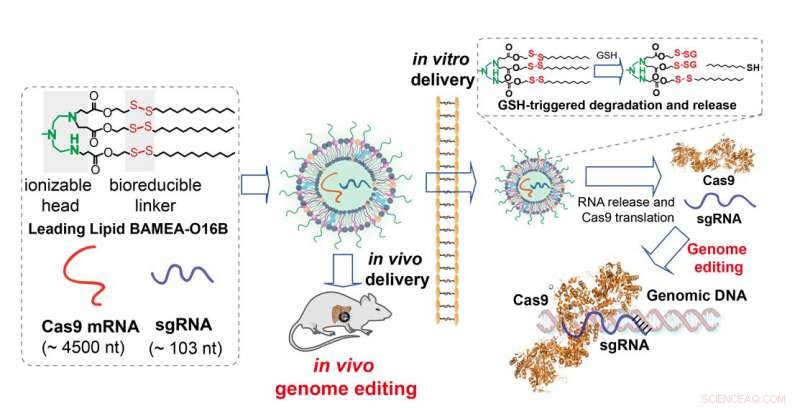
Lipiden geformuleerd met een bioreduceerbare linker vormen de wand van nanodeeltjes die het mRNA van Cas9 plus sgRNA inkapselen. Bij binnenkomst in de cel, in vitro of in vivo, de linkers worden gebroken en de deeltjes vallen uiteen voor levering van inhoud en vertaling van mRNA in actief enzym voor CRISPR/Cas9-genoombewerking Credit:Qiaobing Xu, Tufts University
"We beginnen net menselijke klinische proeven te zien voor CRISPR-therapieën, " zei Qiaobing Xu, co-corresponderende auteur van de studie en universitair hoofddocent biomedische technologie aan de Tufts University. "Er zijn veel ziekten die al lang onhandelbaar zijn en waarvoor CRISPR-therapieën nieuwe hoop kunnen bieden, bijvoorbeeld sikkelcelziekte, Duchenne spierdystrofie, De ziekte van Huntington, en zelfs veel kankers. We hopen dat deze vooruitgang ons een nieuwe stap zal brengen in de richting van het maken van CRISPR een effectieve en praktische benadering van behandeling."
De onderzoekers pasten de nieuwe methode toe op muizen, proberen de aanwezigheid van een gen dat codeert voor PCSK9 te verminderen, waarvan het verlies gepaard gaat met een lager LDL-cholesterol, en verminderd risico op hart- en vaatziekten. "De lipidenanodeeltjes zijn een van de meest efficiënte CRISPR/Cas9-dragers die we hebben gezien, " zei Ming Wang, tevens co-corresponderende auteur van de studie en professor aan de Chinese Academie van Wetenschappen, Nationaal laboratorium voor moleculaire wetenschappen in Peking. "We kunnen de PCSK9-expressie bij muizen zelfs uitschakelen met een efficiëntie van 80 procent in de lever, suggereert een echte belofte voor therapeutische toepassingen."
 De ecologische voetafdruk van het avondeten:hoe groen zijn vissticks?
De ecologische voetafdruk van het avondeten:hoe groen zijn vissticks? Uitgebreid beeld van vegetatie en klimaat op het Tibetaanse plateau tijdens de Kwartaire ijstijden
Uitgebreid beeld van vegetatie en klimaat op het Tibetaanse plateau tijdens de Kwartaire ijstijden Nieuw model van de mariene zwavelcyclus na de ijstijd van de sneeuwbalaarde
Nieuw model van de mariene zwavelcyclus na de ijstijd van de sneeuwbalaarde As van vulkanen uit het dinosaurustijdperk verbonden met schalieolie, gas-
As van vulkanen uit het dinosaurustijdperk verbonden met schalieolie, gas- Bosbranden in Californië geven aanleiding tot bezorgdheid over de gevolgen voor het milieu en de gezondheid
Bosbranden in Californië geven aanleiding tot bezorgdheid over de gevolgen voor het milieu en de gezondheid
Hoofdlijnen
- Kuikenembryo's leveren waardevolle genetische gegevens voor het begrijpen van de menselijke ontwikkeling
- Meeluisteren:akoestische bewakingsapparatuur detecteert illegale jacht en houtkap
- Vingerafdrukexperimenten
- Music Science Fair Project Ideas
- Sequentiebepaling van het genoom van stevia-planten voor het eerst onthuld
- Wat zijn de primaire functies van fosfolipiden?
- Onderzoekers ontdekken moleculaire add-ons die eiwitinterfaces aanpassen
- Waarom gifkikkers zichzelf niet vergiftigen?
- Luie valsspeler leeft onder de grond,
- Nieuwe technologie maakt metalen draden op zonnecellen bijna onzichtbaar voor licht

- Neutronen onthullen potentiële gevaren van gouden nanodeeltjes - farmaceutische medicijnafleveringsagent van de toekomst

- Sneeuwvlokken worden vierkant met een beetje hulp van grafeen

- Kunstmatig DNA kan de afgifte van actieve ingrediënten uit medicijnen regelen

- Nanodeeltjes die stolsels vormen, verhogen de overlevingskans na explosietrauma
 Hoe ideeën over volwassenheid, zijn rechten en plichten, veranderen over de hele wereld
Hoe ideeën over volwassenheid, zijn rechten en plichten, veranderen over de hele wereld De aard van kernkrachten ingeprent in fotonen
De aard van kernkrachten ingeprent in fotonen Japan lanceert satelliet om militaire communicatie te moderniseren
Japan lanceert satelliet om militaire communicatie te moderniseren De uitstoot van broeikasgassen verminderen met behulp van microgolfplasmatechnologie
De uitstoot van broeikasgassen verminderen met behulp van microgolfplasmatechnologie Onderzoekers verplaatsen grafeenelektronica naar 3D
Onderzoekers verplaatsen grafeenelektronica naar 3D Apparaat haalt energie uit laagfrequente trillingen
Apparaat haalt energie uit laagfrequente trillingen Nieuwe waarnemingen tonen aan dat een rotsachtige exoplaneet slechts de helft van de massa van Venus heeft
Nieuwe waarnemingen tonen aan dat een rotsachtige exoplaneet slechts de helft van de massa van Venus heeft Methoden voor het maken van Opals in een Lab
Methoden voor het maken van Opals in een Lab
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

