
Wetenschap
Nanostraws leveren moleculen veilig en efficiënt aan menselijke cellen
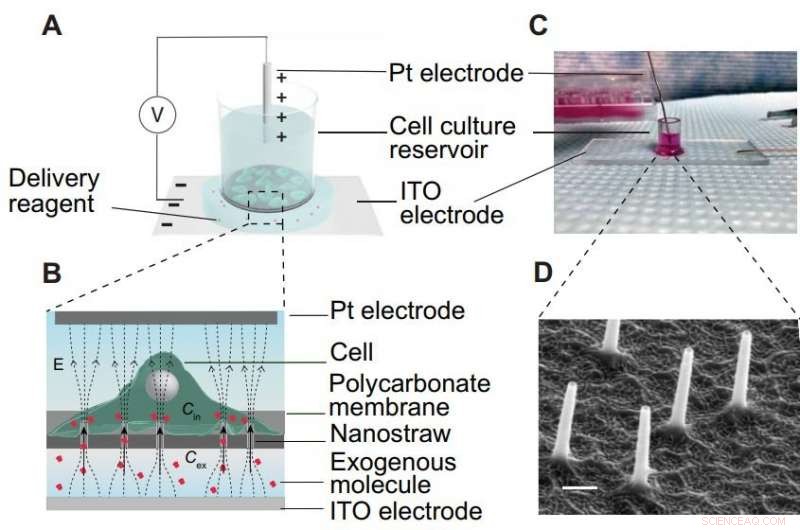
Ontwerp en werking van de NES. (A) Cellen worden gekweekt op het NS-membraan in de geometrie van een putplaat. (B) Het leveringsreagens wordt onder de bodem van het reservoir geplaatst. Een elektrisch veld wordt aangelegd tussen de platina- en ITO-elektrode om exogene moleculen in cellen af te leveren. (C) Schematische voorstelling van het NES-aflevermechanisme. De moleculen onder het NS-membraan worden elektroforetisch via de NS in cellen van belang geïnjecteerd. De afgegeven concentratie (Cin) staat in kwadratische relatie met de spanningsintensiteit die op de cellen (V) wordt toegepast en is evenredig met de concentratie van exogene moleculen (Cex) en de leveringsduur. (D) SEM-beeld van de NS die uit het membraan steekt. Schaalbalk, 300 nm. Credit: wetenschappelijke vooruitgang (2018). DOI:10.1126/sciadv.aat8131
Onderzoekers kunnen het perfecte molecuul ontwerpen om een gen te bewerken, kanker behandelen of de ontwikkeling van een stamcel begeleiden, maar uiteindelijk zal dat er allemaal niet toe doen als ze hun moleculen niet in de menselijke cellen kunnen krijgen die ze willen manipuleren. De oplossing voor dat probleem, beschreven in een studie gepubliceerd op 31 oktober in wetenschappelijke vooruitgang , kunnen minuscule nanorietjes zijn, kleine glasachtige uitsteeksels die even kleine gaatjes in celwanden prikken om hun lading af te leveren.
Een team onder leiding van Nicholas Melosh, een universitair hoofddocent materiaalkunde en techniek, begon ongeveer vijf jaar geleden met het testen van nanorietjes met behulp van relatief taaie cellijnen afgeleid van kankers, muiscellen en andere bronnen. Nutsvoorzieningen, Melosh en collega's hebben aangetoond dat de techniek ook in menselijke cellen werkt, een resultaat dat medisch en biologisch onderzoek zou kunnen versnellen en op een dag gentherapie voor oogziekten zou kunnen verbeteren, immuunsysteem of kanker.
"Wat je ziet is een enorme impuls voor gentherapie en kankerimmunotherapie, " zei Melosh, die ook lid is van Stanford Bio-X, Stanford ChEM-H en het Wu Tsai Neurosciences Institute, maar bestaande technieken zijn niet de uitdaging om materialen aan alle relevante menselijke celtypen te leveren, vooral immuuncellen. "Ze zijn echt taai vergeleken met bijna alle andere cellen die we hebben behandeld, " hij zei.
Het celmembraan oversteken
Het idee om chemicaliën door het celmembraan en in de cel zelf te transporteren is niet nieuw, maar er zijn een aantal problemen met de methoden waarop wetenschappers tot nu toe vertrouwden. In een gemeenschappelijke methode, elektroporatie genoemd, onderzoekers gebruiken een elektrische stroom om gaten in celwanden te openen waardoor moleculen zoals DNA of eiwitten kunnen diffunderen, maar de methode is onnauwkeurig en kan veel van de cellen doden waarmee onderzoekers proberen te werken.
Bij een andere methode, onderzoekers gebruiken virussen om het betreffende molecuul door een celwand te vervoeren, maar het virus zelf brengt risico's met zich mee. Hoewel er vergelijkbare methoden zijn die virussen vervangen door meer goedaardige chemicaliën, ze zijn minder nauwkeurig en effectief.
Dat was de stand van zaken tot vijf of zes jaar geleden, toen Melosh en collega's een nieuwe manier bedachten om moleculen in cellen te krijgen, gebaseerd op Melosh's expertise in nanomaterialen. Ze zouden elektroporatie gebruiken, maar doe het op een veel preciezere manier met nanorietjes, die vanwege hun relatief lange, smal profiel helpt elektrische stromen in een zeer kleine ruimte te concentreren.
Destijds, ze testten die techniek op dierlijke cellen die bovenop een bed van nanorietjes zaten. Toen ze een elektrische stroom aanzetten, de nanorietjes gingen piepklein open, poriën van regelmatige grootte in het celmembraan - genoeg om moleculen binnen te laten, maar niet genoeg om ernstige schade aan te richten.
De elektrische stroom diende ook nog een ander doel. In plaats van te wachten tot moleculen willekeurig door de nieuw geopende poriën drijven, de stroom trok moleculen rechtstreeks de cel in, het verhogen van de snelheid en precisie van het proces. De vraag was op dat moment of de techniek even effectief zou zijn op het soort menselijke cellen dat clinici zouden moeten manipuleren om ziekten te behandelen.
sneller, veiliger, Precieser
In de nieuwe krant Melosh en team toonden aan dat het antwoord ja was - ze leverden met succes moleculen af in drie menselijke celtypen en muizenhersencellen, die in het verleden allemaal moeilijk waren gebleken om mee te werken.
Bovendien, de methode was nauwkeuriger, sneller en veiliger dan andere methoden. De nanostraw-techniek kostte slechts 20 seconden om moleculen aan cellen te leveren, vergeleken met dagen voor sommige methoden, en doodde minder dan tien procent van de cellen, een enorme verbetering ten opzichte van standaard elektroporatie.
Melosh en zijn lab werken nu aan het testen van de nanostraw-methode in enkele van de moeilijkst te bewerken cellen in de buurt, menselijke immuuncellen. Als ze slagen, het kan een grote stap zijn, niet alleen voor wetenschappers die cellen willen aanpassen voor onderzoeksdoeleinden, maar ook voor artsen die kanker willen behandelen met immunotherapie, wat op dit moment inhoudt dat de immuuncellen van een persoon worden gewijzigd met behulp van virale methoden. Nanostraws zouden niet alleen dat gevaar vermijden, maar zouden het immunotherapieproces mogelijk kunnen versnellen en de kosten ervan kunnen verlagen, ook, zei Melosh.
 Het productieproces van rubber
Het productieproces van rubber Schrijf met warmte, afkoelen en herhaal dan met herschrijfbaar papier
Schrijf met warmte, afkoelen en herhaal dan met herschrijfbaar papier Onderzoekers smeden nieuwe rekenhulpmiddelen om nauwkeuriger voorspellingen te doen van eiwitstructuren
Onderzoekers smeden nieuwe rekenhulpmiddelen om nauwkeuriger voorspellingen te doen van eiwitstructuren X-ray fluorescentie mapping om tumorpenetratie te meten door een nieuw middel tegen kanker
X-ray fluorescentie mapping om tumorpenetratie te meten door een nieuw middel tegen kanker Onderzoekers creëren deeltjes van één nanometer trimetaallegering
Onderzoekers creëren deeltjes van één nanometer trimetaallegering
 De stranden van Tel Aviv vallen tegen in Israëls passie voor plastic
De stranden van Tel Aviv vallen tegen in Israëls passie voor plastic Duiken in waterbehandelingsstrategieën voor zwembaden
Duiken in waterbehandelingsstrategieën voor zwembaden Van scheve wortelen en vlekkerige aardappelen:een verhaal over voedselverspilling
Van scheve wortelen en vlekkerige aardappelen:een verhaal over voedselverspilling Hoe de eenheid en diversiteit van het leven te verklaren
Hoe de eenheid en diversiteit van het leven te verklaren  Wetenschappers meten nieuwe diepten aan de onderkant van de hydrologische cyclus
Wetenschappers meten nieuwe diepten aan de onderkant van de hydrologische cyclus
Hoofdlijnen
- 3D-verpakking van DNA reguleert celidentiteit
- Wat zijn de meest voorkomende oorzaken van uitsterven?
- Netwerken gebruiken om weefselspecifieke genregulatie te begrijpen
- Van wilde kamelen tot cocaïne-nijlpaarden, grote dieren verwilderen de wereld
- Cel Life Functies
- Hoe verschilt DNA & RNA?
- Rechtbank vindt het goed om een soort uil te doden om het effect op andere uilen te zien
- Prehistorische skeletten van vrouwen tonen impact van rigoureuze handenarbeid
- Wat zijn de verschillen van eenvoudig en gestratificeerd weefsel?
- Snelle tijden en hotspots in plasmonische nanostructuren
- Team gebruikt nanotechnologie om elektronen te koelen zonder externe bronnen

- Sandwichkatalysatoren bieden een hogere activiteit en duurzaamheid

- Moleculaire gum zorgt voor betere gegevensopslag en computers voor AI

- De flinterdunne e-skin reageert op aanraking door op te lichten

 Onderzoekers onthullen patronen van seksueel misbruik in religieuze omgevingen
Onderzoekers onthullen patronen van seksueel misbruik in religieuze omgevingen Zwitserse autoriteiten waarschuwen voor instorting gletsjer gebied evacueren
Zwitserse autoriteiten waarschuwen voor instorting gletsjer gebied evacueren EU onderzoekt videogamebedrijven wegens antitrustkwesties
EU onderzoekt videogamebedrijven wegens antitrustkwesties Celmembraan als materiaal voor botvorming
Celmembraan als materiaal voor botvorming Spitzer legt geweldig familieportret vast
Spitzer legt geweldig familieportret vast Amerikaans vrachtruimtevaartuig klaar voor vertrek vanuit het internationale ruimtestation
Amerikaans vrachtruimtevaartuig klaar voor vertrek vanuit het internationale ruimtestation Archeologen in de voorhoede van milieu- en klimaatonderzoek
Archeologen in de voorhoede van milieu- en klimaatonderzoek Wetenschappers voorspellen veelbelovende nieuwe familie van materialen voor koeling in vaste toestand
Wetenschappers voorspellen veelbelovende nieuwe familie van materialen voor koeling in vaste toestand
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

