
Wetenschap
Nieuwe op nanodeeltjes gebaseerde aanpak detecteert en behandelt tandplak zonder medicijnen
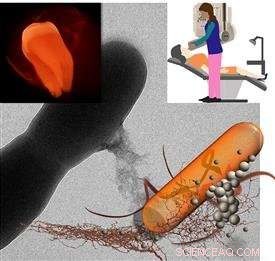
In deze illustratie, nanodeeltjes hechten aan of worden opgenomen door de bacteriecellen. Pan en zijn studenten zijn de eerste groep die aantoont dat vroege detectie van tandplak in de kliniek mogelijk is met behulp van de reguliere intraorale röntgenmachine die schadelijke bacteriepopulaties kan opsporen. Krediet:University of Illinois Laboratory for Materials in Medicine.
Wanneer de goede en slechte bacteriën in onze mond uit balans raken, de slechte bacteriën vormen een biofilm (ook wel plaque genoemd), die gaatjes kunnen veroorzaken, en indien onbehandeld na verloop van tijd, kan leiden tot cardiovasculaire en andere ontstekingsziekten zoals diabetes en bacteriële longontsteking.
Een team van onderzoekers van de Universiteit van Illinois heeft onlangs een praktische op nanotechnologie gebaseerde methode ontwikkeld voor het detecteren en behandelen van de schadelijke bacteriën die tandplak veroorzaken en leiden tot tandbederf en andere schadelijke aandoeningen.
Universitair hoofddocent bio-engineering Dipanjan Pan (zittend) en promovendus Fatemeh Ostadhossein hebben een drugsvrij, op nanotechnologie gebaseerde methode voor het detecteren en vernietigen van de bacteriën die tandplak veroorzaken.
Mondplak is onzichtbaar voor het oog, dus tandartsen visualiseren het momenteel met onthullende middelen, die ze aan patiënten toedienen in de vorm van een oplosbare tablet of een uitstrijkje. Hoewel nuttig om patiënten te helpen de omvang van hun plaque te zien, deze methoden zijn niet in staat om het verschil tussen goede en slechte bacteriën te identificeren.
"Momenteel in de kliniek, detectie van tandplak is zeer subjectief en hangt alleen af van de visuele evaluatie van de tandarts, " zei universitair hoofddocent bio-engineering Dipanjan Pan, hoofd van het onderzoeksteam. "We hebben voor het eerst aangetoond dat vroege detectie van tandplak in de kliniek mogelijk is met behulp van de reguliere intraorale röntgenmachine die schadelijke bacteriepopulaties kan opsporen."

University of Illinois Associate Professor of Bioengineering Dipanjan Pan (zittend) en doctoraalstudent Fatemeh Ostadhossein hebben een drugsvrij, op nanotechnologie gebaseerde methode voor het detecteren en vernietigen van de bacteriën die tandplak veroorzaken. Credit:Heather Coit/University of Illinois College of Engineering
Om dit te realiseren, Fatemeh Ostadhossein, een afgestudeerde bio-ingenieurswetenschappen in Pan's groep, ontwikkelde een tandplakdetectiesonde die werkt in combinatie met gangbare röntgentechnologie en die in staat is om specifieke schadelijke bacteriën te vinden die bekend staan als Streptococcus mutans (S. mutans) in een complex biofilmnetwerk. Aanvullend, ze toonden ook aan dat door de chemische samenstelling van de sonde aan te passen, het kan worden gebruikt om de S. mutans-bacteriën te richten en te vernietigen.
De sonde bestaat uit nanodeeltjes gemaakt van hafniumoxide (HfO2), een niet-toxisch metaal dat momenteel klinisch wordt getest voor intern gebruik bij mensen. In hun studie hebben het team toonde de werkzaamheid van de sonde aan om biochemische markers te identificeren die aanwezig zijn aan het oppervlak van de bacteriële biofilm en tegelijkertijd S. mutans te vernietigen. Ze voerden hun onderzoek uit op Sprague Dawley-ratten.
In praktijk, Pan stelt zich voor dat een tandarts de sonde op de tanden van de patiënt aanbrengt en de röntgenmachine gebruikt om de omvang van de biofilmplak nauwkeurig te visualiseren. Als de plaque als ernstig wordt beschouwd, dan zou de tandarts het toedienen van de therapeutische HfO2-nanodeeltjes in de vorm van een tandpasta.
In hun studie hebben het team vergeleek het therapeutische vermogen van hun nanodeeltjes met chloorhexidine, een chemische stof die momenteel door tandartsen wordt gebruikt om biofilm uit te roeien. "Onze HfO2-nanodeeltjes zijn veel efficiënter in het doden van de bacteriën en het verminderen van de biofilmbelasting, zowel in celculturen van bacteriën als in [geïnfecteerde] ratten, zei Ostadhossein, opmerkend dat hun nieuwe technologie ook veel veiliger is dan conventionele behandeling.
Het therapeutische effect van de nanodeeltjes is te wijten, zei Pan, aan hun unieke oppervlaktechemie, die een vergrendelings- en kill-mechanisme biedt. "Dit mechanisme onderscheidt ons werk van eerder nagestreefde benaderingen op basis van nanodeeltjes, waarbij het medicinale effect afkomstig is van antibiotica ingekapseld in de deeltjes, " zei Pan, ook een faculteitslid van het Carle Illinois College of Medicine en het Beckman Institute for Advanced Science and Technology. "Dit is goed omdat onze aanpak problemen met antibioticaresistentie vermijdt en het is veilig en zeer schaalbaar, waardoor het zeer geschikt is voor eventuele klinische vertaling."
Naast Pan en Ostadhossein, andere leden van het onderzoeksteam zijn onder meer bio-engineering postdoctoraal onderzoeker Santosh Misra, gastwetenschapper Indu Tripathi, niet-gegradueerde Valeriya Kravchuk, gastwetenschapper Gururaja Vulugundam; en diergeneeskunde klinische assistent-professor Denae LoBato en adjunct-assistent-professor Laura Selmic.
Hun werk wordt beschreven in de krant, "Hafniumoxide-nanodeeltjes met twee doelen bieden beeldvorming van de tandheelkundige biofilm van Streptococcus mutans en bestrijden deze in vivo via een drugsvrije benadering, " online gepubliceerd op 30 juli, 2018, in het journaal Biomaterialen .
 Een wrede oorlog en rivieren vergiftigd bij elke regenval:hoe een mijn een eiland vernietigde
Een wrede oorlog en rivieren vergiftigd bij elke regenval:hoe een mijn een eiland vernietigde De natuurlijke habitat van olifanten
De natuurlijke habitat van olifanten  Het noordpoolgebied staat in brand:de Siberische hittegolf alarmeert wetenschappers
Het noordpoolgebied staat in brand:de Siberische hittegolf alarmeert wetenschappers Britse bedrijfsreuzen ondertekenen pact om plastic afval te verminderen
Britse bedrijfsreuzen ondertekenen pact om plastic afval te verminderen Er wordt vertrouwd op groene groei om klimaatverandering op te lossen, maar dat is een probleem
Er wordt vertrouwd op groene groei om klimaatverandering op te lossen, maar dat is een probleem
Hoofdlijnen
- Wat is het Malthusiaanse uitgangspunt?
- Wat is een regeling in de microbiologie?
- Hoe worden genen aan- en uitgezet?
- Is de Krebs-cyclus aëroob of anaëroob?
- Is er een verband tussen dankbaarheid en geluk?
- Wat is een gen?
- Wetenschappers werken aan een omkeerbare vorm van genbewerking
- Biofysici ontrafelen de exacte vouwing van een enkel gen
- Beperkingen van enzymen gebruikt in Forensic Science
- Onderzoekers maken 's werelds grootste DNA-origami

- Onderzoeksteam slaagt erin transistors te bouwen met siliceen

- Individuele onzuiverheidsatomen detecteerbaar in grafeen

- Onderzoekers gebruiken aluminium nanostructuren voor fotorealistisch printen van plasmonische kleurenpaletten

- Atomic mismatch creëert nano-halters

 Negatieve opvattingen over flexibel werken heersen, vooral onder mannen
Negatieve opvattingen over flexibel werken heersen, vooral onder mannen Het klimaat in het Jura-tijdperk
Het klimaat in het Jura-tijdperk  Alarmerend lage regenniveaus zorgen ervoor dat Californië in de zomer brandgevaarlijk is, val
Alarmerend lage regenniveaus zorgen ervoor dat Californië in de zomer brandgevaarlijk is, val Prijskaartje op de planeet? Zakelijk helpen de natuur te waarderen
Prijskaartje op de planeet? Zakelijk helpen de natuur te waarderen Waarom de atmosfeer van de zon honderden keren heter is dan het oppervlak?
Waarom de atmosfeer van de zon honderden keren heter is dan het oppervlak? Landdegradatie duwt planeet richting zesde massa-extinctie
Landdegradatie duwt planeet richting zesde massa-extinctie Stonehenge-mysterie opgelost? Prehistorische Fransen hebben het en andere Europese megalieten misschien geïnspireerd
Stonehenge-mysterie opgelost? Prehistorische Fransen hebben het en andere Europese megalieten misschien geïnspireerd Journalistieke banen zijn precair, financieel onzeker en hulp van het gezin nodig
Journalistieke banen zijn precair, financieel onzeker en hulp van het gezin nodig
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway | French |

-
Wetenschap © https://nl.scienceaq.com

