
Wetenschap
De 7 diatomische elementen die niet tegen alleen zijn kunnen

Diatomische elementen Ik heb er een hekel aan om alleen te zijn, zozeer zelfs dat ze niet als afzonderlijke atomen worden aangetroffen.
In plaats daarvan zijn het altijd twee atomen van hetzelfde pure element die aan elkaar zijn gebonden. Het staat al in de naam:Di - betekent "twee" en atomisch betekent ‘van de atomen’. En elementen zijn de basisbouwstenen van het universum.
Inhoud
- Wat zijn de 7 diatomische elementen?
- Hoe u de 7 diatomische elementen kunt onthouden
- Diatomische elementen zijn overal
Wat zijn de 7 diatomische elementen?
Op het periodiek systeem, dat 118 elementen bevat, zijn er slechts zeven diatomische elementen:
- Waterstof :H2
- Stikstof :N2
- Fluor :F2
- Zuurstof :O2
- Jodium :Ik2
- Chloor :Cl2
- Broom :Br2
Met uitzondering van waterstof, dat linksboven in het periodiek systeem verschijnt, raken de diatomische elementen elkaar en vormen een omgekeerde L-vorm. Dus als je er een tegenkomt, zou je ze allemaal gemakkelijk moeten kunnen vinden.
Hoe u de 7 diatomische elementen kunt onthouden
Heb je een gemakkelijke manier nodig om deze zeven te onthouden? Probeer dit geheugensteuntje:H met N o F oor O f Ik ce C oude B eer. De eerste letter van elk woord herinnert je aan elk diatomisch element.
Diatomische elementen zijn overal
Er zijn slechts zeven diatomische elementen die deze dubbele binding standaard gebruiken. Vijf ervan – waterstof, stikstof, fluor, zuurstof en chloor – zijn gassen bij kamertemperatuur en normale druk. Ze worden ook wel 'elementaire gassen' genoemd.
Broom is altijd een vloeistof, terwijl jodium bij kamertemperatuur vloeibaar of vast kan zijn, afhankelijk van verschillende factoren. Alle zeven zijn niet-metaalachtig.
Diatomische elementen zijn niet zeldzaam – integendeel! Stikstof en zuurstof, in hun tweeatomige vormen N2 en O2 , vormen 99 procent van de atmosfeer op aarde. Dat is het tegenovergestelde van zeldzaam.
Diatomische moleculen
Andere elementen kunnen zich binden met diatomische elementen om diatomische moleculen te vormen. Zo krijgen we keukenzout (natrium + chloor =NaCl, natriumchloride).
Je kunt overal een diatomisch molecuul vinden. Sommige andere elementen kunnen diatomische moleculen vormen, maar de bindingen zijn erg zwak en onstabiel. Ze blijven niet lang diatomisch. Alleen de zeven diatomische elementen vormen sterke banden en verschijnen bijna altijd in deze vorm.
Dat is elementairElementen kunnen ook monatomisch zijn, wat betekent dat er maar één atoom is. (ma - betekent "één.") Helium is een monatomisch element. En zuurstof kan triatomisch zijn, waarbij de zuurstofatomen een drievoudige binding vormen. Dat is wat wij gewoonlijk ‘ozon’ noemen.
Veel beantwoorde vragen
Wat is een diatomisch element?
Een diatomisch element is een element dat bestaat uit atomenparen. Het meest voorkomende diatomische element is waterstof, dat bestaat als H2. Nieuwe trucjes leren van zeesponzen, naturen meest onwaarschijnlijke civiel ingenieurs
Nieuwe trucjes leren van zeesponzen, naturen meest onwaarschijnlijke civiel ingenieurs Techniek kan helpen bij massaproductie van biologisch afbreekbaar plastic
Techniek kan helpen bij massaproductie van biologisch afbreekbaar plastic Kunstmatige vorming van peptidebindingen geeft aanwijzingen voor het creëren van leven op aarde
Kunstmatige vorming van peptidebindingen geeft aanwijzingen voor het creëren van leven op aarde Fotokatalytische nanovezels ontwikkeld voor gebruik bij efficiënte waterstofproductie
Fotokatalytische nanovezels ontwikkeld voor gebruik bij efficiënte waterstofproductie Hoe Delta H
Hoe Delta H
 Nieuwe anti-namaaktechniek combineert twee lichtreactieve afbeeldingen in één materiaal
Nieuwe anti-namaaktechniek combineert twee lichtreactieve afbeeldingen in één materiaal  Diepe ondergrondse krachten verklaren aardbevingen op San Andreas Fault
Diepe ondergrondse krachten verklaren aardbevingen op San Andreas Fault Onderzoekers vinden wolken gevuld met ijslolly's
Onderzoekers vinden wolken gevuld met ijslolly's Het land van het Vega Granada-gebied zakt tot één centimeter per jaar in als gevolg van de droogte
Het land van het Vega Granada-gebied zakt tot één centimeter per jaar in als gevolg van de droogte Duurzaamheid inbouwen in traditionele Chinese medicijnenhandel op de nieuwe zijderoutes
Duurzaamheid inbouwen in traditionele Chinese medicijnenhandel op de nieuwe zijderoutes
Hoofdlijnen
- Paarden kunnen onze lichaamstaal lezen, zelfs als ze ons niet kennen
- Man of vrouw? Wetenschappers ontdekken het genetische mechanisme dat de geslachtsontwikkeling bij vlinders bepaalt
- Wat zijn de functies van microfilamenten en microtubuli?
- Vetmolecuul in menselijk bloed controleert malariaparasieten beslissing om op muggen te springen
- Wetenschappers ontdekken dat hogere CO₂-niveaus de overleving van virussen in de lucht vergroten en het overdrachtsrisico vergroten
- VS overweegt de bescherming van beren in het noordwesten van Montana te beëindigen
- Verlichting aan het water verstoort de natuur in het omliggende ecosysteem drastisch
- Kaperparasiet geblokkeerd voor infiltratie van bloed
- Waarom doden we?
- Verbetering van de weerstand tegen aardbevingen met een enkel kristal

- Onderzoek onthult een nieuwe manier om de hechting van bevriezingsdruppels te verbeteren of te verminderen
- Onderzoekers ontwikkelen oceaanlidar met dubbele golflengte voor oceaandetectie

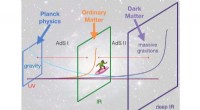
- Zouden massieve gravitonen levensvatbare kandidaten voor donkere materie kunnen zijn?
- Wetenschappers herzien optische constanten van ultradunne goudfilms

 Zinnen omzetten in media:kunnen we kunstmatige intelligentie leren waarnemen?
Zinnen omzetten in media:kunnen we kunstmatige intelligentie leren waarnemen? Soepele opeenvolging:Jack Ma komt uit een bloeiende Alibaba
Soepele opeenvolging:Jack Ma komt uit een bloeiende Alibaba Trump kan de koolstofmarkt voor klimaatverandering in Californië niet verzwakken, federale rechter regels
Trump kan de koolstofmarkt voor klimaatverandering in Californië niet verzwakken, federale rechter regels Opinie:het is onzin om te zeggen dat fracking veilig kan worden gemaakt, welke richtlijnen we ook bedenken
Opinie:het is onzin om te zeggen dat fracking veilig kan worden gemaakt, welke richtlijnen we ook bedenken Hoe de sterke kracht de zwaartekrachtgolfachtergrond beïnvloedt
Hoe de sterke kracht de zwaartekrachtgolfachtergrond beïnvloedt  De dunste cd-rw:gegevensopslag op atomaire schaal mogelijk
De dunste cd-rw:gegevensopslag op atomaire schaal mogelijk NASA berekende zware regenval die leidde tot modderstromen in Californië
NASA berekende zware regenval die leidde tot modderstromen in Californië Inzichten uit Oeganda over waarom straatverlichting op zonne-energie zinvol is
Inzichten uit Oeganda over waarom straatverlichting op zonne-energie zinvol is
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

