
Wetenschap
Kunstmatige vorming van peptidebindingen geeft aanwijzingen voor het creëren van leven op aarde
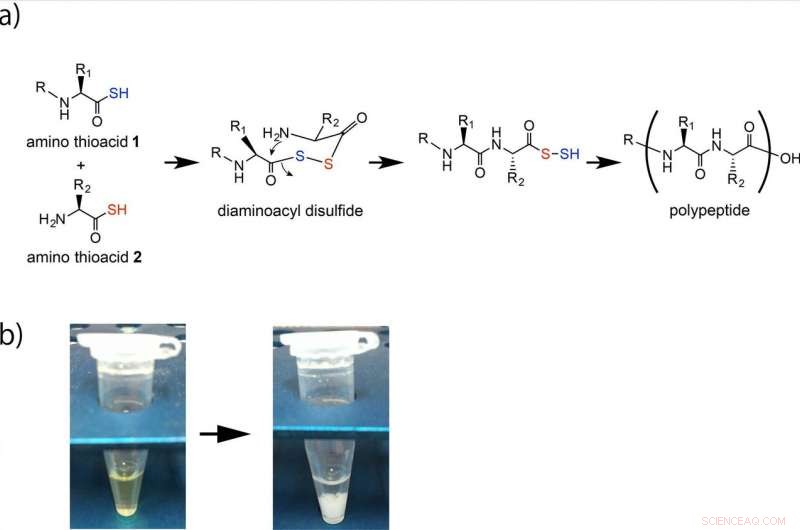
Polypeptidevorming door de oxidatieve reactie van aminothiozuren. (a) Aminothiozuren 1 en 2 zijn gekoppeld via een diaminoacyldisulfide-tussenproduct en daaropvolgende intramoleculaire amidevorming genereert een alfa-amidebinding. IJzererts of Fe2O3 in zure oplossing versnelt deze polypeptidevorming. De repetitieve uitvoering van deze reactie levert het polypeptide op. (b) Het polypeptide wordt gevormd als een wit neerslag. Krediet:Universiteit van Osaka
De belangrijkste bestanddelen van cellen, zakdoek, organen, en hele organismen zijn eiwitten, die worden opgebouwd door de ene na de andere aminozuren toe te voegen om lange eiwitketens te vormen die polypeptiden worden genoemd. Hoewel levende cellen geavanceerde machines hebben die deze kettingverlenging met verbazingwekkende snelheid en nauwkeurigheid kunnen bereiken, pogingen om deze reactie in het laboratorium na te bootsen om natuurlijke peptideproducten of peptidegeneesmiddelen te maken, zijn in vergelijking daarmee ruw en arbeidsintensief gebleven.
Met behulp van varianten van aminozuren genaamd aminothiozuren, een team van de universiteit van Osaka heeft deze moeilijkheden overwonnen om de nauwkeurige en eenvoudige verlenging van peptideketens in een snelle reactie te bereiken. Hun werk, gepubliceerd in het tijdschrift Biochemie , suggereert ook dat, miljarden jaren geleden, dit specifieke chemische mechanisme had ervoor kunnen zorgen dat er een overvloed aan grotere, complexere moleculen verscheen, mogelijk de voorwaarden verschaft waaruit het leven uiteindelijk is voortgekomen.
In dit onderzoek, het team concentreerde zich op het verbeteren van eerdere inspanningen om polypeptiden kunstmatig te synthetiseren, waarin een belangrijk obstakel de noodzaak was om beschermende groepen op te nemen. Dergelijke beschermende groepen worden toegevoegd aan functionele groepen binnen een molecuul om ervoor te zorgen dat een volgende reactie specifiek is. Echter, ze vereisen dat meerdere reactiestadia worden uitgevoerd, wat de procedure inefficiënt maakt.
"In onze inspanningen om de vorming van kunstmatige peptidebindingen te verbeteren, in plaats van zich te concentreren op aminozuren, we keken in plaats daarvan naar aminothiozuren, die een zwavelatoom bevatten, " zegt Yasuhiro Kajihara. "We zijn begonnen met de aminothiozuurversie van fenylalanine als monomeer, en onder een reactie die slechts vijf minuten duurde, werden peptideketens gevormd die twee tot vijf fenylalanines bevatten. Een alternatieve analyse onthulde ketens zo lang als 12 fenylalanines."
Een beeld van polypeptidevorming door aminothiozuren op het oppervlak van ijzererts in zure oplossing. Krediet:Universiteit van Osaka
Het team toonde vervolgens aan dat de peptideketenverlenging plaatsvond met mengsels van aminothiozuren en ook alleen onder zure omstandigheden, wat suggereerde dat oxidatie de sleutel was tot het betrokken mechanisme. Het team bevestigde dit door de reactie te karakteriseren, en toonde ook aan dat het een uniek reactietussenproduct betrof, die ervoor zorgde dat het beoogde product nauwkeurig werd gegenereerd.
"Aangezien de uitbreiding van reguliere aminozuren in ketens een sleutelfactor is voor het leven, we vroegen ons af of miljarden jaren geleden, aminothiozuren hadden kunnen werken als een voorloper van de meer complexe chemie die leidde tot de ontwikkeling van bewust leven, gezien hun snelle en eenvoudige integratie in ketens, " zegt hoofdauteur Ryo Okamoto. "We ontdekten dat de oligomerisatiereactie ook verliep onder chemische omstandigheden die lijken op die op aarde voordat het leven ontstond, met behulp van reactiecomponenten zoals ijzererts en zwavelzuur, die zou kunnen zijn gegenereerd uit vulkanisch gas."
Het werk van het team biedt dus niet alleen een efficiënt laboratoriuminstrument voor een reeks praktische toepassingen, maar ook een potentieel kijkje in de chemie van waaruit het leven begon.
 Waterafdichtingsprojecten van de tweede graad
Waterafdichtingsprojecten van de tweede graad  Virushydrofobiciteit kan helpen bij het zuiveren van vaccins
Virushydrofobiciteit kan helpen bij het zuiveren van vaccins Onderzoekers ontwikkelen nieuwe röntgendetectietechnologie
Onderzoekers ontwikkelen nieuwe röntgendetectietechnologie Eerste direct bewijs van chemische reacties in deeltjes
Eerste direct bewijs van chemische reacties in deeltjes Een antibioticum dat zich voordoet als een natuurlijke verbinding in de gigantische Madeiraanse squill
Een antibioticum dat zich voordoet als een natuurlijke verbinding in de gigantische Madeiraanse squill
 Zowel de beroemde Hope-diamant als de Britse kroonjuweeldiamanten, kan superdiep zijn
Zowel de beroemde Hope-diamant als de Britse kroonjuweeldiamanten, kan superdiep zijn Besturingsalgoritmen kunnen met sensoren beladen ballonnen een week lang in orkanen drijven
Besturingsalgoritmen kunnen met sensoren beladen ballonnen een week lang in orkanen drijven NASA ziet Flossie nu een overblijfsel van lagedrukgebied
NASA ziet Flossie nu een overblijfsel van lagedrukgebied Hoe zijn schelpen gevormd?
Hoe zijn schelpen gevormd?  Voorschoolse lessen die de delen van een bloem onderwijzen
Voorschoolse lessen die de delen van een bloem onderwijzen
Hoofdlijnen
- Plantenpathologen ontdekken ongebruikelijke evolutionaire overgang in gewone bacteriën
- Invasieve planten hebben een ongekend vermogen om nieuwe continenten en klimaten te verkennen
- De toekomst van gewastechniek
- Chromosomale afwijkingen: wat is het?, Typen en oorzaken
- Interessante feiten over DNA-vingerafdrukken
- Vrouwelijke wetenschappers die de wereld veranderden
- Duplicaties van niet-coderend DNA kunnen de evolutie van mensspecifieke eigenschappen hebben beïnvloed
- Lignine-afval aangepast voor industrieel gebruik van bio-olie
- How Do Living Things Grow?
- Draagbare sensoren die gaslekken detecteren

- Zijdevezels kunnen hightech natuurlijke metamaterialen zijn

- Wetenschappers stellen voor om meta-oppervlakken van gouden nanodeeltjes te gebruiken om de moleculaire samenstelling van de stof te bepalen

- Op katoen gebaseerde hybride biobrandstofcel kan implanteerbare medische apparaten van stroom voorzien

- Hybride katalysator met hoge enantiomeerselectiviteit
 Hoe gram te converteren naar droge ounces
Hoe gram te converteren naar droge ounces  Amerikanen die de financiële stress vergroten, zullen het coronavirus een stuk moeilijker te bevatten maken
Amerikanen die de financiële stress vergroten, zullen het coronavirus een stuk moeilijker te bevatten maken Solide autoverkopen in de VS in 2019 onderstrepen de kracht van de consument
Solide autoverkopen in de VS in 2019 onderstrepen de kracht van de consument Voordelen en nadelen van Honeybees
Voordelen en nadelen van Honeybees Nieuw ontdekte magnetische toestand kan leiden tot groene IT-oplossingen
Nieuw ontdekte magnetische toestand kan leiden tot groene IT-oplossingen Bemanning ruimtestation verhuist Sojoez om plaats te maken voor nieuwe bemanningsleden
Bemanning ruimtestation verhuist Sojoez om plaats te maken voor nieuwe bemanningsleden Onderzoekers simuleren een magnetische storm uit 1770 met behulp van gegevens uit historische documentatie
Onderzoekers simuleren een magnetische storm uit 1770 met behulp van gegevens uit historische documentatie Magische hoek grafeen en het creëren van onverwachte topologische kwantumtoestanden
Magische hoek grafeen en het creëren van onverwachte topologische kwantumtoestanden
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

