
Wetenschap
Vriespuntdaling berekenen:benzeen in chloroform
1. Begrijp het concept
* Vriespuntdaling: Wanneer een niet-vluchtige opgeloste stof (zoals benzeen) wordt opgelost in een oplosmiddel (zoals chloroform), neemt het vriespunt van de oplossing af in vergelijking met het zuivere oplosmiddel.
* Vriespuntdepressievergelijking: ΔTf =Kf * m
* ΔTf =Verandering in vriespunt
* Kf =Cryoscopische constante van het oplosmiddel (voor chloroform, Kf =4,68 °C/m)
* m =Molaliteit van de oplossing (mol opgeloste stof per kg oplosmiddel)
2. Bereken de molaliteit (m)
* Molen benzeen:
* Molaire massa van benzeen (C6 H6 ) =78,11 g/mol
* Mol benzeen =(2,50 g) / (78,11 g/mol) =0,0320 mol
* Massa van chloroform in kg:
* 120 gram =0,120 kg
* Molaliteit:
* m =(0,0320 mol) / (0,120 kg) =0,267 mol/kg
3. Bereken de verandering in het vriespunt (ΔTf )
* ΔTf =(4,68 °C/m) * (0,267 mol/kg) =1,25 °C
4. Bepaal het vriespunt van de oplossing
* Vriespunt van zuivere chloroform: -63,5 °C
* Vriespunt van de oplossing: -63,5 °C - 1,25 °C =-64,75 °C
Daarom is het vriespunt van de oplossing die 2,50 g benzeen in 120 g chloroform bevat, -64,75 °C.
 Hoeveel valentie -elektronen moet stikstof vol zijn?
Hoeveel valentie -elektronen moet stikstof vol zijn?  Snel, nauwkeurig en niet-destructief:de nieuwe methode om voedselkwaliteit te analyseren
Snel, nauwkeurig en niet-destructief:de nieuwe methode om voedselkwaliteit te analyseren Is chemische reactiviteit een kenmerk van eigendom?
Is chemische reactiviteit een kenmerk van eigendom?  Is waterstofsulfide een element of een verbinding?
Is waterstofsulfide een element of een verbinding?  Wanneer water in stoom verandert, ondergaat het een chemische verandering. Waar of niet waar?
Wanneer water in stoom verandert, ondergaat het een chemische verandering. Waar of niet waar?
 Hoe wereldwijde voedselsystemen duurzamer te maken
Hoe wereldwijde voedselsystemen duurzamer te maken Oude vulkanen hebben ooit koolstof in de oceaan gestimuleerd, maar mensen zijn nu veel sneller dan hen
Oude vulkanen hebben ooit koolstof in de oceaan gestimuleerd, maar mensen zijn nu veel sneller dan hen Om stranden te versterken, gewoon zand toevoegen?
Om stranden te versterken, gewoon zand toevoegen? Kleine kristallen dichten gaten en beperken de opname van verontreinigingen in gesteenten
Kleine kristallen dichten gaten en beperken de opname van verontreinigingen in gesteenten Kokende hitte en geen water:kranen lopen droog in Zuid-Irak
Kokende hitte en geen water:kranen lopen droog in Zuid-Irak
Hoofdlijnen
- Hoe evolueren genomen tussen soorten? Team onderzoekt de sleutelrol van 3D-structuur in mannelijke geslachtscellen
- Waarom zijn micro -organismen belangrijk in oceaanketens?
- Welk lichaamssysteem houdt menselijke soorten op deze planeet?
- Wat is een carnivoor in de eerste orde?
- Wat zijn enkele voorbeelden van levende organismen?
- Wat zijn ribosomen bij mensen?
- Wie moet eerst een biologische observatie van microscoop opnemen?
- Monoculturen of gemengde soorten? Nieuw onderzoek laat zien hoe verschillende bossen omgaan met droogte
- Cicade-palooza! Miljarden insecten om Amerika te bedekken
- Uranium onthult zijn ware aard

- Verbetering van methoden voor het afleveren van genen

- Voedingswetenschappers vinden de sleutel tot perfect gladde chocolade

- Team combineert geavanceerde modellering met 300 jaar oude statistische analysetechniek om materiaaleigenschappen te verbeteren

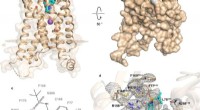
- Studie onthult structuur van receptor die betrokken is bij diabetes type 2 en meer
 Welke wetenschapper bestudeert levende organismen te klein om met het blote oog te worden gezien?
Welke wetenschapper bestudeert levende organismen te klein om met het blote oog te worden gezien?  Onderzoeksbewijs onthult misbruik van Holocaust-datasets
Onderzoeksbewijs onthult misbruik van Holocaust-datasets Hete rotsen, geen warme sfeer, leidde tot relatief recente door water uitgesleten valleien op Mars
Hete rotsen, geen warme sfeer, leidde tot relatief recente door water uitgesleten valleien op Mars Robotleraren vallen Chinese kleuterscholen binnen
Robotleraren vallen Chinese kleuterscholen binnen Taal die op creditcardwebsites wordt gebruikt, is het moeilijkst te begrijpen
Taal die op creditcardwebsites wordt gebruikt, is het moeilijkst te begrijpen Fort Lauderdale overweegt wegen te verhogen om de stijgende zeeën te bestrijden
Fort Lauderdale overweegt wegen te verhogen om de stijgende zeeën te bestrijden  Groeiende algenbloei in Arabische Zee gekoppeld aan klimaatverandering
Groeiende algenbloei in Arabische Zee gekoppeld aan klimaatverandering Hoe veranderen maden in vliegen?
Hoe veranderen maden in vliegen?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

