
Wetenschap
Azijnzuur- en zuiveringszoutreactie:chemie uitgelegd
* Kooldioxidegas (CO2): Dit is het gas dat het bruisen en borrelen veroorzaakt dat je ziet.
* Natriumacetaat: Dit is een zout dat in oplossing blijft.
* Water (H2O): Dit ontstaat ook bij de reactie.
De chemische vergelijking voor deze reactie is:
CH3COOH (azijnzuur) + NaHCO3 (natriumbicarbonaat) → CO2 (kooldioxide) + H2O (water) + CH3COONa (natriumacetaat)
Dit is wat er gebeurt:
1. Zuur-base-reactie: Azijnzuur is een zuur en natriumbicarbonaat is een base. Wanneer ze reageren, neutraliseren ze elkaar, waarbij een zout (natriumacetaat) en water ontstaat.
2. Afbraak van bicarbonaat: Het bicarbonaation (HCO3-) valt uiteen in kooldioxidegas (CO2) en water (H2O). Daarom zie je het bruisen en borrelen.
De reactie is exotherm, wat betekent dat er warmte vrijkomt. Het kan zijn dat u voelt dat de container enigszins opwarmt.
Toepassingen:
Deze reactie heeft vele toepassingen, waaronder:
* Bakken: Zuiveringszout wordt vaak gebruikt in bakrecepten in combinatie met een zuur ingrediënt zoals azijn, karnemelk of citroensap om een rijsmiddel te creëren dat gebakken producten laat rijzen.
* Reiniging: De bruisende werking kan worden gebruikt voor reinigingsdoeleinden, zoals het verwijderen van vlekken of het ontstoppen van afvoeren.
* Wetenschappelijke experimenten: Het is een populaire demonstratie in de scheikundeles om zuur-base-reacties te illustreren.
Veiligheid:
Hoewel de reactie over het algemeen veilig is, is het belangrijk om verdund azijnzuur (zoals azijn) en kleine hoeveelheden zuiveringszout te gebruiken. De reactie kan behoorlijk krachtig zijn, vooral bij hogere concentraties reactanten. Zorg ervoor dat het mengsel niet overstroomt of spettert.
 Het grootste deel van het volume van een atoom wordt ingenomen door de ruimte die nodig is, waarvoor?
Het grootste deel van het volume van een atoom wordt ingenomen door de ruimte die nodig is, waarvoor?  In ionische verbindingen moeten de som van de aanklachten alle kationen en anionen zijn?
In ionische verbindingen moeten de som van de aanklachten alle kationen en anionen zijn?  Synthesereacties uitgelegd:hoe twee of meer reactanten een nieuwe verbinding vormen
Synthesereacties uitgelegd:hoe twee of meer reactanten een nieuwe verbinding vormen  Waarom zijn metaaloxides amfoteer van aard?
Waarom zijn metaaloxides amfoteer van aard?  Thermische dynamica experimenten voor kinderen
Thermische dynamica experimenten voor kinderen
 Nieuwe studie toont aan dat microplastics knooppunten worden voor ziekteverwekkers antibiotica-resistente bacteriën
Nieuwe studie toont aan dat microplastics knooppunten worden voor ziekteverwekkers antibiotica-resistente bacteriën Welke fysieke effecten hebben tornado's op dieren in het wild?
Welke fysieke effecten hebben tornado's op dieren in het wild?  Levensduur van Fungus
Levensduur van Fungus Waarom vergelijkt Housman het leven met het bloeien van een liefste bomen van kersenboom nu?
Waarom vergelijkt Housman het leven met het bloeien van een liefste bomen van kersenboom nu?  Globale analyse toont ongekende schaal van Australische vuurzomer
Globale analyse toont ongekende schaal van Australische vuurzomer
Hoofdlijnen
- Waarom zijn prokaryoten ouder dan eukaryoten?
- Wetenschappers ontdekken hoe twee eiwitten helpen cellen gezond te houden
- Naar welke Gruop van dieren behoren de spinnen?
- De symbolische aap? Door tokens gemedieerde economische keuzes in getufte kapucijnen
- Wat zijn eerstelijns verdedigingen tegen pathogenen in het algemeen?
- Het celmembraan bevat lipidemoleculen die?
- Wat is autotrofe en heterotrofe?
- Wat betekent in de wetenschap?
- Wat is het domein van prokaryoten?
- Bacteriën helpen bij het maken van caloriearme suiker

- Nieuwe antibacteriële geneesmiddelen ontwikkeld aan de Universiteit van Oost-Finland
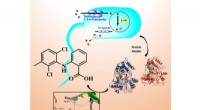
- Nieuwsgierige in elkaar grijpende moleculen vertonen een dubbele respons
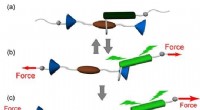
- Onderzoekers creëren eerste draagbare technologie voor het detecteren van cyanotoxinen in water

- Bouw van betere biosensoren in de gasfase voor de bestrijding van ziekten
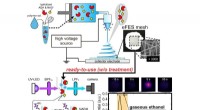
 Wat is sterker NaOH of NH3?
Wat is sterker NaOH of NH3?  Hoe elektriciteit wordt geproduceerd bij energiecentrales?
Hoe elektriciteit wordt geproduceerd bij energiecentrales?  Waarom is er zoveel mos in polaire regio's?
Waarom is er zoveel mos in polaire regio's?  Waarom magnesiumhydroxide gebruikt als een antacida in tegenstelling tot calciumhydroxide?
Waarom magnesiumhydroxide gebruikt als een antacida in tegenstelling tot calciumhydroxide?  Hoe wordt het klimaat beïnvloed door hoogte?
Hoe wordt het klimaat beïnvloed door hoogte?  Moderne gezinsrollen verbeteren de levenstevredenheid van ouders
Moderne gezinsrollen verbeteren de levenstevredenheid van ouders Wat betekent kinetisch werk?
Wat betekent kinetisch werk?  Bundelmers (nieuwe polymeereenheden) kunnen industrieën transformeren
Bundelmers (nieuwe polymeereenheden) kunnen industrieën transformeren
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

