
Wetenschap
Chloorgas versus waterstofgas:vergelijking en uitleg van reactiviteit
* Elektronegativiteit: Chloor is veel elektronegatiever dan waterstof. Dit betekent dat chloor een sterkere aantrekkingskracht heeft op elektronen.
* Verbindingssterkte: De binding tussen twee chlooratomen in Cl₂ is zwakker dan de binding tussen twee waterstofatomen in H₂. Dit betekent dat het gemakkelijker is om de Cl-Cl-binding te verbreken en nieuwe bindingen met andere elementen te vormen.
* Elektronenaffiniteit: Chloor heeft een hoge elektronenaffiniteit, wat betekent dat het gemakkelijk elektronen opneemt om negatieve ionen (Cl⁻) te vormen. Dit maakt het een sterk oxidatiemiddel.
Samengevat: De hoge elektronegativiteit van chloor, de zwakke bindingssterkte en de sterke elektronenaffiniteit dragen allemaal bij aan de veel hogere reactiviteit ervan in vergelijking met waterstof.
Belangrijke opmerking: Hoewel chloor reactiever is, is waterstofgas zeer brandbaar en kan het explosief reageren met zuurstof. Met beide gassen moet uiterst voorzichtig worden omgegaan.
 Fossiele soorten van Quokka-formaat laten voor de vierde keer zien dat kangoeroes evolueren om bladeren te eten
Fossiele soorten van Quokka-formaat laten voor de vierde keer zien dat kangoeroes evolueren om bladeren te eten  Wat zijn de goede houdingen van wetenschappers?
Wat zijn de goede houdingen van wetenschappers?  Japans ANA streeft naar koolstofneutraliteit in 2050
Japans ANA streeft naar koolstofneutraliteit in 2050 Onderzoekers bepalen één bron van een krachtig broeikasgas
Onderzoekers bepalen één bron van een krachtig broeikasgas Grondschudden tijdens verwoestende overstroming biedt nieuwe inzichten
Grondschudden tijdens verwoestende overstroming biedt nieuwe inzichten
Hoofdlijnen
- Wat wordt virale DNA opgenomen in bacterie?
- Wat is een oplossing zonder micro -organismen?
- Waarom gebruiken biologen vlekken om cellen te bestuderen?
- Wat is Bacteriuria?
- Het diploïde getal begrijpen:wat het betekent voor de genetica
- Wat zijn feiten over schimmels?
- Waarom is longen het lichtste orgaan in het menselijk lichaam?
- Waar is het membraan van alle cellen van gemaakt?
- Hoe u het hart van uw hond gezond kunt houden
- Analyseren van de voor- en nadelen van twee composietproductiemethoden

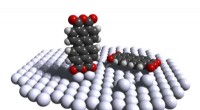
- Lastige prestatie met opstaand molecuul
- COVID-ademtesten - zou het de volgende kunnen zijn? Onderzoek zegt ja

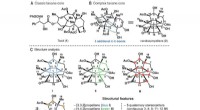
- Eindelijk synthetisch canataxpropellane:een van de meest complexe producten van de natuur reproduceren
- Kunstmatige bladeren uit het lab de lucht in verplaatsen

 Sound Wave-wetenschapsprojecten
Sound Wave-wetenschapsprojecten  Wat is de naam van de wetenschap die bestudeert welke eigenschappen worden doorgegeven van ouders tot nakomelingen?
Wat is de naam van de wetenschap die bestudeert welke eigenschappen worden doorgegeven van ouders tot nakomelingen?  Onderzoek laat zien hoe beschadigde celkernen zichzelf opnieuw afsluiten en repareren
Onderzoek laat zien hoe beschadigde celkernen zichzelf opnieuw afsluiten en repareren  De evolutie van voedingsstrategieën bij oude krokodillen ontrafelen
De evolutie van voedingsstrategieën bij oude krokodillen ontrafelen Venus:de massa- en grootte-tweeling van de aarde – een nadere blik op hun verschillen
Venus:de massa- en grootte-tweeling van de aarde – een nadere blik op hun verschillen  NASA vindt Kiko verzwakking in de oostelijke Stille Oceaan
NASA vindt Kiko verzwakking in de oostelijke Stille Oceaan Wat is een samengestelde vorm?
Wat is een samengestelde vorm?  Wat is de uitleg van significantie begrijpen van cultuur zijn elementkenmerken en component?
Wat is de uitleg van significantie begrijpen van cultuur zijn elementkenmerken en component?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap & Ontdekkingen © https://nl.scienceaq.com

