
Wetenschap
Waarom zijn molecuul stabiel?
Hier is een uitsplitsing van de redenen voor moleculaire stabiliteit:
1. Chemische binding:
* Covalente binding: Atomen delen elektronen om een stabiele elektronenconfiguratie te bereiken, zoals een edelgas. Dit gedeelde elektronenpaar houdt de atomen bij elkaar en vormt een stabiel molecuul.
* ionische binding: Het ene atoom verliest elektronen en wordt positief geladen (kation), terwijl een ander elektronen krijgt en negatief wordt geladen (anion). De elektrostatische aantrekkingskracht tussen tegengestelde ladingen houdt de ionen bij elkaar en vormt een stabiele ionische verbinding.
* Metallic binding: Elektronen worden gedelokaliseerd en beweegt vrij door een rooster met metaalatomen. Deze "zee" van elektronen bindt de atomen samen, waardoor een sterke, stabiele structuur ontstaat.
2. Lagere energietoestand:
* Wanneer atomen verbinden om een molecuul te vormen, bereiken ze een lagere energietoestand in vergelijking met wanneer ze worden geïsoleerd. Dit komt omdat de elektronen die betrokken zijn bij de binding stabieler zijn in hun nieuwe configuratie.
* De afgifte van energie tijdens de vorming van bindingen (exotherme reactie) geeft aan dat het molecuul stabieler is dan de individuele atomen.
3. Octetregel:
* De octetregel stelt dat atomen de neiging hebben om elektronen te winnen, verliezen of delen om een stabiele configuratie te bereiken met acht elektronen in hun buitenste schaal. Dit is een vereenvoudigde verklaring, maar het helpt de stabiliteit van veel moleculen te begrijpen.
4. Afstotingen en attracties:
* De balans tussen aantrekkelijke en afstotende krachten tussen atomen is cruciaal voor stabiliteit.
* Afstotende krachten bestaan tussen de positief geladen kernen van atomen. Deze krachten worden echter overwonnen door de sterke aantrekkelijke krachten van chemische bindingen.
5. Moleculaire vorm:
* De vorm van een molecuul kan ook de stabiliteit ervan beïnvloeden.
* Bijvoorbeeld, bepaalde vormen zorgen voor effectievere elektronenuitwisseling en minimaliseren elektronenafstandingen, wat leidt tot een grotere stabiliteit.
Belangrijke opmerking: Hoewel de meeste moleculen stabiel zijn onder normale omstandigheden, kunnen bepaalde omstandigheden zoals hoge temperatuur of druk ervoor zorgen dat moleculen afbreken.
Concluderend komt moleculaire stabiliteit voort uit de sterke aantrekkelijke krachten tussen atomen, wat resulteert in een lagere energietoestand en een stabielere elektronenconfiguratie. Chemische binding, de octetregel en de balans tussen weerzinwekkende en aantrekkelijke krachten spelen allemaal een cruciale rol bij het bereiken van moleculaire stabiliteit.
 Klimaatveranderingen veroorzaakten immigratie naar Amerika in de 19e eeuw
Klimaatveranderingen veroorzaakten immigratie naar Amerika in de 19e eeuw Tsunami's in het meer vormen een aanzienlijke bedreiging in het opwarmende klimaat
Tsunami's in het meer vormen een aanzienlijke bedreiging in het opwarmende klimaat  Zeebodemdieren onderzoeken voor offshore hernieuwbare energie
Zeebodemdieren onderzoeken voor offshore hernieuwbare energie Een van 's werelds meest afgelegen onbewoonde eilanden is letterlijk bedekt met onze prullenbak
Een van 's werelds meest afgelegen onbewoonde eilanden is letterlijk bedekt met onze prullenbak  Verzuring van de oceaan veroorzaakt osteoporose van koraal op iconische riffen
Verzuring van de oceaan veroorzaakt osteoporose van koraal op iconische riffen
Hoofdlijnen
- Wat is het verschil tussen een bacterie en een virus?
- Wat is de koloniemorfologie voor Pseudomonas fluorescens?
- Waar worden lysosomen gevonden in een plantencel?
- Wat zijn de 2 dingen die nodig zijn om evolutie te laten plaatsvinden?
- 'S Werelds kleinste bandrecorder is gemaakt van microben
- Wat zijn de functies van Triglyceride Phospholipid & Sterol?
- Wat zijn de belangrijkste verschillen tussen plantencellen en dierlijke cellen?
- Wat is de eigenschap van isolaten tegen Cold Survival Advantange?
- Welke leden van de Phyla -specie zijn parasieten mensen?
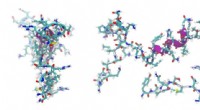
- Onderzoekers ontwikkelen een nieuw peptidesysteem voor gericht transport van moleculen naar levende zoogdiercellen
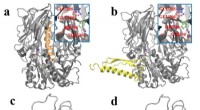
- Nieuwe glucagon-achtige peptide-1 medicijnen ontworpen voor diabetes type 2
- Het bouwen van zetmeelruggengraat voor in het laboratorium gekweekt vlees met behulp van Lego-stukken

- Hoe kunstmatige nanofabrieken te bouwen om onze toekomst van energie te voorzien?

- Ervoor zorgen dat broccolispruiten hun kankerbestrijdende stoffen behouden

 Feestelijke traktatie voor sterrenkijkers terwijl Geminid-meteoren pieken
Feestelijke traktatie voor sterrenkijkers terwijl Geminid-meteoren pieken Hoe worden de sterren in een sterrenbeeld genoemd?
Hoe worden de sterren in een sterrenbeeld genoemd?  'Wat als er een stoere Barbie bestond?' Barbie's genderpolitiek onderzocht
'Wat als er een stoere Barbie bestond?' Barbie's genderpolitiek onderzocht  De magnetische eigenschappen van stervormende dichte kernen
De magnetische eigenschappen van stervormende dichte kernen Waarom zijn er niet elke maand verduisteringen?
Waarom zijn er niet elke maand verduisteringen?  In meercellige organismen zijn er verschillende soorten cellen die zich in weefsels en organen hebben georganiseerd om speciale functies uit te voeren. Wat is de functie van een huidcel?
In meercellige organismen zijn er verschillende soorten cellen die zich in weefsels en organen hebben georganiseerd om speciale functies uit te voeren. Wat is de functie van een huidcel?  De Einstein-sonde opent zijn grote ogen voor de röntgenhemel
De Einstein-sonde opent zijn grote ogen voor de röntgenhemel  Mondiale rivierdelta's worden steeds meer door mensen gevormd, studie zegt:
Mondiale rivierdelta's worden steeds meer door mensen gevormd, studie zegt:
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

