
Wetenschap
Wat zijn de overeenkomsten en verschillen tussen inerte gassen van halogeenfamilie?
halogeenfamilie
* elementen: Fluor (F), chloor (CL), bromine (Br), jodium (i), astatine (AT)
* Locatie op periodieke tabel: Groep 17 (VIIA)
* eigenschappen: Zeer reactieve niet -metalen, hebben de neiging om één elektron te krijgen om negatief geladen ionen (anionen) te vormen, zouzouten met metalen vormen.
inerte gassen (edelgassen)
* elementen: Helium (HE), Neon (NE), Argon (AR), Krypton (KR), Xenon (XE), Radon (RN)
* Locatie op periodieke tabel: Groep 18 (VIIIA)
* eigenschappen: Extreem niet -reactief, hebben volledige buitenste elektronenschalen, bestaan als individuele atomen, historisch beschouwd als inert (maar sommige kunnen verbindingen vormen onder specifieke omstandigheden).
overeenkomsten:
* beide zijn niet -metalen: Ze missen de metalen eigenschappen van andere elementen.
* beide bestaan als gassen bij kamertemperatuur: Hoewel sommige halogenen vloeistoffen of vaste stoffen kunnen zijn onder specifieke omstandigheden.
* beide bevinden zich in de meest rechtse kolommen van de periodiek systeem.
Verschillen:
* Reactiviteit: Halogenen zijn zeer reactief, terwijl edelgassen uiterst niet -reactief zijn.
* Elektronenconfiguratie: Halogenen hebben zeven elektronen in hun buitenste schaal, terwijl edelgassen er acht hebben (behalve voor helium, dat twee heeft).
* ionen: Halogenen vormen meestal negatief geladen ionen (anionen), terwijl edelgassen zelden ionen vormen.
* Samengestelde vorming: Halogenen vormen gemakkelijk verbindingen met andere elementen, terwijl edelgassen historisch als inert werden beschouwd, maar kunnen verbindingen vormen onder specifieke omstandigheden.
Key Takeaway: Halogenen en edelgassen zijn verschillende families met verschillende chemische eigenschappen en reactiviteit. Hoewel ze beide niet -metalen zijn en bestaan als gassen bij kamertemperatuur, zijn hun reactiviteit en elektronenconfiguraties aanzienlijk verschillend.
 Mexico herdenkt twee verjaardagen van dodelijke aardbevingen
Mexico herdenkt twee verjaardagen van dodelijke aardbevingen Het mysterie oplossen waarom de koolstofdioxide in de atmosfeer tijdens ijstijden lager was
Het mysterie oplossen waarom de koolstofdioxide in de atmosfeer tijdens ijstijden lager was Schoolverzuim correleert met verminderde luchtkwaliteit
Schoolverzuim correleert met verminderde luchtkwaliteit Duurzaamheid van het voedselsysteem vereist een lager energieverbruik
Duurzaamheid van het voedselsysteem vereist een lager energieverbruik NASA-ogen intensiveren tropische cycloon Frances
NASA-ogen intensiveren tropische cycloon Frances
Hoofdlijnen
- Kan pizzakruid winterbraakziekte voorkomen?
- Waarom heb je enzymen in je lichaam nodig?
- Welke mensen zijn erg vatbaar voor ziektekiemen?
- Bij de VN is overeenstemming bereikt over het biopiraterijverdrag
- Wat produceert in de hersenen secreties die de lichaamsfunctie regelen?
- Hoe grootte cellen splitst:Cellen meten het oppervlak om te weten wanneer ze delen
- Welk chemisch proces gebruiken dieren om voedingsstoffen af te breken in een vorm die door het lichaam kan worden gebruikt?
- Onderzoeker laat zien hoe kegelslakken een gifklier ontwikkelden uit reserve darmdelen
- Hoe zijn zowel een bewerkingen als een gevolgtrekking hoe ze verschillen?
- Chemische sondes maken de weg vrij voor een beter begrip van de ontwikkeling van ziekten
- Onderzoekers kunnen gaatjes aanpassen in nieuw poreus materiaal

- Een nieuwe manier om de cel binnen te gaan met behulp van superchaotrope eigenschappen van boorclusters
- Smartphonelab levert testresultaten in een oogwenk

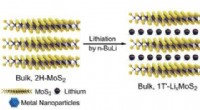
- Waterstofproductie in een besloten ruimte
 Zonder de Noord-Amerikaanse moesson, Bosbranden in bedwang houden wordt moeilijker
Zonder de Noord-Amerikaanse moesson, Bosbranden in bedwang houden wordt moeilijker Invasieve regenwormen aan de basis van de achteruitgang van suikeresdoorn
Invasieve regenwormen aan de basis van de achteruitgang van suikeresdoorn De rots die het meest waarschijnlijk fossielen bevat
De rots die het meest waarschijnlijk fossielen bevat Hoe kwik in de zee komt
Hoe kwik in de zee komt Bodembedekkers kunnen de wintertemperaturen in Noord-Amerika verhogen
Bodembedekkers kunnen de wintertemperaturen in Noord-Amerika verhogen Wat kan nog meer veranderen in een vloeistof van vaste tot vloeistof?
Wat kan nog meer veranderen in een vloeistof van vaste tot vloeistof?  Populaire films boeken onvoldoende vooruitgang in de richting van inclusie, vondsten melden
Populaire films boeken onvoldoende vooruitgang in de richting van inclusie, vondsten melden Methode van mechanische ingenieurs om de groei van op carbonaat gebaseerde kristallen in PNAS . te beheersen
Methode van mechanische ingenieurs om de groei van op carbonaat gebaseerde kristallen in PNAS . te beheersen
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

