
Wetenschap
Combinaties van stoffen met zuurstof bekend als?
Hier is een uitsplitsing:
* oxidatie: Het chemische proces waarbij een stof combineert met zuurstof.
* oxide: De resulterende verbinding gevormd door de combinatie van een stof met zuurstof.
Voorbeelden van oxiden:
* ijzeroxide (fe₂o₃) , algemeen bekend als roest.
* koolstofdioxide (co₂) , een gas geproduceerd door ademhaling en verbranding.
* water (h₂o) , gevormd door de reactie van waterstof met zuurstof.
* siliciumdioxide (Sio₂) , het belangrijkste onderdeel van zand.
Oxiden kunnen worden geclassificeerd op basis van hun chemische eigenschappen en het type binding:
* metalen oxiden: Gevormd door metalen die reageren met zuurstof (bijv. IJzeroxide, calciumoxide).
* Niet-metalen oxiden: Gevormd door niet -metalen die reageren met zuurstof (bijv. Koolstofdioxide, zwaveldioxide).
* amfoterische oxiden: Kan werken als zowel zure als basische oxiden (bijv. Aluminiumoxide, zinkoxide).
Oxiden spelen een cruciale rol in verschillende natuurlijke en industriële processen, waaronder:
* Corrosie: De verslechtering van metalen als gevolg van oxidatie.
* verbranding: De snelle reactie van een stof met zuurstof, waardoor warmte en licht vrijgeeft.
* ademhaling: Het proces waarbij levende organismen zuurstof gebruiken om energie te produceren.
* productie: Oxiden worden gebruikt in verschillende industrieën, zoals keramiek, glas en cementproductie.
 Wat is de elektronencapaciteit van de tweede schil?
Wat is de elektronencapaciteit van de tweede schil?  Hoeveel verschil is er tussen de energie die vrijkomt tijdens chemische reactie en nucleaire reacties?
Hoeveel verschil is er tussen de energie die vrijkomt tijdens chemische reactie en nucleaire reacties?  Wat is niet -beperkende reactant uitgelegd met een geschikt voorbeeld?
Wat is niet -beperkende reactant uitgelegd met een geschikt voorbeeld?  Welk zuur vormt geen anhydride bij verhitting?
Welk zuur vormt geen anhydride bij verhitting?  Wat is dialuminiumtrioxide?
Wat is dialuminiumtrioxide?
 Bewijsgestuurde manieren om gefocust te blijven wanneer je studeert
Bewijsgestuurde manieren om gefocust te blijven wanneer je studeert Ontwikkelingslanden moeten hun eigen koers uitstippelen naar netto nulemissie
Ontwikkelingslanden moeten hun eigen koers uitstippelen naar netto nulemissie Show in Londen verkent de verborgen wereld van gezichtsherkenning
Show in Londen verkent de verborgen wereld van gezichtsherkenning  Klimaatverandering kan leiden tot meer extreme hitte, ozonvervuilingsdagen naar het zuidoosten, onderzoekers zeggen:
Klimaatverandering kan leiden tot meer extreme hitte, ozonvervuilingsdagen naar het zuidoosten, onderzoekers zeggen: Wil je de kortste weg naar een goed leven? Probeer cynisme
Wil je de kortste weg naar een goed leven? Probeer cynisme
Hoofdlijnen
- Wat deden Hooke en Leewenhoek bij hun ontdekking van cellen?
- Terugkijken op de geschiktheid van het verhaal over het economisch beleid dat ten grondslag ligt aan de Groene Revolutie
- Wat zijn aldosen en ketosen?
- Hoe de jacht mensen tot langeafstandslopers heeft gemaakt
- Wat regelt de vorming van spil tijdens celdeling in plantencellen?
- Wat zijn de organismen ontdekt door Jose Rizal?
- Hoe succesvol te zijn in Microbiology
- 3D-analyse van hondenfossielen werpt licht op het debat over domesticatie
- Wat beïnvloedt een Trait Expression de meeste, genetica of de omgeving?
- Chemici synthetiseren platte siliciumverbindingen

- Nieuwe technologie heeft tot doel de levensduur van lithium-metaalbatterijen te verbeteren, veiligheid
- Probe schijnt licht op overactieve immuuncellen om te helpen detecteren, bepaalde vormen van kanker behandelen, auto-immuunziekten

- efficiënt, stabiele thermo-elektrische module op basis van hoogwaardige vloeistofachtige materialen

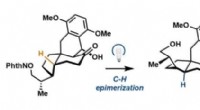
- Beknopte synthese van pleurotine ontwikkeld
 Eigenschappen van Ash Wood
Eigenschappen van Ash Wood  Impliceert de nieuwe slogan van Google een verschuiving naar zakelijke apps?
Impliceert de nieuwe slogan van Google een verschuiving naar zakelijke apps?  Jet in de atmosfeer van Jupiter blijkt in perioden van ongeveer vier jaar te fluctueren
Jet in de atmosfeer van Jupiter blijkt in perioden van ongeveer vier jaar te fluctueren  Sensorische gevarenzones:hoe sensorische vervuiling de overleving van dieren beïnvloedt
Sensorische gevarenzones:hoe sensorische vervuiling de overleving van dieren beïnvloedt  Volkswagen winst springt, maar grote uitdagingen voor de boeg
Volkswagen winst springt, maar grote uitdagingen voor de boeg Qatar tekent zonne-deal van $ 470 miljoen
Qatar tekent zonne-deal van $ 470 miljoen Nanotechnologie kan de Arabische regio helpen
Nanotechnologie kan de Arabische regio helpen Hoe wordt een darmmicrobe een ziekteverwekker?
Hoe wordt een darmmicrobe een ziekteverwekker?
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com

