Wetenschap
Chemici synthetiseren platte siliciumverbindingen
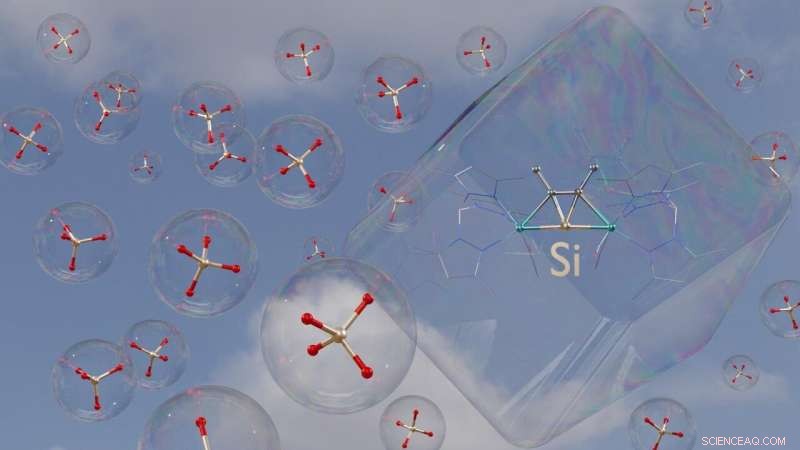
3D-weergave van een van de nieuwe moleculen. Silicaationen in tetraëdrische rangschikking zijn te zien in de bolvormige zeepbellen ter vergelijking. Krediet:Jens Rump / Universiteit van Bonn
Chemici van de Universiteit van Bonn (Duitsland) hebben buitengewoon ongebruikelijke verbindingen gesynthetiseerd. Hun centrale bouwsteen is een siliciumatoom. Anders dan normaal, echter, is de rangschikking van de vier bindingspartners van het atoom, die niet de vorm hebben van een tetraëder eromheen, maar plat als een trapezium. Deze regeling is doorgaans energetisch zeer ongunstig, toch zijn de moleculen zeer stabiel. Hun eigenschappen zijn tot nu toe volledig onbekend; onderzoekers willen ze nu verkennen. De resultaten worden gepubliceerd in de Tijdschrift van de American Chemical Society , maar zijn al online beschikbaar.
Net als zijn relatieve koolstof, silicium vormt in het algemeen vier bindingen met andere atomen. Wanneer het gebeurt, het resultaat is meestal een tetraëder. Het siliciumatoom bevindt zich in het midden, zijn bindingspartners (de zogenaamde liganden) op de tetraëdrische hoeken. Deze regeling is energetisch het gunstigst. Het ontstaat dus quasi automatisch, net zoals een zeepbel meestal bolvormig is.
Onderzoekers onder leiding van Prof. Dr. Alexander C. Filippou van het Instituut voor Anorganische Chemie aan de Universiteit van Bonn hebben nu siliciumbevattende moleculen geconstrueerd die zo ongewoon zijn als een kubusvormige zeepbel. In deze, de vier liganden vormen geen tetraëder, maar een vervormd vierkant, een trapezium. Ze liggen samen met het silicium in één vlak. "Ondanks dit, de verbindingen zijn zo stabiel dat ze zonder problemen in flessen kunnen worden gevuld en wekenlang kunnen worden bewaard, " legt Dr. Priyabrata Ghana uit, een voormalig promovendus die inmiddels is verhuisd naar de RWTH Aachen University.
Moleculaire exoten zijn ongewoon stabiel
De onderzoekers waren zelf verrast door deze ongewone stabiliteit. Ze ontdekten de reden door de moleculen op de computer te modelleren. De liganden vormen ook bindingen met elkaar. In het proces, ze vormen een stevig kader. Dit lijkt zo sterk te zijn dat het volledig voorkomt dat de trapeziumvormige opstelling in een tetraëder "klikt". "Onze computerberekeningen geven aan dat er geen structuur voor de moleculen is die energetisch gunstiger zou zijn dan de vlakke trapeziumvorm, " benadrukt Jens Rump, een doctoraatsstudent aan het Instituut voor Anorganische Chemie.
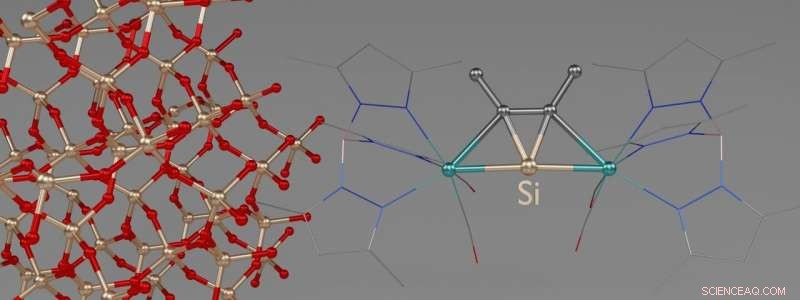
3D-weergave van een van de nieuwe moleculen. De linkerhelft van de afbeelding toont een doorsnede van de kristalstructuur van een kwartskristal met tetraëdrisch omgeven siliciumatomen. Krediet:Jens Rump / Universiteit van Bonn
De onderzoekers kweekten kristallen van de stoffen en bestraalden ze vervolgens met röntgenstralen. Het röntgenlicht wordt verstrooid door de atomen en verandert van richting. Deze afwijkingen kunnen dus gebruikt worden om de ruimtelijke structuur van de moleculen in het kristal te berekenen. Samen met spectroscopische metingen, deze methode bevestigde dat liganden en silicium inderdaad in hetzelfde vlak zitten in de nieuwe moleculen.
Hoewel de synthese van de exotische verbindingen onder inert gas moet gebeuren, het is verder relatief eenvoudig. Het produceren van de uitgangsmaterialen, anderzijds, is ingewikkeld; een van hen werd pas iets meer dan tien jaar geleden voor het eerst gesynthetiseerd en is al de bron geweest voor de synthese van verschillende nieuwe klassen van siliciumverbindingen.
De invloed van de ongebruikelijke structuur op de eigenschappen van silicium, een belangrijk element voor de elektronica-industrie, is op dit moment totaal onduidelijk. In ieder geval, lange tijd werd het als volledig onmogelijk beschouwd om dergelijke verbindingen te produceren.
 Luchtkwaliteit verbeterd tijdens lockdown in India, studie toont
Luchtkwaliteit verbeterd tijdens lockdown in India, studie toont Nieuw begrip van oceaanturbulentie kan klimaatmodellen verbeteren
Nieuw begrip van oceaanturbulentie kan klimaatmodellen verbeteren Parken haasten zich om omgevallen bomen op te ruimen, prullenbak na afsluiten
Parken haasten zich om omgevallen bomen op te ruimen, prullenbak na afsluiten Stanford-onderzoeker onderzoekt onbezongen held van de wetenschap:beoordeling
Stanford-onderzoeker onderzoekt onbezongen held van de wetenschap:beoordeling Kust Groenland hervormd naarmate het massaverlies van de Groenlandse ijskap versnelt
Kust Groenland hervormd naarmate het massaverlies van de Groenlandse ijskap versnelt
Hoofdlijnen
- Waarom was frenologie een rage in de Victoriaanse tijd?
- Oudste Homo Sapiens-fossielen die ooit zijn gevonden, suggereren een herschrijving van menselijke evolutie
- Wilde vogels:oplevende kalkoenen sparren met menselijke buren
- Een nieuw type robotmicroscoop
- Onderzoek onthult een nieuwe overlevingsstrategie in belangrijke bacteriën
- Wat zijn de stappen van de stikstofcyclus?
- Een eiwitduo zorgt ervoor dat de chromosomen in de voortplantingscellen hun significante andere vinden
- Hoe een eenvoudige microscoop te maken
- Soorten organellen
 Onderzoekers leggen uit hoe slangen in een rechte lijn kunnen kruipen
Onderzoekers leggen uit hoe slangen in een rechte lijn kunnen kruipen Hoe UTM Convergence
Hoe UTM Convergence Nieuwe microfluïdische methode breidt toolbox uit voor manipulatie van nanodeeltjes
Nieuwe microfluïdische methode breidt toolbox uit voor manipulatie van nanodeeltjes Gigantische verbetering van het magnetische effect zal de spintronica ten goede komen
Gigantische verbetering van het magnetische effect zal de spintronica ten goede komen 3 manieren om beter te studeren, volgens cognitief onderzoek
3 manieren om beter te studeren, volgens cognitief onderzoek Website voor het delen van gegevens kan de reactie op nieuwe illegale drugs versnellen
Website voor het delen van gegevens kan de reactie op nieuwe illegale drugs versnellen In enquêtes, mensen zeggen dat ze twee keer betalen wat ze eigenlijk willen uitgeven
In enquêtes, mensen zeggen dat ze twee keer betalen wat ze eigenlijk willen uitgeven Schaalbare prognoses voor IoT in de cloud
Schaalbare prognoses voor IoT in de cloud
- Elektronica
- Biologie
- Zonsverduistering
- Wiskunde
- French | Italian | Spanish | Portuguese | Swedish | German | Dutch | Danish | Norway |

-
Wetenschap © https://nl.scienceaq.com